SABCS 2017
5. bis 9. Dezember, San Antonio
- Mammakarzinom: neueste Daten vom SABCS 2017 zu Behandlung und Therapie
Prof. Dr. med. Michael Braun, Rotkreuzklinikum München Frauenklinik
 Was gibt es Neues in der Therapie des Mammakarzinoms? Diese Frage lässt sich anhand der aktuellen Studienergebnisse, die alljährlich beim San Antonio Breast Cancer Symposium (SABCS) vorgestellt werden, meist gut beantworten. In diesem Jahr fand der Kongress vom 5. bis 9. Dezember bereits zum vierzigsten Mal statt. Lesen Sie in unserem Bericht das Wichtigste vom SABCS kompakt zusammengefasst. Mit dabei sind diesmal unter anderem Ergebnisse der Gepar-7-Studie und der SUCCESS-A-Studie.
Was gibt es Neues in der Therapie des Mammakarzinoms? Diese Frage lässt sich anhand der aktuellen Studienergebnisse, die alljährlich beim San Antonio Breast Cancer Symposium (SABCS) vorgestellt werden, meist gut beantworten. In diesem Jahr fand der Kongress vom 5. bis 9. Dezember bereits zum vierzigsten Mal statt. Lesen Sie in unserem Bericht das Wichtigste vom SABCS kompakt zusammengefasst. Mit dabei sind diesmal unter anderem Ergebnisse der Gepar-7-Studie und der SUCCESS-A-Studie.
Liebe Kolleginnen und Kollegen,
seit seinen Anfängen im Jahr 1977 hat sich das San Antonio Breast Cancer Symposium (SABCS) von einem regionalen Treffen zum internationalen Kongress entwickelt. In diesem Jahr fand sein vierzigjähriges Jubiläum statt – und zwar vom 5. bis 9. Dezember.
Den über 7.000 Besuchern bot sich ein buntes Programm aus den aktuellen Forschungsergebnissen zum Mammakarzinom. Die relevanten Daten für die Klinik haben wir für Sie in bewährter Weise zusammengefasst. Freuen Sie sich auf Ergebnisse der deutschen Studien Gepar-7 und SUCCESS-A sowie auf Langzeitergebnisse zu dosisdichten Chemotherapien. Am Ende steht ein Ausblick auf vielversprechende neue Therapiekonzepte.
Ich würde mich freuen, wenn Sie mir eine Rückmeldung zum Bericht geben würden. Dies können Sie ganz einfach über die Funktion „Ihre Meinung ist wichtig“ tun. Ich hoffe, Ihnen mit dem Bericht eine informative und spannende Lektüre bieten zu können.
Mit kollegialen Grüßen
 Prof. Dr. med. Michael Braun, Rotkreuzklinikum München
Prof. Dr. med. Michael Braun, Rotkreuzklinikum München
Mammakarzinom: neueste Daten vom SABCS 2017 zu Behandlung und Therapie
Prof. Dr. med. Michael Braun, Rotkreuzklinikum München, Frauenklinik Taxisstraße
 Zum vierzigsten Mal fand in diesem Jahr das San Antonio Breast Cancer Symposium (SABCS) in Texas statt. Auf dem Jubiläumskongress wurden in bewährter Weise den über 7.000 Besuchern neueste Daten zur Grundlagen- und zur translationalen Forschung und zu deren Überführung in klinische Studien präsentiert. Wie schon in den Jahren zuvor schafften es auch heuer wieder Daten aus Deutschland in die Hauptvorträge der Konferenz – und zwar mit der Präsentation der Ergebnisse der Gepar-7-Studie und der SUCCESS-A-Studie. Weitere Themen waren neben Langzeitergebnissen zu dosisdichten Chemotherapiekonzepten und der endokrinen Therapie der prämenopausalen Patientin unter anderem aktuelle Daten zu Inhibitoren der cyclinabhängigen Kinase 4/6 (CDK4/6) und der Poly(Adenosindiphosphat-Ribose)-Polymerase 1 (PARP).
Zum vierzigsten Mal fand in diesem Jahr das San Antonio Breast Cancer Symposium (SABCS) in Texas statt. Auf dem Jubiläumskongress wurden in bewährter Weise den über 7.000 Besuchern neueste Daten zur Grundlagen- und zur translationalen Forschung und zu deren Überführung in klinische Studien präsentiert. Wie schon in den Jahren zuvor schafften es auch heuer wieder Daten aus Deutschland in die Hauptvorträge der Konferenz – und zwar mit der Präsentation der Ergebnisse der Gepar-7-Studie und der SUCCESS-A-Studie. Weitere Themen waren neben Langzeitergebnissen zu dosisdichten Chemotherapiekonzepten und der endokrinen Therapie der prämenopausalen Patientin unter anderem aktuelle Daten zu Inhibitoren der cyclinabhängigen Kinase 4/6 (CDK4/6) und der Poly(Adenosindiphosphat-Ribose)-Polymerase 1 (PARP).
Adjuvante Therapie
Dosisdichte Therapie
Die Early Breast Cancer Trialist Group (EBCTG) machte mit einer Metaanalyse zur Effektivität der dosisdichten und der sequentiellen Chemotherapien den Auftakt einer Reihe hochinteressanter Vorträge. Die Grundlage für das dosisdichte Konzept ist die sogenannte Norton-Simon-Hypothese, nach der die Absterberate von Tumorzellen als Ergebnis der zytotoxischen Therapie direkt proportional zur Tumorwachstumsrate zum Zeitpunkt der Behandlung ist.
Richard Gray stellte hierzu die gepoolten Daten aus 25 Studien mit insgesamt über 34.000 Patientinnen vor [1]. Während eine Dosiseskalation nicht zu einer Verbesserung des Outcomes führte, erreichte man durch die Verkürzung der Therapieintervalle und/oder durch die sequentielle Verabreichung der Chemotherapie eine signifikante Reduktion der Rezidivrate um 15% und eine Senkung der brustkrebsspezifischen Mortalität um 13%.
Diese Verbesserung des Outcomes trat unabhängig vom Hormonrezeptorstatus oder anderen Tumor- oder Patientencharakteristika auf. Sie lag in der Größenordnung der Effektivitätssteigerung, die wir durch die Einführung der Taxane im Vergleich zu den reinen Anthrazyklinschemata beobachten konnten. Des Weiteren konnte nachgewiesen werden, dass die Dosisintensivierung nicht mit einer Verschlechterung der therapieassoziierten Mortalität einhergeht.
Somit konnten nun die bereits 2003 von Marc Citron publizierten Ergebnisse der CALBG-9741-Studie nach mehr als 14 Jahren bestätigt werden [2]. Danach wird das klinische Outcome von Brustkrebspatientinnen durch eine Erhöhung der Dosisdichte signifikant verbessert.
Fazit
- Die dosisdichte und sequentielle Therapie (viermal Epirubicin+Cyclophosphamid [EC] alle drei Wochen und zwölfmal Paclitaxel wöchentlich), wie wir sie seit Jahren in Deutschland durchführen, wurde mit dieser großen Übersichtsarbeit eindrucksvoll als Goldstandard bestätigt.
- Der Vorteil ist dabei von der Tumorbiologie unabhängig.
„Wenn wir Patientinnen identifiziert haben, deren Risiko wir als hoch genug einschätzen, um eine Chemotherapie durchzuführen, dann sollten wir ein dosisdichtes Schema wählen, wenn es die Konstitution der Patientin zulässt.“ Prof. Dr. med. Michael Braun
Trastuzumab bei Patientinnen mit HER2-low-Tumoren
Das Problem geeigneter Cut-off-Werte für die HER2neu-Bestimmung in der klinischen Anwendung wurde vor zehn Jahren durch Beobachtungen der NSABP-B31- und der N9831-Studie deutlich [3]. Darin wiesen 10% der Patientinnen, die mit Trastuzumab behandelt wurden, in der zentralen Testung weder eine HER2-Amplifikation noch eine Überexpression auf. Erstaunlich war, dass diese Patientinnen dennoch von einer Trastuzumabtherapie profitierten. Die Frage, ob somit die derzeit gültige Definition für HER2neu-Positivität haltbar ist, sollte in der NSABP-B-47-Studie untersucht werden [4]. In diese Studie wurden Patientinnen mit einem nodalpositiven oder einem high-risk nodalnegativen Mammakarzinom mit sogenannten HER2-low-Tumoren (Immunhistochemie[IHC]-Sore 1+ und 2+). Nach der Randomisierung erhielt je die Hälfte der 3.270 Patientinnen entweder eine alleinige Chemotherapie oder zusätzlich Trastuzumab für ein Jahr.
Nach einem medianen Follow-up von 46,1 Monaten zeigte sich weder für das erkrankungsfreie Überleben (DFS; Hazard Ratio [HR] 0,98; Abb. 1) noch für das Gesamtüberleben (OS; HR 1,33) ein Unterschied zwischen beiden Patientengruppen.
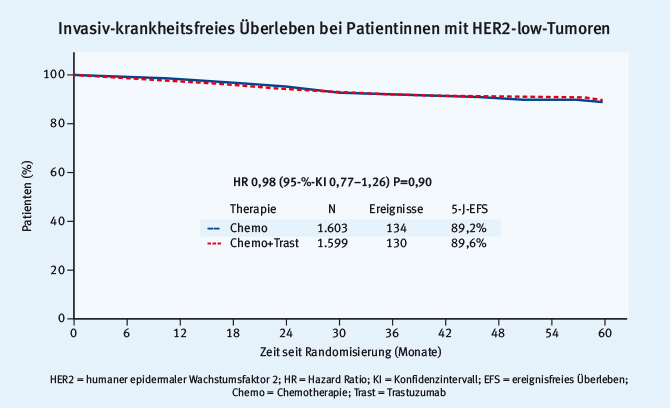 Abb. 1: Patientinnen mit HER2-low-Tumoren profitieren nicht von der Hinzunahme von Trastuzumab zu einer zytotoxischen Chemotherapie (modifiziert nach [4])
Abb. 1: Patientinnen mit HER2-low-Tumoren profitieren nicht von der Hinzunahme von Trastuzumab zu einer zytotoxischen Chemotherapie (modifiziert nach [4])In dieser Studie waren 78,5% der Patientinnen nodalpositiv und 26,1% wiesen mehr als drei positive Lymphknoten auf. Trotzdem konnte ein gutes 5-Jahres-iDFS von 89,2% für die alleinige Chemotherapie beziehungsweise 89,6% für die Kombination der Chemotherapie mit Trastuzumab gezeigt werden.
Es besteht somit kein Vorteil für die Hinzunahme einer Trastuzumabtherapie bei Patientinnen mit einer Fluoreszenz-in-situ-Hybridisierungs(FISH)-Ratio <2,0 und einer IHC-Färbeintensität von 1+ und 2+.
Fazit
- Diese Studie beweist abschließend, dass Trastuzumab nur bei HER2neu-positiven (Dako-Score 3+ oder FISH/IHC-positiv) Tumoren wirkt.
- Gleichzeitig wird die Wichtigkeit exakter und reproduzierbarer Bestimmungsmethoden herausgestellt, um Unter- oder Übertherapien zu vermeiden.
Bisphosphonate in der adjuvanten Behandlung des Mammakarzinoms
In den aktuellen ASCO-Guidelines wird die adjuvante Gabe von Bisphosphonaten bei sicher postmenopausalen Patientinnen (natürlich entstanden oder durch Gonadotropin-Releasing-Hormon [GnRH] induziert) für drei bis fünf Jahre (Zoledronat 4 mg halbjährlich) oder zwei bis drei Jahre (Clodronat 1600 mg/d oral) empfohlen [5]. Zur geeigneten Therapiedauer gibt es bisher keine Daten. Von Wolfgang Janni wurden zu diesem Thema die Ergebnisse der deutschen SUCCESS-A-Studie präsentiert [6]. In dieser randomisierten Open-Label-Phase-III-Studie (2 x 2 factorial design) wurden Patientinnen mit einem frühen Mammakarzinom und hohem Rückfallrisiko randomisiert für drei Zyklen 5-Fluorouracil+Epirubicin+Cyclophosphamid (FEC), gefolgt von Docetaxel mit oder ohne Gemcitabin. Im Anschluss an die Chemotherapie erfolgte eine weitere Randomisierung in
- fünf Jahre Zoledronat (4 mg i.v. alle drei Monate für zwei Jahre, gefolgt von 4 mg i.v. alle sechs Monate für drei Jahre) versus
- zwei Jahre Zoledronat (4 mg i.v. alle drei Monate für zwei Jahre).
Insgesamt erhielten 3.421 von 3.754 Patientinnen in der SUCCESS-A-Studie mindestens einen Zyklus Zoledronat. Für die Analyse standen 2.987 Patientinnen (1.540 für fünf Jahre und 1.447 für zwei Jahre einer Zoledronattherapie) zur Verfügung. Bezüglich DFS und adaptiertem OS gab es keinen signifikanten Unterschied zwischen den beiden Behandlungsdauern. Im Fünfjahresarm traten allerdings mehr Nebenwirkungen auf. Dies traf unabhängig vom Menopausenstatus zu.
Auch für die reine ossäre Metastasierung gab es bezüglich der Bisphosphonatgabe keinen Vorteil für eine längere Gabe. Die längere Zoledronatgabe führte hingegen zu einer Verdoppelung der Nebenwirkungen.
Fazit
- Einschränkungen der SUCCESS-A-Studie sind eine relativ kurze Nachbeobachtungszeit und die Verabreichung des Bisphosphonats in dreimonatigen Intervallen.
- Trotzdem kann die in unseren Tumorboards gängige Empfehlung, sicher postmenopausalen Patientinnen Zoledronat 4 mg halbjährlich für drei Jahre anzubieten, als ausreichend angesehen werden.
Einsatz von nab-Paclitaxel neoadjuvant und in der Erstlinie
Der neoadjuvante Einsatz von nab-Paclitaxel führt im Vergleich zu lösungsmittelhaltigem Paclitaxel insbesondere bei tripelnegativen Tumoren zu einer Erhöhung der Rate von pathologisch bestätigten kompletten Remissionen (pCR). Dies konnte unter anderem in der Gepar-Septo-Studie gezeigt werden [7]. Von Andreas Schneeweiss wurden jetzt Ergebnisse der prospektiv randomisierten Phase-III-Gepar-7-Studie präsentiert [8]. Bei Patientinnen mit einem tripelnegativen Mammakarzinom cT2 bis cT4, cT1c N1+ oder high-risk N0 wurden neoadjuvant zwölf Wochen nab-Paclitaxel (150 mg/m2 wöchentlich, nach einem Amendment 125 mg/m2 wöchentlich) mit Paclitaxel (80 mg/m2 wöchentlich), jeweils gefolgt von viermal EC (Epirubicin 90 mg/m2 und Cyclophosphamid 600 mg/m2 an Tag 1 alle drei Wochen) verglichen. HER2-positive Patientinnen erhielten zusätzlich alle drei Wochen Trastuzumab und Pertuzumab. Hervorgehoben werden muss, dass die Dosierung von initial 150 mg/m2 nab-Paclitaxel nach der Rekrutierung von 464 Patientinnen auf 125 mg/m2 reduziert wurde.
Die Daten zur pathologischen Komplettremission, dem primären Endpunkt der Studie, wurden schon 2016 von Michael Untch publiziert [9]. Die pCR konnte durch die Anwendung von nab-Paclitaxel von 29% mit Paclitaxel auf 38% signifikant gesteigert werden (p<0,001; Abb. 2). In der Gruppe der tripelnegativen Tumoren war dieser Vorteil am deutlichsten (48% vs. 26%, p<0,001).
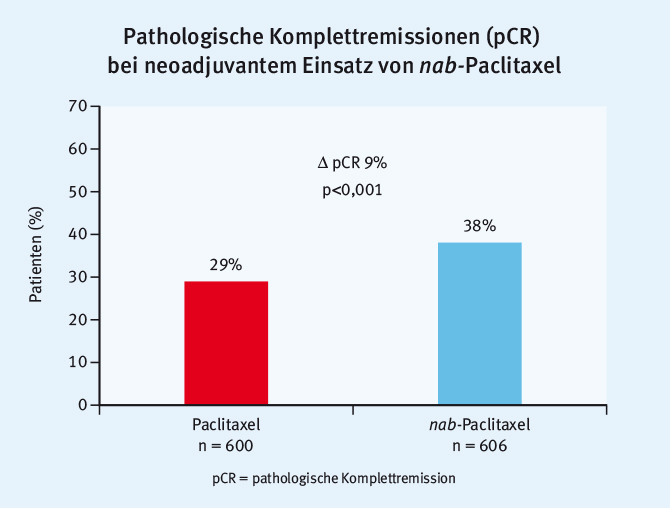 Abb. 2: Pathologische Komplettremissionen als primärer Endpunkt der Gepar-Septo-Studie (modifiziert nach [9])
Abb. 2: Pathologische Komplettremissionen als primärer Endpunkt der Gepar-Septo-Studie (modifiziert nach [9])Die jetzt vorgestellten Daten sollten zeigen, ob sich dieser pCR-Vorteil für nab-Paclitaxel auch in eine Verbesserung des Outcomes übersetzt. Dies konnte eindrucksvoll demonstriert werden [8]: Das DFS wurde nach einem medianen Nachbeobachtungszeitraum von 49 Monaten von 80,7% für Paclitaxel auf 87,1% für nab-Paclitaxel um absolut 6,4% (HR 0,69; p=0,0044) verbessert (Abb. 3).
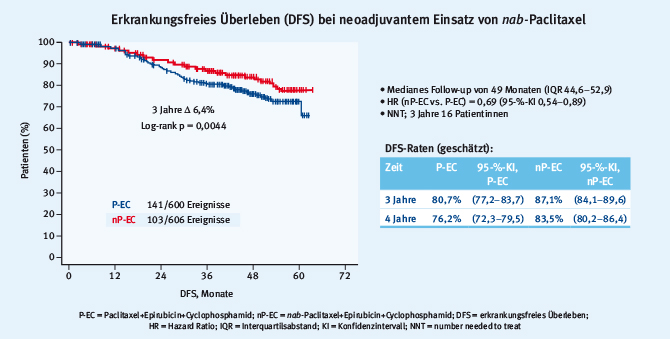 Abb. 3: Der neoadjuvante Einsatz von nab-Paclitaxel zeigt Vorteile im erkrankungsfreien Überleben nach 49 Monaten Follow-up (modifiziert nach [8])
Abb. 3: Der neoadjuvante Einsatz von nab-Paclitaxel zeigt Vorteile im erkrankungsfreien Überleben nach 49 Monaten Follow-up (modifiziert nach [8])Im tripelnegativen Kollektiv lag der Vorteil, der vermutlich alleine aufgrund der niedrigen Fallzahlen in dieser Subgruppenanalyse gerade nicht mehr signifikant war, für den experimentellen Arm sogar bei etwa 10% (HR nP+EC zu P+EC 0,66; p=0,0694). Überaschenderweise ergab sich auch für die hormonrezeptorpositive/HER2neu-negative Gruppe eine Verbesserung des DFS durch nab-Paclitaxel um 8% (HR 0,71; p= 0,0660). Es profitierten alle Subgruppen von der Prüfsubstanz, unter anderem auch die weniger proliferierenden Tumoren mit einem Ki67 von ≤20%. Ein Vorteil für das Gesamtüberleben konnte nicht nachgewiesen werden. Nach Aussage der Autoren traten die Rezidive zu einem hohen Prozentsatz als Fernmetastasen auf, sodass nach längerer Nachbeobachtung ein Überlebensvorteil zu erwarten ist.
Unabhängig von der Art der Therapie übersetzte sich die pCR in ein besseres DFS. Patientinnen, die keine pCR erreichten, profitierten signifikant häufiger von nab-Paclitaxel. Die unter nab-Paclitaxel aufgetretenen Neuropathien von Grad 3 und 4 konnten durch die Dosisreduktion von 150 mg/m2 auf 125 mg/m2 von 15% auf 8% reduziert werden [9].
Fazit
- Diese Daten unterstreichen den Stellenwert von nab-Paclitaxel beim tripelnegativen Mammakarzinom.
- Es wird in der weiteren Analyse untersucht werden müssen, ob diese guten Ergebnisse auch für die Gruppe der Patientinnen zutreffen, die ausschließlich eine niedrigere Dosierung (125 mg/m2) erhielten.
Erstlinientherapien
Nab-Paclitaxel
Eine weitere Studie zum Einsatz von nab-Paclitaxel, die CALBG-40502-Studie, unterstreicht noch einmal dessen besondere Wirksamkeit bei tripelnegativen Tumoren [10]. Dabei handelt es sich um eine randomisierte Phase-III-Studie für Patientinnen mit metastasiertem und lokal rezidiviertem Mammakarzinom. Als Erstlinientherapie wurde Paclitaxel (P 90mg/m2) mit Ixabepilon (IX 16 mg/m2) und nab-Paclitaxel (nP 150 mg/m2) verglichen. 98% der Patientinnen erhielten zusätzlich Bevacizumab alle zwei Wochen. Wie bereits 2015 publiziert [11], war Ixabepilone Paclitaxel in seiner Effektivität unterlegen und nab-Paclitaxel (mit 150 mg/m2) in dieser Studie dem lösungsmittelhaltigen Paclitaxel bei schlechterer Verträglichkeit nicht überlegen. Nach nun fünf Jahren Follow-up wurden diese Beobachtungen bestätigt. Der Effekt von nab-Paclitaxel unterschied sich jedoch je nach Tumorsubtyp.
Während Paclitaxel bei Patientinnen mit hormonrezeptorpositiven Tumoren Ixabepilon und nab-Paclitaxel überlegen war, weist nab-Paclitaxel auch in dieser Studie bei tripelnegativen Tumoren bezüglich des progressionsfreien Überlebens (PFS; HR 0,79) und OS (HR 0,74) einen deutlichen Trend zur Überlegenheit gegenüber Paclitaxel auf.
Fazit
- Die Überlegenheit von nab-Paclitaxel im tripelnegativen Kollektiv zeigt sich, zumindest für die Dosierung von 150 mg/m2, auch in dieser Phase-III-Studie bei metastasierten Patientinnen.
- Interessant wären auch hier Daten für die 125-mg/m2-Dosis, allerdings fand in dieser Studie keine Anpassung der Dosis statt.
Endokrine Therapie
Dauer der Aromatasehemmertherapie
Bei Luminaltumoren treten 50% der Rezidive nach fünf Jahren auf. Es stellt sich also die Frage, ob postmenopausale Patientinnen mit einem hormonrezeptorpositiven Mammakarzinom nach fünf Jahren einer adjuvanten endokrinen Therapie von einer längeren Einnahmedauer profitieren. Zum Thema der „erweiterten Adjuvanz“ wurden bereits im letzten Jahr im Rahmen des SABCS die lange erwarteten Ergebnisse der MA17R-, der DATA- und der IDEAL-Studie präsentiert, wobei die Ergebnisse eher ernüchternd waren [12, 13, 14]. Bezüglich des krankheitsfreien Überlebens wurde ein marginal signifikanter Vorteil vor allem für Patientinnen mit höherem Mammakarzinomrisiko (beispielsweise nodalpositive Patientinnen) nachgewiesen, wenn diese länger als fünf Jahre therapiert wurden. Für das Gesamtüberleben konnte kein signifikanter Vorteil nachgewiesen werden.
Weitere Informationen in diesem Kontext wurden nun von den Ergebnissen der ABCSG-16-Studie erwartet, die von Michael Gnant aus Österreich vorgetragen wurden [15]. Verglichen wurde die Gabe von Anastrozol für weitere zwei Jahre mit einer Gabe für weitere fünf Jahre, nachdem bereits vier bis sechs Jahre eine endokrine Therapie eingenommen worden war.
Nach einem medianen Follow-up von knapp neun Jahren (106,2 Monaten) zeigte sich kein Vorteil für eine längere Gabe von Anastrozol über zwei Jahre der erweiterten Therapie hinaus.
Die Therapieadhärenz war, wie zu erwarten, während der zusätzlichen Fünfjahrestherapie schlechter als während der zweijährigen Therapie. Die Frakturrate stieg von 4,7% nach zwei Jahren erweiterter Anastrozolgabe um ein Drittel auf 6,3% an (HR 1,353; p=0,053). Die Autoren schließen aus den Ergebnissen der Studie, dass nach fünf Jahren einer endokrinen Therapie (fünf Jahre Tamoxifen, Tamoxifen für zwei bis drei Jahre und Switch auf einen Aromatasehemmer für zwei bis drei Jahre oder fünf Jahre Aromatasehemmer) zwei zusätzliche Jahre Anastrozol ausreichend sind. Eine längere Gabe geht mit mehr Frakturen einher, ohne einen zusätzlichen Nutzen zu generieren. Ob die zusätzlichen zwei Jahre einer Anastrozoltherapie besser sind als die alleinige Switchtherapie, kann die Studie leider nicht beantworten.
Fazit
- Für die Praxis gilt weiterhin: Nach fünf Jahren Tamoxifen werden fünf Jahre Aromatasehemmer empfohlen.
- Nach einer Switchtherapie (zwei bis drei Jahre Tamoxifen, gefolgt von zwei bis drei Jahren Aromatasehemmer) kann bei hohem Risiko und guter Verträglichkeit der Aromatasehemmer für volle fünf Jahre weitergegeben werden.
- Nach der Upfront-Therapie von fünf Jahren mit einem Aromatasehemmer gibt es keine Evidenz für eine Erweiterung der Therapie.
- Sollte bei guter Verträglichkeit, hohem Rückfallrisiko und hohem Sicherheitsbedürfnis der Patientin eine längere Therapie geplant sein, muss über eine erhöhte Frakturrate aufgeklärt werden.
Einsatz von GnRH-Analoga zur Ovarprotektion während einer (neo-)adjuvanten Chemotherapie
Dr. Matteo Lambertini präsentierte die Ergebnisse einer Metaanalyse zum Thema der Ovarprotektion durch die Gabe eines GnRH-Analogons eine Woche vor und während einer adjuvanten Chemotherapie [16]. In der Studie wurden die individuellen Daten von fünf randomisierten Studien ausgewertet (PROMISE-, POEMS-, Anglo-Celtic-Group-OPTION-, ZORO- und Moffitt-Studie). Das vorzeitige Auftreten einer Ovarialinsuffizienz konnte von 30,9% in der Kontrollgruppe auf 14,1% in der GnRHa-Gruppe gesenkt werden (Abb. 4).
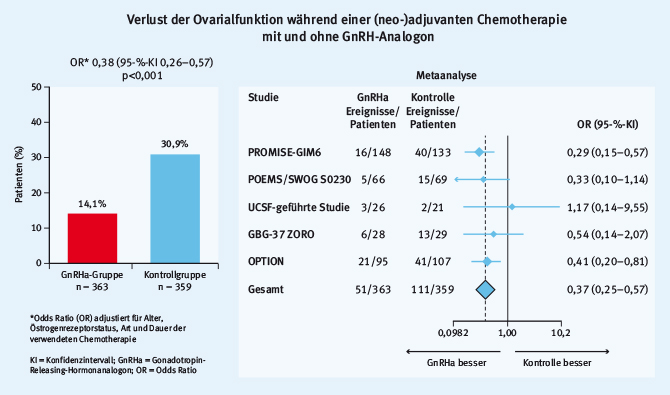 Abb. 4: Der Verlust der Ovarialfunktion konnte durch den Einsatz eines GnRH-Analogons reduziert werden (modifiziert nach [16])
Abb. 4: Der Verlust der Ovarialfunktion konnte durch den Einsatz eines GnRH-Analogons reduziert werden (modifiziert nach [16])Ein Unterschied bezüglich der Amenorrhoerate zeigte sich erst nach zwei Jahren zugunsten der GnRHa-Gruppe (18,2% vs. 30,0%). Dieser Effekt war unabhängig vom Rezeptorstatus, dem Typ und der Dauer der Chemotherapie sowie dem Alter der Patientin zum Zeitpunkt der Diagnose. In der GnRHa-Gruppe wurden mit 37 von 359 (10,3%) Patientinnen signifikant mehr Frauen schwanger als in der Kontrollgruppe mit 20 von 367 (5,5%).
Bezüglich der Sicherheit des Einsatzes der Ovarialprotektion wurde das onkologische Outcome beobachtet. So konnte für den Einsatz der GnRH-Analoga kein signifikanter Nachteil in Bezug auf das krankheitsfreie und das Gesamtüberleben nachgewiesen werden. Dies gilt unabhängig vom Hormonrezeptorstatus.
Fazit
- Entsprechend der aktuellen Empfehlungen der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) sollten prämenopausale Patientinnen immer über die Möglichkeit der Ovarprotektion mit einem GnRH-Analogon aufgeklärt werden.
- Bei dringendem Kinderwunsch stehen darüber hinaus die Kryokonservierung von befruchteten und unbefruchteten Eizellen oder von Eierstockgewebe zur Verfügung.
SOFT-TEXT-Update
Gemeinsame Auswertung
Das Update der kombinierten Daten der SOFT- und TEXT-Studie wurde mit einem Follow-up von nunmehr neun Jahren von Prue Francis präsentiert [17]. In diesem prämenopausalen Patientenkollektiv konnte der statistisch signifikante Vorteil für den Aromatasehemmer gegenüber Tamoxifen jeweils in Kombination mit einem GnRH-Analogon in Bezug auf das DFS bestätigt werden (HR 0,77; p=0,0006). Der Vorteil lag für das fernmetastasenfreie Überleben bei circa 2%. Ein Vorteil für das Gesamtüberleben konnte in der kombinierten Analyse nicht nachgewiesen werden. Dieses war insgesamt aber mit 93,4% und 93,3% nach neun Jahren erfreulich gut. Muskuloskelettale Symptome und Osteoporose waren wie zu erwarten im Aromatasehemmerarm höher.
Fazit
- Nach nunmehr neun Jahren zeigt sich ein DFS-Vorteil von 4% für den Aromatasehemmer gegenüber Tamoxifen, wenn dieser jeweils mit einem GnRH-Analogon kombiniert wird.
- Das Gesamtüberleben kann nicht verbessert werden. Die Toxizität ist allerdings bei Einnahme eines Aromatasehemmers erhöht.
SOFT-Studie: 8-Jahres-Follow-up
Die alleinige Auswertung der SOFT-Studie wurde im Anschluss von Gini Fleming präsentiert [18]. Hier ergab die Hinzunahme eines GnRH-Analogons zu Tamoxifen im Vergleich zur alleinigen Gabe von Tamoxifen nach acht Jahren Follow-up einen signifikanten Vorteil von absolut 4,3% (HR 0,76; p=0,009) im DFS. Jüngere Patientinnen profitierten hierbei mehr von der Kombination mit einem GnRH-Analogon. Dieser Vorteil war vor allem für diejenigen Patientinnen nachweisbar, die zuvor eine Chemotherapie erhalten hatten. Er konnte durch die Hinzunahme von Exemestan zur GnRH-Analogatherapie um 2,7% nur leicht verbessert werden. Ein leichter Vorteil für das Gesamtüberleben gegenüber der alleinigen Tamoxifen-Gabe war dagegen nur für die Kombination des GnRH-Analogons mit Tamoxifen nachweisbar, bei allerdings kleinen Fallzahlen.
Die Einnahme von Exemestan führte zu einer Zunahme von Nebenwirkungen (zum Beispiel muskuloskelettal und Osteoporose), die zu einem vorzeitigen Abbruch der endokrinen Therapie bei 27,8% der Patientinnen führte. Dagegen brachen nur 18,5% der Patientinnen die Therapie ab, wenn Tamoxifen mit einem GnRH-Analogon kombiniert wurde.
Fazit
- Jungen prämenopausalen Patientinnen, deren Rückfallrisiko als so hoch eingeschätzt wird, dass eine Chemotherapie durchgeführt wird, muss die Kombination der endokrinen Therapie mit einem GnRH-Analogon angeboten werden.
- Insbesondere bei Patientinnen unter 35 Jahren kann in diesem Zusammenhang die Kombination mit einem Aromatasehemmer erwogen werden.
„Die insgesamt geringen absoluten Vorteile in Bezug auf das DFS und insbesondere auf das fernmetastasenfreie Überleben ohne das Vorliegen eines klaren Benefits für das Gesamtüberleben müssen im klinischen Alltag in jedem Fall gegen die möglichen substantiellen Nebenwirkungen der Ovarablation und besonders des Aromatasehemmers abgewogen werden. Dabei gilt die Prämisse, dass diejenige Therapie die beste ist, die auch eingenommen wird. Dies wird im Zweifelsfall immer die Therapie mit den geringsten Nebenwirkungen sein.“ Prof. Dr. med. Michael Braun
CDK4/6-Inhibitoren
Ribociclib
Die Erfolgsgeschichte der CDK4/6-Inhibitoren wurde auch auf diesem Kongress mit der Präsentation der Ergebnisse der MONALEESA-7-Studie fortgeschrieben [19]. Erstmals wurde hier mit Ribociclib ein CDK4/6-Inhibitor in einem rein prä- oder perimenopausalen Kollektiv von Patientinnen mit fortgeschrittenem Brustkrebs eingesetzt. In der randomisierten, placebokontrollierten, doppelt verblindeten Phase-III-Studie wurden 672 Frauen mit fortgeschrittenem hormonrezeptorpositivem, HER2neu-negativem Mammakarzinom vor und während der Menopause (zwischen 25 und 58 Jahren) mit Goserelin in Kombination mit einer oralen Hormontherapie (Tamoxifen oder einem nichtsteroidalen Aromatasehemmer) plus Ribociclib oder einem Placebo behandelt.
Die Patientinnen durften vor Einschluss in die Studie keine endokrine Therapie und maximal eine Linie Chemotherapie in der Metastasierung erhalten haben. Die Hinzunahme des CDK4/6-Inhibitors war der alleinigen endokrinen Therapie in Bezug auf das PFS hochsignifikant überlegen (p=0,0000000983). Das mediane progressionsfreie Überleben lag im CDK4/6-Arm bei 23,8 Monaten und im Placeboarm bei 13,0 Monaten (HR 0,553; Abb. 5).
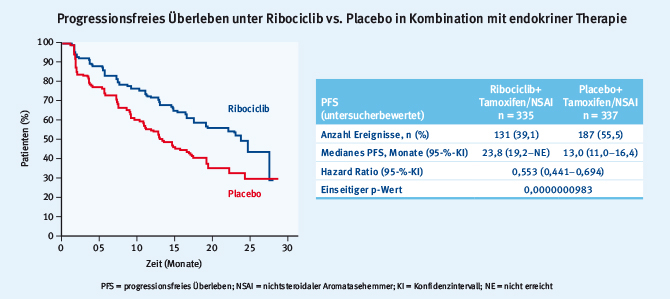 Abb. 5: Ribociclib führt in Kombination mit einer endokrinen Therapie gegenüber dem Placebo zu einer signifikanten Verbesserung des progressionsfreien Überlebens (modifiziert nach [19])
Abb. 5: Ribociclib führt in Kombination mit einer endokrinen Therapie gegenüber dem Placebo zu einer signifikanten Verbesserung des progressionsfreien Überlebens (modifiziert nach [19])Hierbei bewegt sich die Ansprechrate von Patientinnen mit messbarer Erkrankung mit 51% für eine endokrine Therapie auf einem sehr hohen Niveau. Auch die Lebensqualität konnte durch die Hinzunahme von Ribociclib signifikant verbessert werden, wobei unter anderem schon nach acht Wochen eine nachhaltige Verbesserung der Schmerzen im CDK4/6-Inhibitorarm gemessen wurde.
Fazit
- MONALEESA-7 ist somit die erste Phase-III-Studie, in der ein CDK4/6-Inhibitor exklusiv in der prä- und perimenopausalen Altersgruppe seine Effektivität beweist.
- Dieser Effekt trifft für alle Subgruppen und unabhängig vom endokrinen Partner (Tamoxifen oder nichtsteroidaler Aromatasehemmer) zu.
- Die durchgeführte Lebensqualitätsanalyse ist bei der Bewertung des Stellenwertes einer palliativen Therapie äußerst wertvoll und sollte standardisiert in zukünftigen Studien in diesem Setting durchgeführt werden.
„Diese Studie ist ein guter Beweis für die Effektivität einer endokrinen Therapieoption in der Prämenopause, deren Einsatz in der Postmenopause schon gesichert wurde. Zukünftige Studien sollten schon initial unabhängig vom Menopausenstatus durchgeführt werden, um die aufwändige Durchführung separater Studien für prämenopausale Patientinnen vermeiden zu können.“ Prof. Dr. med. Michael Braun
Abemaciclib
Als weiterer oraler CDK4/6-Inhibitor wurde Abemaciclib bei fortgeschrittenem hormonrezeptorpositivem, HER2neu-negativem Mammakarzinom in Kombination mit Fulvestrant (MONARCH-2-Studie) oder einem nichtsteroidalen Aromatasehemmer (MONARCH-3) eingesetzt. Matthew Goetz präsentierte eine explorative Analyse kombinierter Daten aus beiden Studien zur Wirksamkeit in prognostischen Subgruppen [20].
Es konnte gezeigt werden, dass der zusätzliche Einsatz von Abemaciclib zur endokrinen Therapie in allen Subgruppen aktiv war. Dieser Vorteil war vor allem bei Patientinnen mit einer viszeralen Metastasierung, hoher Tumorlast und ungünstigen Tumoreigenschaften (negativer Progesteronrezeptorstatus, G3 etc.) ausgeprägt.
Insbesondere Patientinnen, die weniger als 36 Monate eines tumorfreien Intervalls aufwiesen, profitierten von der Hinzunahme des CDK4/6-Inhibitors. Diese Aussage muss allerdings mit Vorsicht betrachtet werden. Es ist nicht belegt, dass Patientinnen mit einem längeren therapiefreien Intervall nicht von dieser Therapie profitieren.
Fazit
- Abemaciclib als der dritte CDK4/6-Inhibitor neben Palbociclib und Ribociclib hat in dieser gepoolten Analyse seine Effektivität beim metastasierten Mammakarzinom insbesondere bei Patientinnen mit früher Wiedererkrankung und ungünstigen Tumoreigenschaften bewiesen.
- Eine Patientinnengruppe, die nicht von einer CDK4/6-Inhibition profitiert, ist weiterhin nicht identifiziert.
PARP-Inhibitoren
Die gute Datenlage zum Einsatz von PARP-Inhibitoren wurde nun durch die positiven Ergebnisse der EMBRACA-Studie gefestigt [21]. In dieser Phase-III-Studie wurde der orale PARP-Inhibitor Talazoparib bei Patientinnen mit fortgeschrittenem HER2neu-negativem Mammakarzinom, die eine BRCA1- oder BRCA2-Mutation aufwiesen, als Monotherapie eingesetzt. Im Kontrollarm konnte der Therapeut je nach eigenem Dafürhalten Capecitabin, Eribulin, Gemcitabin oder Vinorelbin einsetzen.
Der primäre Endpunkt der Studie war das progressionsfreie Überleben. Dieses konnte durch den PARP-Inhibitor nach 11,2 Monaten Follow-up von medianen 5,6 Monaten im Kontrollarm auf 8,6 Monate im experimentellen Arm signifikant (HR 0,54; p<0,0001) erhöht werden und dies bei einem hervorragenden Anteil von 68,6% (HR 4,28) der Patientinnen ohne Progress.
In dieser bisher größten PARP-Studie zeigte sich die Therapie als insgesamt gut verträglich und führte zu einer signifikanten Verbesserung der Lebensqualität und des allgemeinen Gesundheitsstatus (HR 0,38, p<001).
Fazit
- Der Einsatz der PARP-Inhibitoren bei metastasierten Patientinnen mit nachgewiesener BRCA1- oder -2-Mutation scheint sich als neuer Goldstandard durchzusetzen.
Sacituzumab Govitecan
Am Mittwochvormittag wurden die Effektivitätsdaten zu Sacituzumab Govitecan beim metastasierten tripelnegativen Mammakarzinom vorgestellt [22]. Dabei handelt es sich um ein humanisiertes Antikörper-Wirkstoff-Konjugat aus dem monoklonalen Antikörper TROP2 und SN-38, dem aktiven Metaboliten von Irinotecan. Die stark vortherapierten Patientinnen erhielten nach mindestens zwei Therapielinien (41% nach drei Therapielinien und 59% nach vier und mehr Therapielinien) einer palliativen Chemotherapie bei Fortschreiten der Erkrankung Sacituzumab Govitecan 10 mg/m2 an den Tagen 1 und 8 alle drei Wochen.
Der Wirkstoff zeigte in der ≥3. Therapielinie eine clinical benefit rate von 45% bei einer Gesamtansprechrate (ORR) von 34%. Die Ansprechraten waren mit medianen 7,6 Monaten andauernd. Grad-3- und -4-Nebenwirkungen waren vor allem hämatologisch und beherrschbar. Schwere Neutropenien traten in 41% auf, febrile Neutropenien in 7%. Nur zwei Patientinnen (1,8%) mussten die Therapie aufgrund von Nebenwirkungen abbrechen.
Fazit
- Die vorgestellten Studienergebnisse sind sehr vielversprechend.
- Dieser auch in späten Therapielinien sehr effektive Wirkstoff wird derzeit in mehreren Studien in Kombination mit herkömmlichen Therapeutika überprüft.
Ausblick
Zirkulierende Tumor-DNA (ctDNA)
Der Nachweis zirkulierender Tumor-DNA (ctDNA) im Blut wird zusammen mit zirkulierenden Tumorzellen (CTCs) auch als Liquid Biopsy bezeichnet. An diesem leicht zugänglichen Material wird in Studien zunehmend nach Mutationen gesucht, die als Target für eine zielgerichtete Therapie dienen können. Die Daten der Proof-of-Concept-Studie BELLE-2 wurden bereits auf dem SABCS 2015 von José Baselga gezeigt. Damit konnte belegt werden, dass Patientinnen mit einer an ctDNA nachgewiesenen Mutation der Phosphoinositid-3-Kinase (PI3K) signifikant besser auf die Behandlung mit dem PI3K-Inhibitor Buparlisib ansprachen als Patientinnen mit unmutierter ctDNA [23].
Für die Behandlung mit CDK4/6-Inhibitoren wird derzeit noch nach einem geeigneten prädiktiven Marker gesucht. So auch in der MONALEESA-2-Studie. In dieser Studie führte die Hinzunahme des CDK4/6-Inhibitors Ribociclib zu dem nichtsteroidalen Aromatasehemmer Letrozol im Vergleich zu einem Placebo bei Patientinnen mit einem hormonrezeptorpositiven, HER2neu–negativen metastasierten Mammakarzinom zu einer signifikanten Verbesserung des progressionsfreien Überlebens [24].
In der nun von Hortobagyi präsentierten translationalen Untersuchung [25] wurde in Blutproben zu Beginn der Therapie nach ctDNA gesucht und diese auf Mutationen untersucht, darunter PI3K und Östrogenrezeptor-1 (ESR1). Bei 494 von 668 Patientinnen gelang der Nachweis von ctDNA, wobei nur bei 427 Patientinnen (64%) das Material für DNA-Untersuchungen ausreichte. Mutationen betrafen die Gene PI3KCA (33%), TP53 (12%), ZNF03/FGFR1 (5%) und ESR1 (4%) sowie Gene, welche in den Rezeptortyrosinkinase(RTK)-Signaltransduktionsweg involviert sind. Wie von Turner in der PALOMA-3-Studie [26] schon für Palbociclib am Beispiel der ESR1-Mutation nachgewiesen werden konnte, besteht die Wirksamkeit für den CDK4/6-Inhibitor unabhängig von den derzeit untersuchten Mutationen in ctDNA.
Fazit
- Für diese effektive Substanzgruppe gibt es derzeit keine geeigneten Biomarker, die eine Gruppe von Patientinnen identifizieren, die (nicht) von einer CDK4/6-Therapie profitiert.
„Auch wenn in dieser Studie keine geeigneten prädiktiven Marker für CDK4/6-Inhibitoren identifiziert werden konnten, wird die Liquid Biopsy zukünftig in der Identifizierung therapeutischer Ziele und geeigneter Patientinnen sowie beim Monitoring einer zielgerichteten Therapie eine immer größere Rolle spielen.“ Prof. Dr. med. Michael Braun
IMpassion031-Studie: Atezolizumab
Atezolizumab ist ein humanisierter monoklonaler PD-L1-Antikörper, der die Bindung von programmed cell death 1 ligand 1 (PD-L1) an seinen Rezeptor PD1 und B7.1 unterdrückt und so eine tumorspezifische T-Zell-Antwort ermöglicht. Da nab-Paclitaxel ohne die antiallergische Cortisontherapie verabreicht werden kann, kann so theoretisch eine potenzielle Immunsuppression vermieden werden. Dies macht das Medikament zu einem idealen Kombinationspartner für eine Tumorimmuntherapie. In der IMpassion-031-Studie (Phase III) wird
- neoadjuvant Atezolizumab (840 mg i.v. alle zwei Wochen für zwölf Wochen) mit nab-Paclitaxel (125 mg/m2 i.v. wöchentlich) oder ein Placebo mit nab-Paclitaxel, gefolgt von
- Doxorubicin (60 mg/m2 i.v. alle zwei Wochen) und Cyclophosphamid (600 mg/m2 i.v. alle zwei Wochen), jeweils kombiniert mit Atezolizumab oder einem Placebo verabreicht [27].
Nach erfolgter Operation erhalten die Patientinnen im experimentellen Arm Atezolizumab für weitere elf Dosen (1.200 mg i.v. alle drei Wochen). Die Therapie wird unabhängig von einer PD-L1-Expression appliziert.
Diese Studie ist der logische Schritt hin zur Überprüfung einer weiteren potenziellen Verbesserung der Therapie des tripelnegativen Mammakarzinoms.
Vermeidung von Haarverlust
Die Vermeidung der chemotherapiebedingten Alopezie ist seit vielen Jahren Gegenstand unterschiedlicher Therapieansätze, in deren Rahmen Kühlkappen eingesetzt werden. Aufgrund der aufwändigen Handhabung und der von den Patientinnen oft als unkomfortabel empfundenen Methode sowie aufgrund des mäßigen Erfolgs bei der Vermeidung von Haarverlust konnten sich die Geräte zunächst in der Praxis nicht durchsetzen. Durch die erfolgreiche Weiterentwicklung der Gerätetechnik machen nun insbesondere zwei Anbieter auf sich aufmerksam. Bereits 2016 stellten Nangia et al. die Ergebnisse einer prospektiv randomisierten Studie mit dem Orbis Paxman Hair Loss Prevention System (OPHLPS) vor [28]. Während in einer Zwischenanalyse über 50% der Patientinnen mit dem Kühlkappensystem einen Haarverlust vermeiden konnten, verloren alle Patientinnen in der Kontrollgruppe ihre Haare, sodass die Studie abgebrochen wurde. Insbesondere Patientinnen mit alleiniger Taxantherapie profitierten von dem System, während die Haarverlustrate in dieser Untersuchung bei Anwendung von Anthrazyklinen trotz Scalp Cooling bei schlechten 80% lag.
Eine Studie zur Anwendung des Scalp-Cooling-Systems Dignicap® wurde jetzt von Marc Thill aus Frankfurt vorgestellt [29]. Die Interimsanalyse von insgesamt 48 Patientinnen zeigte eine komplette Vermeidung von Haarverlust bei 8,0% der Patientinnen. Einen moderaten Haarverlust (<20%) wiesen 60,0% der Patientinnen auf. Ein kompletter Haarverlust trat bei nur 27,1% der Patientinnen auf. Dies ist insofern beachtlich, als dass 60,4% der Studienteilnehmerinnen eine anthrazyklinhaltige Chemotherapie erhielten (viermal EC alle drei Wochen, gefolgt von zwölfmal Paclitaxel wöchentlich). Zu den unerwünschten Nebenwirkungen gehörten neben einem unangenehmen Kältegefühl auch Kopfschmerzen (12,5%).
Fazit
- Aufgrund der sich verdichtenden guten Datenlage zum Einsatz von Kühlkappensystemen werden diese zunehmend von Patientinnen nachgefragt.
- Insbesondere beim Einsatz von anthrazyklinfreien taxanhaltigen Chemotherapien (Paclitaxel+Cyclophosphamid, Paclitaxel+Trastuzumab, Docetaxel+Trastuzumab+Pertuzumab etc.) kann in mehr als 80% der Anwendungen ein Haarverlust vermieden werden.
- Eine Herausforderung für die tägliche Praxis sind bisher die Integration der Systeme in den logistischen Ablauf der Tageskliniken und die ungeklärte Kostenerstattung.
Onkoimmunologie
Die prädiktive und prognostische Bedeutung von tumorinfiltrierenden Lymphozyten (TIL) als Ausdruck einer onkoimmunologischen Antwort wurde unter anderem in einer großen Metaanalyse aus Deutschland mit über 3.700 Patientinnen mit frühem Mammakarzinom bestätigt [30]. Als immunologische Marker könnten auch Lymphozyten im peripheren Blut dienen. Eine kombinierte Analyse zweier prospektiver Studien, die durch eine japanische Arbeitsgruppe durchgeführt worden war, beschäftigte sich mit dieser Hypothese. Die Ergebnisse wurden von Kazuhiro Araki präsentiert [31]. In diesen einarmigen Open-Label-Phase-II-Studien mit insgesamt 51 Patientinnen mit einem HER2-positiven fortgeschrittenen Mammakarzinom wurden zusätzlich zu der Kombination Trastuzumab und Pertuzumab (TP) Eribulin (n=30) oder nab-Paclitaxel (n=21) eingesetzt.
Eine hohe prätherapeutische absolute Lymphozytenzahl (ALC) >1.500 Zellen/µl korrelierte im Vergleich zu <1.000 Zellen/µl mit einem signifikant verbesserten PFS unter TP unabhängig vom Kombinationspartner.
Die ALC könnte somit nach Meinung der Autoren möglicherweise als prädiktiver Blutmarker ein Therapieansprechen bei vortherapierten Patientinnen mit HER2-positivem metastasiertem Mammakarzinom voraussagen. Wenngleich der klinische Nutzen dieser Information eingeschränkt ist, erscheint diese Beobachtung aus tumorimmunologischer Sicht interessant und sollte in weiteren Studien begleitend untersucht werden.
Quellen
- Gray R et al. Increasing the dose density of adjuvant chemotherapy by shortening intervals between courses or by sequential drug administration significantly reduces both disease recurrence and breast cancer mortality: An EBCTCG meta-analysis of 21,000 women in 16 randomised trials. Presented at San Antonio Breast Cancer Symposium 2017, abstract GS1-01.
- Citron ML et al. Randomized trial of dose-dense versus conventionally scheduled and sequential versus concurrent combination chemotherapy as postoperative adjuvant treatment of node-positive primary breast cancer: first report of Intergroup Trial C9741/Cancer and Leukemia Group B Trial 9741. J Clin Oncol 2003; 21: 1431-1439.
- Romond EH et al. Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer. N Engl J Med 2005; 353: 1673-1684.
- Fehrenbacher L et al. NSABP B-47 (NRG oncology): Phase III randomized trial comparing adjuvant chemotherapy with adriamycin (A) and cyclophosphamide (C) → weekly paclitaxel (WP), or docetaxel (T) and C with or without a year of trastuzumab (H) in women with node-positive or high-risk node-negative invasive breast cancer (IBC) expressing HER2 staining intensity of IHC 1+ or 2+ with negative FISH (HER2-Low IBC). San Antonio Breast Cancer Symposium 2017, abstract GS1-02.
- Dhesy-Thind S et al. Use of Adjuvant Bisphosphonates and Other Bone-Modifying Agents in Breast Cancer: A Cancer Care Ontario and American Society of Clinical Oncology Clinical Practice Guideline. J Clin Oncol 2017; 35: 2062-2081.
- Janni W et al. Extended adjuvant bisphosphonate treatment over five years in early breast cancer does not improve disease-free and overall survival compared to two years of treatment: Phase III data from the SUCCESS A study. San Antonio Breast Cancer Symposium 2017, abstract GS1-06.
- Untch M et al. A randomized phase III trial comparing neoadjuvant chemotherapy with weekly nanoparticle-based paclitaxel with solvent-based paclitaxel followed by anthracyline/cyclophosphamide for patients with early breast cancer (GeparSepto); GBG 69. San Antonio Breast Cancer Symposium 2014, abstract PD2-6.
- Schneeweiss A et al. Survival analysis of the prospectively randomized phase III GeparSepto trial comparing neoadjuvant chemotherapy with weekly nab-paclitaxel with solvent-based paclitaxel followed by anthracycline/cyclophosphamide for patients with early breast cancer – GBG69. San Antonio Breast Cancer Symposium 2017, abstract GS3-05.
- Untch M et al. Nab-paclitaxel versus solvent-based paclitaxel in neoadjuvant chemotherapy for early breast cancer (GeparSepto-GBG 69): a randomised, phase 3 trial. Lancet Oncol 2016; 17: 345-356.
- Rugo H et al. Long-term follow-up of CALGB 40502/NCCTG N063H (Alliance): A randomized phase III trial of weekly paclitaxel (P) compared to weekly nanoparticle albumin bound nab-Paclitaxel (NP) or ixabepilone (Ix) +/- bevacizumab as first-line therapy for locally recurrent or metastatic breast cancer (MBC). San Antonio Breast Cancer Symposium 2017, abstract GS3-06.
- Rugo HS et al. Randomized Phase III Trial of Paclitaxel Once Per Week Compared With Nanoparticle Albumin-Bound Nab-Paclitaxel Once Per Week or Ixabepilone With Bevacizumab As First-Line Chemotherapy for Locally Recurrent or Metastatic Breast Cancer: CALGB 40502/NCCTG N063H (Alliance). J Clin Oncol 2015; 33: 2361-2369.
- Tjan-Heijnen V et al. First results from the multicenter phase III DATA study comparing 3 versus 6 years of anastrozole after 2-3 years of tamoxifen in postmenopausal women with hormone receptor-positive early breast cancer. San Antonio Breast Cancer Symposium 2016, abstract S1-03.
- Blok E et al. Optimal duration of extended letrozole treatment after 5 years of adjuvant endocrine therapy; results of the randomized phase III IDEAL trial (BOOG 2006-05). San Antonio Breast Cancer Symposium 2016, abstract S1-04.
- Goss PE et al. A randomized trial (MA.17R) of extending adjuvant letrozole for 5 years after completing an initial 5 years of aromatase inhibitor therapy alone or preceded by tamoxifen in postmenopausal women with early-stage breast cancer. J Clin Oncol 34, 2016 (suppl; abstr LBA1).
- Gnant M et al. A prospective randomized multi-center phase-III trial of additional 2 versus additional 5 years of anastrozole after initial 5 years of adjuvant endocrine therapy – results from 3,484 postmenopausal women in the ABCSG-16 trial. Presented at San Antonio Breast Cancer Symposium 2017, abstract GS3-01.
- Lambertini M et al. Pooled analysis of five randomized trials investigating temporary ovarian suppression with gonadotropin-releasing hormone analogs during chemotherapy as a strategy to preserve ovarian function and fertility in premenopausal early breast cancer patients. San Antonio Breast Cancer Symposium 2017, abstract GS4-01.
- Pagani O et al. Randomized comparison of adjuvant aromatase inhibitor exemestane (E) plus ovarian function suppression (OFS) vs tamoxifen (T) plus OFS in premenopausal women with hormone receptor positive (HR+) early breast cancer (BC): Update of the combined TEXT and SOFT trials. San Antonio Breast Cancer Symposium 2017, abstract GS4-02.
- Fleming G et al. Randomized comparison of adjuvant tamoxifen (T) plus ovarian function suppression (OFS) versus tamoxifen in premenopausal women with hormone receptor-positive (HR+) early breast cancer (BC): Update of the SOFT trial. San Antonio Breast Cancer Symposium 2017, abstract GS4-03.
- Tripathy D et al. First-line ribociclib vs placebo with goserelin and tamoxifen or a non-steroidal aromatase inhibitor in premenopausal women with hormone receptor-positive, HER2-negative advanced breast cancer: Results from the randomized phase III MONALEESA-7 trial. San Antonio Breast Cancer Symposium 2017, abstract GS2-05.
- Goetz M et al. The benefit of abemaciclib in prognostic subgroups: An exploratory analysis of combined data from the MONARCH 2 and 3 studies. San Antonio Breast Cancer Symposium 2017, abstract GS6-02.
- Litton J et al. EMBRACA: A phase 3 trial comparing talazoparib, an oral PARP inhibitor, to physician's choice of therapy in patients with advanced breast cancer and a germline BRCA mutation. San Antonio Breast Cancer Symposium 2017, abstract GS6-07.
- Bardia A et al. Sacituzumab govitecan (IMMU-132), an anti-Trop-2-SN-38 antibody-drug conjugate, as ≥3rd-line therapeutic option for patients with relapsed/refractory metastatic triple-negative breast cancer (mTNBC): efficacy results. Presented at San Antonio Breast Cancer Symposium 2017, abstract GS1-07.
- Baselga J et al. PIK3CA status in circulating tumor DNA (ctDNA) predicts efficacy of buparlisib (BUP) plus fulvestrant (FULV) in postmenopausal women with endocrine-resistant HR+/HER2– advanced breast cancer (BC): First results from the randomized, phase III BELLE-2 trial. San Antonio Breast Cancer Symposium 2015, abstract S6-01.
- Hortobagyi GN et al. Ribociclib as First-Line Therapy for HR-Positive, Advanced Breast Cancer. N Engl J Med 2016; 375: 1738-1748.
- Hortobagyi G et al. First-line ribociclib + letrozole in hormone receptor-positive, HER2-negative advanced breast cancer: Efficacy by baseline circulating tumor DNA alterations in MONALEESA-2. San Antonio Breast Cancer Symposium 2017, abstract PD4-06.
- Turner NC et al. Efficacy of palbociclib plus fulvestrant (P+F) in patients (pts) with metastatic breast cancer (MBC) and ESR1 mutations (mus) in circulating tumor DNA (ctDNA). J Clin Oncol 34, 2016 (suppl; abstr 512).
- Mittendorf E et al. IMpassion031: A phase III study comparing neoadjuvant atezolizumab vs placebo in combination with nab-paclitaxel–based chemotherapy in early triple-negative breast cancer (TNBC). San Antonio Breast Cancer Symposium 2017, abstract OT2-07-03.
- Nangia J et al. Scalp cooling alopecia prevention trial (SCALP) for patients with early stage breast cancer. San Antonio Breast Cancer Symposium 2016, abstract S5-02.
- Traub L et al. Effectiveness and adverse events of DigniCap® scalp cooling system. San Antonio Breast Cancer Symposium 2017, abstract P6-11-07.
- Denkert C et al. Evaluation of tumor-infiltrating lymphocytes (TILs) as predictive and prognostic biomarker in different subtypes of breast cancer treated with neoadjuvant therapy - A metaanalysis of 3771 patients. San Antonio Breast Cancer Symposium 2016, abstract S1-09.
- Araki K et al. Predictive impact of absolute lymphocyte counts for progression-free survival in HER2-positive advanced breast cancer treated with pertuzumab and trastuzumab plus eribulin or nab-paclitaxel. San Antonio Breast Cancer Symposium 2017, abstract P2-09-31.
- Bildnachweis: „Turm von Amerika Texas San Antonio”: pixabay; "San Antonio": © Aaron/Fotolia