ESMO 2019
27. September bis 01. Oktober, Barcelona
- Pankreaskarzinom – neoadjuvante Therapieansätze festigen ihren Stellenwert
- Die Immuntherapie beim frühen Mammakarzinom ist auf dem Vormarsch
- ESMO-Kongress 2019: Update zur Thoraxonkologie
 Vom 27. September bis zum 1. Oktober trafen sich die weltweit renommiertesten Onkologie-Experten auf dem Kongress der European Society for Medical Oncology (ESMO) in Barcelona. Hier erhalten Sie kompakte Informationen vom ESMO-Kongress zu den aktuellsten wissenschaftlichen Erkenntnissen aus den Themengebieten Pankreaskarzinom, Mammakarzinom und nichtkleinzelliges Lungenkarzinom (NSCLC).
Vom 27. September bis zum 1. Oktober trafen sich die weltweit renommiertesten Onkologie-Experten auf dem Kongress der European Society for Medical Oncology (ESMO) in Barcelona. Hier erhalten Sie kompakte Informationen vom ESMO-Kongress zu den aktuellsten wissenschaftlichen Erkenntnissen aus den Themengebieten Pankreaskarzinom, Mammakarzinom und nichtkleinzelliges Lungenkarzinom (NSCLC).
Liebe Kolleginnen und Kollegen,
in diesem Jahr fanden über 28.000 Experten den Weg nach Barcelona, um an der Jahrestagung der European Society for Medical Oncology (ESMO) teilzunehmen. Vom 27. September bis zum 1. Oktober fand hier ein reger Erfahrungs- und Wissensaustausch statt. Das zentrale Thema in diesem Jahr war die Verbesserung der Versorgung von Krebspatienten.
In unseren Berichten vom ESMO-Kongress können Sie sich über die neuesten Entwicklungen und Empfehlungen zu den Themen Pankreaskarzinom, Mammakarzinom und nichtkleinzelliges Lungenkarzinom informieren. Die Forscher beschäftigten sich dabei vor allem mit der Frage, wie die verschiedenen Therapieansätze weiterentwickelt und schließlich im klinischen Alltag umgesetzt werden können. Auch zielgerichtete Therapien mit monoklonalen Antikörpern oder immunologische Ansätze mit Checkpointinhibitoren beschäftigen die Experten weit über die Indikationsgrenzen hinweg.
Seien Sie gespannt, was es Neues gibt. Wir wünschen Ihnen eine abwechslungsreiche Lektüre.
Mit kollegialen Grüßen
 Dr. med. Gabriele Siegler, Klinik für Innere Medizin 5 mit Schwerpunkt Onkologie und Hämatologie, Klinikum Nürnberg/Paracelsus Medizinische Privatuniversität, Nürnberg
Dr. med. Gabriele Siegler, Klinik für Innere Medizin 5 mit Schwerpunkt Onkologie und Hämatologie, Klinikum Nürnberg/Paracelsus Medizinische Privatuniversität, Nürnberg Prof. Dr. med. Diana Lüftner, Medizinische Klinik und Poliklinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie, Charité Campus Benjamin Franklin, Humboldt-Universität zu Berlin
Prof. Dr. med. Diana Lüftner, Medizinische Klinik und Poliklinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie, Charité Campus Benjamin Franklin, Humboldt-Universität zu Berlin
Dr. med. Nikolaj Frost, Med. Klinik m. S. Infektiologie/ Pneumologie, Charité
Universitätsmedizin Berlin
Pankreaskarzinom – neoadjuvante Therapieansätze festigen ihren Stellenwert
Dr. med. Gabriele Siegler, Klinik für Innere Medizin 5 mit Schwerpunkt Onkologie und Hämatologie, Klinikum Nürnberg/Paracelsus Medizinische Privatuniversität, Nürnberg
 Das Pankreaskarzinom gehört zu den Krebserkrankungen mit einer der höchsten tumorspezifischen Mortalitäten. Eine Heilung ist nur durch Resektion erreichbar. Ein multimodaler, interdisziplinärer Ansatz mittels neoadjuvanter Chemotherapien und Implementation einer explorativen Laparotomie bei zumindest stabiler Krankheitssituation kann die Resektionsrate und das Überleben signifikant steigern.
Das Pankreaskarzinom gehört zu den Krebserkrankungen mit einer der höchsten tumorspezifischen Mortalitäten. Eine Heilung ist nur durch Resektion erreichbar. Ein multimodaler, interdisziplinärer Ansatz mittels neoadjuvanter Chemotherapien und Implementation einer explorativen Laparotomie bei zumindest stabiler Krankheitssituation kann die Resektionsrate und das Überleben signifikant steigern.
Therapie des lokal fortgeschrittenen Pankreaskarzinoms
Circa 30% der Pankreaskarzinome werden bei der Erstdiagnose schon zu den lokal fortgeschrittenen Tumoren gerechnet. Eingeschlossen sind hier sowohl die primär irresektablen als auch die grenzwertig resektablen Tumoren. Die Festlegung von Resektabilitätskriterien anhand der Bildgebung wird jedoch von den verschiedenen onkologischen Gesellschaften, wie zum Beispiel von dem National Comprehensive Cancer Network (NCCN) oder dem MD Anderson Cancer Center in Houston, Texas, und insbesondere auch von den Tumorchirurgen kontrovers diskutiert.
Mehrere nicht randomisierte Multizentrumsstudien zeigten in den letzten Jahren durch intensivierte Therapieprotokolle wie FOLFIRINOX (Folinsäure+5-Fluorouracil+Irinotecan+Oxaliplatin) Resektionsraten von bis zu 15% bei lokal fortgeschrittenen Tumoren (LAPCs) [1,2,3].
Beim ESMO-Kongress 2019 präsentierte nun die Studiengruppe um Volker Kunzmann aus Würzburg Ergebnisse aus der ersten prospektiven randomisierten Studie (NEOLAP-Studie, NCT02125136) zur neoadjuvanten Therapie bei grenzwertig resektablen und primär irresektablen duktalen Adenokarzinomen [4]. Als primärer Endpunkt wurde die Konversionsrate von Irresektabilität zu Resektabilität nach einer neoadjuvanten Chemotherapie gewählt. Nach der Biopsie erfolgten zunächst 2 Zyklen Induktionschemotherapie mit nab-Paclitaxel+Gemcitabin (nab-P+Gem) für alle Patienten. Nach 8 Wochen wurde in die beiden sich anschließenden Therapiearme randomisiert: entweder in Arm A mit 2 weiteren Zyklen nab-P+Gem oder in Arm B mit einem Switch des neoadjuvanten Chemotherapieprotokolls in nachfolgend 4 Zyklen eines sequentiellen, nicht modifizierten FOLFIRINOX-Schemas (= sqFOLFIRINOX mit Oxaliplatin, Irinotecan, Leucovorin, 5-Fluorouracil [5-FU]). Der Hintergrund für dieses Vorgehen sind Daten, die zeigen, dass durch die vorgeschaltete Chemotherapie mit einer nab-Paclitaxel-Kombination das tumorumgebende Stroma durchlässiger für andere Zytostatika wird. Dadurch können die intratumoralen Zytostatikakonzentrationen gesteigert werden [5]. Nach der Applikation der Neoadjuvanz war eine explorative Laparotomie bei zumindest stabiler Krankheitssituation in der Bildgebung protokollgemäß vorgeschrieben. Wurde eine R0- oder R1-Resektion erreicht, erfolgte eine adjuvante Therapie mit 3 weiteren Zyklen nab-P+Gem (Abb. 1).
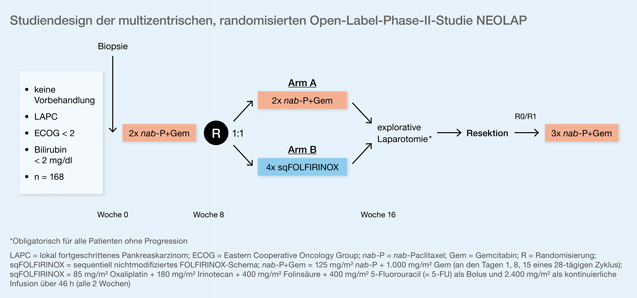
Abb. 1: NEOLAP-Studie: neoadjuvante Therapie mit nab-P+Gem versus sqFOLFIRINOX nach Induktion mit nab-P+Gem bei nicht resektablem LPAC (modifiziert nach [4])
Von 168 eingeschlossenen Patienten aus 33 deutschen Zentren erhielten 60 mit nab-P+Gem beziehungsweise 52 Patienten mit sqFOLFIRINOX die protokollgerechte Neoadjuvanz. 40 Patienten aus dem nab-P+Gem-Arm beziehungsweise 42 Patienten aus dem sqFOLFIRINOX-Arm wurden im Verlauf explorativ laparotomiert. Insgesamt 33 Patienten waren während der Neoadjuvanz progredient (20%). Diese Gruppe scheint somit zu einer Population mit prognostisch ungünstigem Verlauf und aggressivem Tumorwachstum zu gehören. Diese Patienten hätten auch bei Vorliegen primärer Resektabilitätskriterien wohl kaum von einer Primariusresektion profitiert, da man schon prätherapeutisch von einer Therapierefraktärität der bereits initial vorliegenden Systemerkrankung hätte ausgehen können.
Bei 45,0% der Patienten im sqFOLFIRINOX-Arm und bei 30,6% der Patienten im nab-P+Gem-Arm konnte eine R0/R1-Resektion erreicht werden (Odds Ratio [OR]: 0,54; 95-%-Konfidenzintervall [95-%-KI]: 0,26─1,13; p = 0,135). Von der gesamten Intention-to-treat(ITT)-Population konnten 27,9% der Patienten letztendlich reseziert werden (Abb. 2).
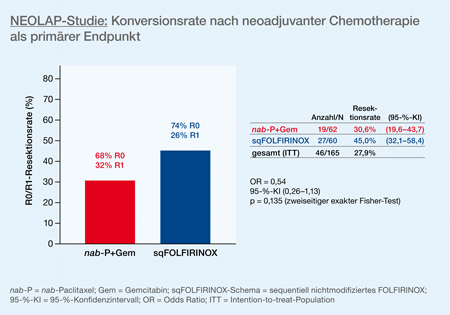 Abb. 2: NEOLAP-Studie: unter Therapie mit sqFOLFIRINOX nach Induktion mit nab-P+Gem konnte eine verbesserte Konversionsrate von Irresektabilität zu Resektabilität erreicht werden (modifiziert mach [4])
Abb. 2: NEOLAP-Studie: unter Therapie mit sqFOLFIRINOX nach Induktion mit nab-P+Gem konnte eine verbesserte Konversionsrate von Irresektabilität zu Resektabilität erreicht werden (modifiziert mach [4])Die Toxizität war gut tolerabel und warf keine neuen Sicherheitsbedenken auf. Das mediane progressionsfreie Überleben (PFS) betrug 7,9 Monate im nab-P+Gem-Arm versus 9,7 Monate im sqFOLFIRINOX-Arm mit einer Krankheitskontrollrate von 75,0% im sqFOLFIRINOX-Arm beziehungsweise 82,3% im nab-P+Gem-Arm. Das mediane Gesamtüberleben (mOS) betrug 22,5 Monate im sqFOLFIRINOX-Arm versus 17,2 Monate im nab-P+Gem-Arm (adjustierte Hazard Ratio [HR]: 0,73; 95-%-KI: 0,42─1,28; p = 0,268). Es zeigt sich also ein Trend für eine höhere Konversionsrate und für ein besseres Gesamtüberleben mit sqFOLFIRINOX. Dieser Trend war aber nicht signifikant – eventuell auch aufgrund der kleinen Fallzahl.
Ein signifikanter Überlebensvorteil zeigte sich jedoch in der resezierten Gruppe mit einem mOS von 27,4 Monaten im Vergleich zu den nicht resezierten Patienten mit nur 14,2 Monaten (HR: 0,45; 95-%-KI: 0,26─0,78; p = 0,0035) (Abb. 3).
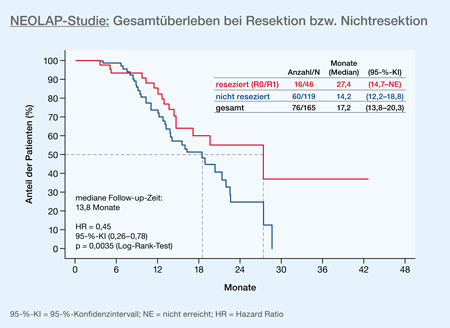 Abb. 3: NEOLAP-Studie: Patienten, die reseziert wurden, hatten ein signifikant verbessertes medianes Gesamtüberleben (modifiziert nach [4])
Abb. 3: NEOLAP-Studie: Patienten, die reseziert wurden, hatten ein signifikant verbessertes medianes Gesamtüberleben (modifiziert nach [4])Erwähnenswert sind auch die im Rahmen einer Posterdiskussion vorgestellten Ergebnisse der multizentrischen randomisierten Phase-II-GAP-Studie (NCT02043730) der italienischen Studiengruppe GISCAD [6]. Hierbei wurde erstmals die bereits in vielen Ländern in der palliativen Situation etablierte Chemotherapie mit nab-P+Gem in der nicht metastasierten Situation bei lokal fortgeschrittenem und irresektablem Tumor direkt mit einer Gem-Monotherapie verglichen. Bei Vorliegen einer zumindest stabilen Krankheitssituation nach 3 Zyklen erfolgte eine konsolidierende Radiochemotherapie mit Capecitabin über 5 Wochen. 124 Patienten konnten in die Studie eingeschlossen und in die beiden Therapiearme randomisiert werden. Der primäre Endpunkt, die Progressionsrate (disease progression rate, DPR) nach 3 Zyklen Chemotherapie, zeigte eine deutliche Überlegenheit des Kombinationsarms (25,4% im nab-P+Gem-Arm versus 45,6% im Gem-Arm; p = 0,01). Das mediane PFS (7,6 Monate versus 5,1 Monate; HR: 0,71; 95-%-KI: 0,51─0,99) und das mediane OS (13,1 Monate versus 10,7 Monate; HR: 0,65; 95-%-KI: 0,44─0,94; p = 0,03) spiegelten den Vorteil der Kombinationstherapie nab-P+Gem wider. Interessant ist hierbei auch, dass insbesondere die Fernmetastasierungsrate deutlich von 31,6% im Gem-Arm auf 9,5% im nab-P+Gem-Arm gesenkt werden konnte.
Fazit
- Die Daten der NEOLAP- und GAP-Studien wurden auf dem ESMO-Kongress 2019 als die beiden Highlights zur Thematik des Pankreaskarzinoms vorgestellt.
- Ein neoadjuvantes Vorgehen mittels intensivierter Chemotherapie mit nab-Paclitaxel+Gemcitabin beziehungsweise mit einem nicht modifizierten FOLFIRINOX-Schema nach Induktion mit nab-P+Gem führt bei lokal fortgeschrittenen Pankreaskarzinomen bei etwa einem Drittel der Patienten zu einer R0/R1-Resesktion.
- Eine Aussage darüber, ob die Therapie mit dem sqFOLFIRINOX-Schema effektiver ist als mit der Kombination von nab-Paclitaxel+Gemcitabin, kann anhand der NEOLAP-Studie nicht getroffen werden.
- Die explorative Laparotomie zeigte, dass die alleinige Bildgebung zur Wertung eines Therapieansprechens nach einer intensivierten Chemotherapie oftmals unzureichend ist.
- Die bereits beim metastasierten Pankreaskarzinom zugelassene Kombination von nab-Paclitaxel+Gemcitabin ist in der irresektablen, aber metastasenfreien Situation einer Gemcitabin-Monotherapie überlegen und senkt insbesondere das Metastasierungsrisiko. Welchen Stellenwert die konsolidierende Radiochemotherapie dabei einnimmt, bleibt noch unklar. Sie kann aber basierend auf den Daten der Phase-II-GAP-Studie nach 3 Zyklen Chemotherapie angeboten werden.
“Die Diskussion neoadjuvant intendierter Therapieansätze beim lokal fortgeschrittenen Pankreaskarzinom muss als Standard in den interdisziplinären Tumorkonferenzen etabliert werden. Eine explorative Laparotomie sollte bei fehlenden eindeutigen Progresszeichen in der Bildgebung angestrebt werden.“ Dr. med. Gabriele Siegler
Therapie des metastasierten Pankreaskarzinoms
Auch beim Pankreaskarzinom werden intensiv zielgerichtete Therapieansätze untersucht. Monotherapien mit Tyrosinkinaseinhibitoren (TKIs), mit Immuncheckpointinhibitoren oder mit EGFR/VEGFR-Antikörpern (EGFR = epidermaler Wachstumsfaktorrezeptor; VEGFR = vaskulärer endothelialer Wachstumsfaktorrezeptor) erbrachten bisher keinen signifikanten Nutzen. Umso erwähnenswerter ist die Tatsache, dass Patienten mit einer Keimbahnmutation im BRCA1/2-Gen von einer Erhaltungstherapie mit einem PARP-Inhibitor (PARP = Poly-ADP-Ribose-Polymerase) wie Olaparib profitieren. Aufgrund der bereits beim diesjährigen ASCO-Kongress (siehe auch den Pankreaskarzinom-Bericht vom ASCO-Kongress 2019 auf hematooncology.com) vorgestellten Ergebnisse der randomisierten, doppelt verblindeten, placebokontrollierten Phase-III-POLO-Studie (NCT02184195) [7] empfiehlt das NCCN die Testung aller Pankreaskarzinompatienten auf eine BRCA-Keimbahnmutation in seinen Leitlinien. Der primäre Endpunkt war das PFS. Olaparib führte nach einer platinhaltigen Chemotherapie in der Erstlinie zu einer signifikanten Verlängerung des medianen PFS (von 3,8 auf 7,4 Monate; HR für Progression oder Tod: 0,53; 95-%-KI: 0,35─0,82; p = 0,004), was sich allerdings bis jetzt nicht auf eine signifikante Verlängerung des medianen OS überträgt (18,1 Monate in der Placebogruppe versus 18,9 Monate in der Olaparib-Gruppe; HR für Tod: 0,91; 95-%-KI: 0,56─1,46; p = 0,68). Ein möglicher Grund hierfür könnte die Einnahme von PARP-Inhibitoren in den Folgetherapien nach einer Progression sein. Dies betraf einen kleinen Anteil (9%) der 53 Patienten des initialen Kontrollarms. Nicht unterschätzt werden sollte zudem der Nutzen einer platinhaltigen Erstlinientherapie bei BRCA-positiven Patienten. Auch hier wurden inzwischen die NCCN-Leitlinien angepasst.
Pascal Hammel stellte auf dem diesjährigen ESMO-Kongress nun Daten zur gesundheitsbezogenen Lebensqualität (HRQoL) der POLO-Studie vor [8]. Die Lebensqualitätsscores waren unter der Olaparib-Erhaltungstherapie nicht signifikant unterschiedlich im Vergleich zum Placeboarm. Allerdings litten die Patienten unter Olaparib vermehrt unter Inappetenz (p = 0,003) und Fatigue (p = 0,001). Die Auswertung weiterer sekundärer Endpunkte zeigte eine deutliche Verlängerung der Dauer der Erstlinientherapie (TTD = time-to-treatment discontinuation) von 3,8 Monaten im Placeboarm auf 7,2 Monate im Olaparib-Arm (HR: 0,45; 95-%-KI: 0,30─0,67; p = 0,0001) und der Zeit bis zur ersten Folgetherapie (TFST = time to first subsequent therapy) von 5,7 Monaten auf 8,6 Monate (HR: 0,50; 95-%-KI: 0,32─0,76; p = 0,0013) sowie der Zeitdauer bis zur 2. Folgetherapie oder Tod (TSST = time to second subsequent therapy) von 9,2 Monaten auf 13,2 Monate (HR: 0,68; 95-%-KI: 0,44─1,05; p = 0,083).
Zusammenfassend lässt sich festhalten, dass diese in Europa noch nicht zugelassene Therapieoption nur für etwa 5% aller Pankreaskarzinompatienten nutzbringend sein könnte. Des Weiteren liegt in Deutschland die Standardtestung auf Keimbahnmutationen in den BRCA-Genen bei Pankreaskarzinomen aufgrund der fehlenden Abrechnungsmöglichkeit leider noch in weiter Ferne. Allerdings darf den Patienten auch bei einer Genehmigung eines individuellen Heilversuchs mit Olaparib nicht die Information vorenthalten werden, dass zwar mit einem längeren progressions- und chemotherapiefreien Intervall gerechnet werden kann, dies sich aber bis dato nicht in einem Überlebensvorteil widerspiegelt und möglicherweise mit einer Einschränkung der Lebensqualität durch mehr Inappetenz und Fatigue erkauft wird.
In der metastasierten Situation fehlen noch immer weitere innovative, wirklich Erfolg versprechende Therapiemöglichkeiten. Phase-I-Studien mit onkolytischen Viren wie VCN-01 oder Studien mit immunmodulatorischen, in die Epigenetik eingreifenden Strategien (z. B. die geplante multizentrische Phase-I/II-SEPION-Studie [AIO-PAK-0118]) können Hinweise auf eine mögliche Wirksamkeit geben. Ob diese Ansätze weiterverfolgt werden sollten, bleibt abzuwarten.
Daten der „First-in-Human“-Phase-I-Studie zur Therapie mit VCN-01 (NCT02045602) stellte Rocio Garcia-Carbonero nun auf dem ESMO-Kongress vor [9]. VCN-01 zeigt bei systemischer Applikation ein gutes Sicherheitsprofil in Kombination mit Standard-of-Care(SoC)-Regimen beim Pankreaskarzinom. Aufgrund der Tatsache, dass VCN-01 die Tumoren systemisch erreicht, kann die Tumormatrix so verändert werden, dass eine Infiltration mit Immunzellen möglich wird.
Pankreaskarzinome mit einer hohen Expression von Hyaluronsäure im desmoplastischen Stroma könnten von einer spezifischen Therapie mit Hyaluronidasederivaten profitieren (Phase-III-HALO-109-301-Studie, NCT02715804).
Fazit:
- Patienten mit einer BRCA-Keimbahnmutation können durch eine zielgerichtete Therapie mit Olaparib nach einer platinhaltigen Chemotherapie mit einem längeren chemotherapiefreien Intervall und einem verlängerten progressionsfreien Überleben rechnen. Durch die alleinige Therapie mit Olaparib ist keine signifikante Einschränkung der Lebensqualität zu befürchten. Fatigue und Inappetenz können jedoch vermehrt auftreten.
- Therapieansätze mit Hyaluronidasederivaten oder die epigenetische Modulation in Kombination mit Chemotherapien sind derzeit eine der wenigen möglicherweise Erfolg versprechenden Innovationen beim Pankreaskarzinom.
“Eine breite molekulare Testung auf BRCA-Keimbahnmutationen, welche sich auch im einheitlichen Bewertungsmaßstab (EBM) abbilden würde, wäre wünschenswert. So könnten Therapieansätze mit platinhaltigen Kombinationen oder gegebenenfalls mit Olaparib schneller gezielt für geeignete Patientensubgruppen angeboten werden. Gerade für dieses Patientenkollektiv mit einer der höchsten tumorspezifischen Mortalitätsraten wäre es enorm wichtig, zeitnah entsprechende Real-World-Daten zu generieren, um den Therapiefortschritt voranzutreiben.” Dr. med. Gabriele Siegler
Adjuvante Therapie
Bereits beim diesjährigen ASCO-Kongress wurden die Ergebnisse der multizentrischen, randomisierten Open-Label-Phase-III-Studie APACT (NCT01964430) vorgestellt [10]. Wider Erwarten zeigte sich nach einer chirurgischen Tumorresektion beim rezidivfreien Überleben (RFS = relapse-free survival) kein signifikanter Vorteil für die Kombination von nab-P+Gem gegenüber der Gem-Monotherapie. Dies mag zunächst erstaunen, da die Kombination aus nab-P+Gem im Vergleich zu einer Monotherapie mit Gem in der metastasierten Situation einen deutlichen Vorteil sowohl im PFS als auch im OS zeigen konnte [11] und weltweit neben dem modifizierten FOLFIRINOX-Regime als effektiver Goldstandard gilt. Beim genaueren Hinsehen darf jedoch nicht außer Acht gelassen werden, dass bei der APACT-Studie erstmalig das durch einen prüfungszentrumunabhängigen Gutachter (IR = independent reviewer) beurteilte krankheitsfreie Überleben (DFS = disease-free survival) als primärer Endpunkt festgelegt wurde. Die Bewertung erfolgte ausschließlich anhand von CT-Material ohne Bewertung der klinischen Verläufe oder der Entwicklung von Tumormarkern. Das DFS nach Maßgabe des Prüfarztes, ein sekundärer Endpunkt der APACT-Studie, zeigte einen signifikanten Vorteil für die Kombinationschemotherapie (16,6 Monate versus 13,7 Monate; HR: 0,82; 95-%-KI: 0,69─0,97; p = 0,0168). Das mediane IR-beurteilte DFS, der primäre Endpunkt der Studie, ergab dagegen keinen signifikanten Vorteil von nab-P+Gem gegenüber der Gem-Monotherapie (19,4 Monate versus 18,8 Monate; HR: 0,88; 95-%-KI: 0,73─1,06; p = 0,1824). Auf dem diesjährigen ESMO-Kongress wurden nun die Interimsanalysen nach circa 38 Monaten Nachbeobachtung bezüglich des OS der stratifizierten Subgruppen Resektionsstatus (R1: 24%) und Lymphknotenstatus (LN+ = positive Lymphknoten: 72%) vorgestellt [12]. Nur in der LN+-Gruppe konnte im Kombinationsarm ein signifikanter Überlebensvorteil mit einem Median von 33,8 Monaten gegenüber 28,9 Monaten im Monotherapiearm gezeigt werden (HR: 0,79; 95-%-KI: 0,64─0,97; p=0,025) (Abb. 4).
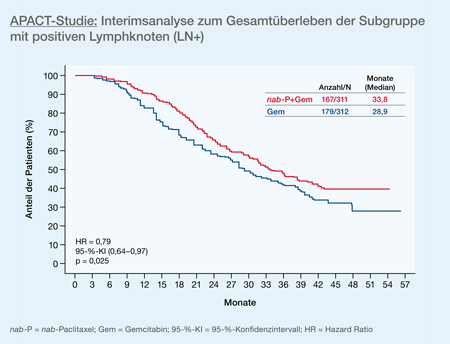 Abb. 4: APACT-Studie: in der Subgruppe der LN+-Patienten war das mediane Gesamtüberleben im nab-P+Gem-Arm gegenüber dem Gem-Arm signifikant verlängert (modifiziert nach [12])
Abb. 4: APACT-Studie: in der Subgruppe der LN+-Patienten war das mediane Gesamtüberleben im nab-P+Gem-Arm gegenüber dem Gem-Arm signifikant verlängert (modifiziert nach [12])Die R1-Subgruppe (32,5 Monate vs. 27,0 Monate) sowie die R1/LN+-Subgruppe (30,7 Monate versus 24,9 Monate) zeigten nur einen Trend zum besseren Gesamtüberleben unter einer Kombinationstherapie aus nab-P+Gem.
Hanno Riess stellte aktuelle Daten der APACT-Studie zur Lebensqualität vor [13]. Die Lebensqualitätsindizes, die anhand der EORTC(European Organisation for Research and Treatment of Cancer)-QLQ-C30- und PAN26-Bogen erhoben wurden, zeigten eine etwas stärkere vorübergehende Beeinträchtigung der Lebensqualität während der Chemotherapie. In der Nachbeobachtung war jedoch kein Unterschied mehr zu verzeichnen, was auf reversible Toxizitäten hinweist.
Fazit
- Die Subgruppenzwischenanalyse der APACT-Daten konnte nur für Patienten mit Lymphknotenbefall einen signifikanten Überlebensvorteil unter einer adjuvanten Kombinationschemotherapie aus nab-Paclitaxel+Gemcitabin im Vergleich zu einer Gemcitabin-Monotherapie zeigen.
- Die adjuvante Therapie mit der Kombination aus nab-Paclitaxel+Gemcitabin ist relativ gut verträglich und führt während des Therapieintervalls zwar zu einer signifikanten, aber rasch reversiblen Einschränkung der Lebensqualität im Vergleich zu einer Monotherapie mit Gemcitabin.
- Zur adjuvanten Therapie wurden keine neuen, “practice changing”-Ansätze vorgestellt. Das modifizierte FOLFIRINOX-Regime [14] bei relativ jungen und fitten Patienten beziehungsweise die Gemcitabin-Monotherapie, gegebenenfalls mit Capecitabin im Off-Label-Use, bleiben der Therapiestandard.
„Beim Pankreaskarzinom ist die Bewertung eines möglichen Rezidivs sehr wahrscheinlich nicht alleine nur durch die Bildgebung möglich. Der klinische Verlauf, die Entwicklung des Tumormarkers CA19-9 sowie der Vergleich mit den Vorbefunden müssen dabei mit einfließen. Die Wahl des primären Endpunktes sollte daher auch sehr sorgfältig getroffen werden. Anstelle des krankheitsfreien Überlebens nach Meinung eines unabhängigen Gutachters („DFS by IR“) könnte der Endpunkt „Zeit bis zur ersten Folgetherapie“ (TFST) eine Alternative sein.“ Dr. med. Gabriele Siegler
Erwähnenswert ist auch die prospektive dänische BIOPAC-Studie (NCT03311776) von Louise Rasmussen et al. [15]. Bei 1.271 Patienten mit Pankreaskarzinom wurden die prätherapeutischen Vitamin-D-Serumspiegel ermittelt. Patienten mit Serumspiegeln über 50 nmol/l (232 Patienten), insbesondere im Stadium I/II, hatten ein signifikant verlängertes OSS im Vergleich zu Patienten mit Serumspiegeln unter 25 nmol/l (24 Patienten) (27,8 Monate versus 18,3 Monate; HR: 1,36; 95-%-KI: 1,10─1,68, p < 0,01). Ob dieser Effekt aufgrund eines besseren Allgemeinzustandes oder anderer Lebensfaktoren bedingt ist, müssen zukünftige Studien zeigen.
Auf dem Gebiet der Grundlagenforschung wurden im Rahmen eines ESMO-Colloquiums von David K. Chang (What are the biological reasons for treatment resistance in pancreatic adenocarcinoma?), Eileen M. O`Reilly (New targets on the horizon: Integrating genomics with tumour microenvironment) und David A. Tuveson (Molecular profiling of pancreatic cancer in guiding tumour biology understanding and drug target discovery) sehr interessante Daten zu multiplen Resistenzmechanismen, molekularen Signaturen und deren unterschiedlicher Sensitivität gegenüber den verschiedenen Zytostatika vorgestellt. Ob und wann diese Erkenntnisse den Weg in die Klinik finden, bleibt jedoch noch abzuwarten.
Quellen
- Hammel P et al. Phase II LAPACT trial of nab-paclitaxel (nab-P) plus gemcitabine (G) for patients with locally advanced pancreatic cancer (LAPC). Journal of Clinical Oncology 2018; 36: 204-204.
- Hammel P et al. Effect of Chemoradiotherapy vs Chemotherapy on Survival in Patients With Locally Advanced Pancreatic Cancer Controlled After 4 Months of Gemcitabine With or Without Erlotinib: The LAP07 Randomized Clinical Trial. JAMA 2016; 315: 1844-1853.
- Mukherjee S et al. Gemcitabine-based or capecitabine-based chemoradiotherapy for locally advanced pancreatic cancer (SCALOP): a multicentre, randomised, phase 2 trial. The Lancet. Oncology 2013; 14: 317-326.
- Kunzmann V et al. Conversion rate in locally advanced pancreatic cancer (LAPC) after nab-paclitaxel/gemcitabine- or FOLFIRINOX-based induction chemotherapy (NEOLAP): Final results of a multicenter randomised phase II AIO trial. Presented at Proffered paper session 1 – Gastrointestinal tumours, non-colorectal, ESMO Congress 2019, Barcelona, abstract 671O. .
- Alvarez R et al. Stromal disrupting effects of nab-paclitaxel in pancreatic cancer. British journal of cancer 2013; 109: 926-933.
- Cascinu S et al. Nab-paclitaxel (Nab) plus gemcitabine (G) is more effective than G alone in locally advanced, unresectable pancreatic cancer (LAUPC): The GAP trial, a GISCAD phase II comparative randomized trial. Presented at Poster discussion session – Gastrointestinal tumours, non-colorectal, ESMO Congress 2019, Barcelona, abstract 673PD.
- Golan T et al. Maintenance Olaparib for Germline BRCA-Mutated Metastatic Pancreatic Cancer. New England Journal of Medicine 2019; 381: 317-327.
- Hammel P et al. POLO: Health-related quality of life (HRQoL) of olaparib maintenance treatment versus placebo in patients with a germline BRCA mutation and metastatic pancreatic cancer (mPC). Presented at Poster discussion session – Gastrointestinal tumours, non-colorectal, ESMO Congress 2019, Barcelona, abstract 675PD.
- Garcia-Carbonero R et al. Systemic administration of the hyaluronidase-expressing oncolytic adenovirus VCN-01 in patients with advanced or metastatic pancreatic cancer: First-in-human clinical trial. Poster display session 2, ESMO Congress 2019, Barcelona, abstract 710P. .
- Tempero MA et al. APACT: phase III, multicenter, international, open-label, randomized trial of adjuvant nab-paclitaxel plus gemcitabine (nab-P/G) vs gemcitabine (G) for surgically resected pancreatic adenocarcinoma. Journal of Clinical Oncology 2019; 37: 4000-4000.
- Von Hoff DD et al. Increased Survival in Pancreatic Cancer with nab-Paclitaxel plus Gemcitabine. New England Journal of Medicine 2013; 369: 1691-1703.
- Tempero M et al. Phase III, international, multicenter, randomized, open-label trial of adjuvant nab-paclitaxel plus gemcitabine (nab-P/G) vs gemcitabine (G) alone for surgically resected pancreatic adenocarcinoma (APACT): Subgroup analyses. Presented at Poster display session 2, ESMO Congress 2019, Barcelona, abstract 682P.
- Riess H et al. Impact of adjuvant treatment with nab-paclitaxel and gemcitabine (nab-P+GEM) vs gemcitabine alone (GEM) on health-related quality of life (QoL) in patients (pts) with surgically resected pancreatic adenocarcinoma (PA) in the adjuvant pancreatic adenocarcinoma clinical trial (APACT). Presented at Poster display session 2, ESMO 2019, Barcelona, abstract 684P.
- Conroy T et al. FOLFIRINOX or Gemcitabine as Adjuvant Therapy for Pancreatic Cancer. New England Journal of Medicine 2018; 379: 2395-2406.
- Rasmussen L et al. Pre-treatment serum 25-hydroxyvitamin D levels and survival in a Danish cohort of patients with pancreatic cancer. Presented at Poster display session 2, ESMO Congress 2019, Barcelona, abstract 699P.
- Bildnachweis: „Ceramic bench and entrance pavilion of park Guell”: © David Pereiras/Adobe Stock; "port de barcelone": © Lotharingia /Adobe Stock
Die Immuntherapie beim frühen Mammakarzinom ist auf dem Vormarsch
Prof. Dr. med. Diana Lüftner, Medizinische Klinik und Poliklinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie, Charité Campus Benjamin Franklin, Humboldt-Universität zu Berlin
 Die Diskussion der Therapieansätze beim Mammakarzinom nahm während des ESMO-Kongresses 2019 einen breiten Raum ein. Die erste von insgesamt 3 Presidential Sessions war ausschließlich Beiträgen zum Mammakarzinom gewidmet worden. Dies unterstreicht die Tatsache, wie sehr man auf neue Ideen und Ansätze wartet, um wirksamere Therapiestrategien zu entwickeln und umzusetzen.
Die Diskussion der Therapieansätze beim Mammakarzinom nahm während des ESMO-Kongresses 2019 einen breiten Raum ein. Die erste von insgesamt 3 Presidential Sessions war ausschließlich Beiträgen zum Mammakarzinom gewidmet worden. Dies unterstreicht die Tatsache, wie sehr man auf neue Ideen und Ansätze wartet, um wirksamere Therapiestrategien zu entwickeln und umzusetzen.
Mammakarzinom in der neoadjuvanten und adjuvanten Therapiesituation
KEYNOTE-522-Studie: Die neoadjuvante und adjuvante Behandlung mit einem Checkpointinhibitor beim tripelnegativen Mammakarzinom ist effektiv – Langzeitdaten fehlen allerdings noch
Auf Basis der KEYNOTE-173- und der I-SPY-2-Studie wurde die KEYNOTE-522-Studie (NCT03036488) als placebokontrollierte Phase-III-Untersuchung entwickelt. Sie prüfte Pembrolizumab sowohl im neoadjuvanten wie auch im adjuvanten Ansatz beim frühen tripelnegativen Mammakarzinom (TNBC). Peter Schmid stellte dazu auf dem diesjährigen ESMO-Kongress aktuelle Daten vor [1]. Abb. 1 zeigt das Studiendesign mit allen relevanten Einschluss- und Therapiekomponenten.
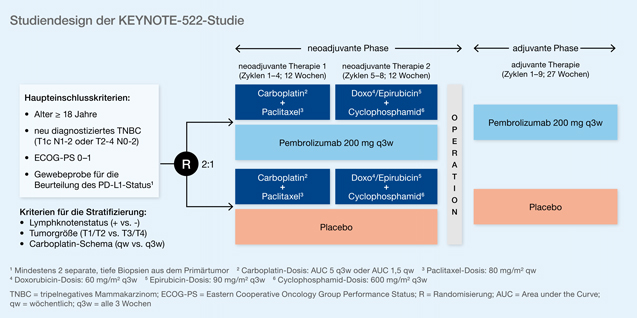
Abb. 1: KEYNOTE-522-Studie: Pembrolizumab+Chemotherapie versus Placebo+Chemotherapie beim tripelnegativen Mammakarzinom (modifiziert nach [1])
Die mediane Follow-up-Zeit war mit 15,5 Monaten eher kurz (Spannweite: 2,7–25,0 Monate). Insgesamt wurden 784 Patientinnen in den Pembrolizumab-Arm und weitere 390 Patientinnen in den Placeboarm randomisiert. Unter den insgesamt 602 Patientinnen, die bezüglich des primären Endpunktes, der pathologisch kompletten Remission (pCR), ausgewertet werden konnten, zeigte die Kombination aus Pembrolizumab+Chemotherapie eine statistisch signifikante Verbesserung (p = 0,00055) der pCR (ypT0/Tis ypN0) gegenüber Placebo+Chemotherapie mit Raten von 64,8% (95-%-Konfidenzintervall [95-%-KI]: 59,9–69,5) versus 51,2% (95-%-KI: 44,1–58,3). Das Ergebnis ist in Relation zur gesamten aktuell vorliegenden Evidenz erstaunlich, da sowohl bei der PD-L1(Programmed-Cell-Death-Ligand 1)-positiven wie auch bei der PD-L1-negativen Population ein relevanter Effekt gezeigt werden konnte (PD-L1-positive Population: Pembrolizumab versus Placebo: 68,9% versus 54,9%; PD-L1-negative Population: 45,3% versus 30,3%).
Auch das ereignisfreie Überleben (EFS) wurde durch die Hinzunahme von Pembrolizumab zur Chemotherapie gegenüber Placebo plus Chemotherapie verbessert (EFS nach 18 Monaten, Pembrolizumab-Arm: 91,3% versus Placeboarm: 85,3%; Hazard Ratio [HR]: 0,63; 95-%-KI: 0,43–0.93). Allerdings scheint angesichts der kurzen Nachbeobachtungszeit zunächst noch keine Euphorie angebracht zu sein. Neue Sicherheitssignale ergaben sich zwar nicht, da es sich aber um einen adjuvanten Therapieansatz handelt, ist Umsicht geboten. Es gibt keine Daten zur möglichen Beeinflussung der Fertilität und einige wenige Patientinnen werden auf jeden Fall die für Checkpointinhibitoren typischen Langzeitschäden, wie eine permanente Hypothyreose, erleiden.
IMpassion130-Studie: Die optimale Patientinnenselektion für die Checkpointblockade bleibt beim Mammakarzinom ein Buch mit sieben Siegeln
Die erste den Standard verändernde Studie zu den Checkpointinhibitoren beim metastasierten TNBC war die IMpassion130-Studie (NCT02425891) im Jahr 2018, in der Atezolizumab+nab-Paclitaxel gegenüber Placebo+nab-Paclitaxel als Erstlinienbehandlung geprüft wurde [2]. Die PD-L1-Positivität wurde in der Studie als Anteil der Immunzellen (IC) ≥ 1% der Tumorfläche mit Hilfe des VENTANA-PD-L1-SP142-IHC(Immunhistochemie)-Assays bestimmt. Hope S. Rugo stellte nun Daten einer Post-hoc-Analyse vor, welche die Konkordanz der SP142-Testung mit 2 anderen PD-L1-Immunhistochemie-Assays und ihrem prädiktiven Wert für den Nutzen der Therapie untersuchte [3]. Insgesamt wurden also 3 Techniken in einer zentralen Analyse genutzt: der VENTANA-PD-L1-SP142-Test, der VENTANA-PD-L1-SP263-Test (IC ≥ 1%, SP142+ oder SP263+) sowie der Dako-PD-L1-22C3-IHC-Test (Combined-Proportion-Score [CPS] ≥ 1, 22C3+).
Unter Berücksichtigung der jeweils gewählten Cut-off-Grenzen identifizierten die 22C3- und der SP263-Assay mehr Patientinnen mit PD-L1-positive Tumoren. Allerdings detektierte der SP142-PD-L1+-Assay innerhalb der positiven Population der beiden anderen Assays die Patientinnen mit dem größten Nutzen der Kombination aus Atezolizumab+nab-Paclitaxel: Fast alle Patientinnen mit SP142-Positivität waren auch 22C3-positiv und bedingten den Überlebensvorteil mit einer HR von 0,71 (95-%-KI: 0,52–0,98). Die SP142-negativen Patientinnen, die allerdings mit dem 22C3-Assay positiv waren, zeigten keinen Überlebensvorteil (HR: 0,92). Dies stützt durchaus den Ansatz, dass die Systemtherapie mit den hierfür entwickelten „Companion Diagnostics“ eingesetzt werden sollte.
Fazit
- Mit der KEYNOTE-522-Studie wurde ein neuer Meilenstein in der neoadjuvanten und adjuvanten Systemtherapie des tripelnegativen Mammakarzinoms gesetzt.
- Voraussetzung für eine bestmögliche Selektion der Patientinnen ist eine entitätenadaptierte, aus den Studien entlehnte Testung auf PDL-1.
- Es fehlen Daten für eine nachhaltige Abwägung der lebenslangen Toxizitäten, wenngleich es keine neuen Sicherheitssignale gibt. Man sollte zudem unbedingt über die bekannten unerwünschten Effekte hinaus an eine mögliche Beeinträchtigung der Fertilität denken.
“Es verbleiben zentrale Fragen: Was machen wir in Zukunft bei Patientinnen mit tripelnegativem Mammakarzinom, die schon in der Frühsituation einen Checkpointinhibitor erhalten haben und rasch rezidivieren? Würden wir mit dem erneuten Einsatz eines Checkpointinhibitors reexponieren, auch wenn es sich um eine andere Substanz handelt? Oder werten wir dies als Versagen der gesamten Substanzklasse? Welche Rolle spielt hier das rezidivfreie Intervall? Dies bleiben wichtige, zukünftig noch zu lösende Probleme.” Prof. Dr. med. Diana Lüftner
Metastasiertes Mammakarzinom
KATE2-Studie: Gesamtüberlebensvorteil unter Atezolizumab+Trastuzumab Emtansin bei vorbehandelten Patientinnen mit metastasiertem, HER2-positivem Mammakarzinom
Auch bei der HER2-positiven (HER2 = human epidermal growth factor receptor 2) Patientin in der metastasierten Situation gab es Daten zur Checkpointinhibition. Leisha A. Emens stellte Daten zum Gesamtüberleben (OS) aus der zweiarmigen Phase-II-KATE2-Studie (NCT02924883) vor [4]. Hier wurden tripelpositive Patientinnen, die nach einer Therapie mit Trastuzumab und einem Taxan in Mono- oder Kombinationstherapie eine Progression erlitten, 2 : 1 in einen Therapiearm mit Atezolizumab+Trastuzumab Emtansin (T-DM1) oder in einen Placeboarm mit Placebo+T-DM1 randomisiert. Abb. 2 zeigt das Studiendesign.
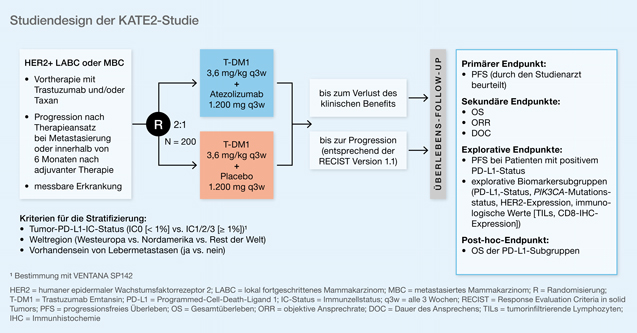
Abb. 2: KATE2-Studie: Atezolizumab+T-DM1 versus Placebo+T-DM1 beim tripelpositiven Mammakarzinom (modifiziert nach [4])
Bei einer medianen Follow-up-Zeit von rund 20 Monaten zeigte sich in der Gesamtgruppe kein Überlebensunterschied. In der PD-L1-positiven Subgruppe war das 1-Jahresüberleben allerdings im Therapiearm mit Atezolizumab+T-DM1 gegenüber dem Placeboarm mit Placebo+T-DM1 bei Bestätigung des bekannten Sicherheitsprofils numerisch verlängert (94,3% versus 87,9%).
Insgesamt bleibt die Zahl der OS-Ereignisse in dieser Studie jedoch noch zu klein. Auch ein statistisch signifikanter Effekt konnte aktuell noch nicht gezeigt werden. Dennoch sollte die Checkpointblockade in Kombinationstherapie auch beim HER2-positiven metastasierten Mammakarzinom weiter untersucht werden.
monarcHER-Studie: Abemaciclib+Fulvestrant+Trastuzumab könnte eine relevante Lücke im Armamentarium bei der Behandlung der tripelpositiven metastasierten Mammakarzinompatientin schließen
Die Nutzung der beiden gezielten Therapiemöglichkeiten, das heißt der endokrinen Therapie und der HER2-Inhibition, ist schon Inhalt vieler Phase-II/III-Studien gewesen. In der dreiarmigen Phase-II-monarcHER-Studie (NCT02675231) wurde nun erstmals der Nutzen des CDK4/6-Inhibitors (CDK4/6 = cyclinabhängige Kinase 4/6) Abemaciclib beim metastasierten tripelpositiven Mammakarzinom untersucht [5]. Das Studiendesign ist in Abb. 3 dargestellt.
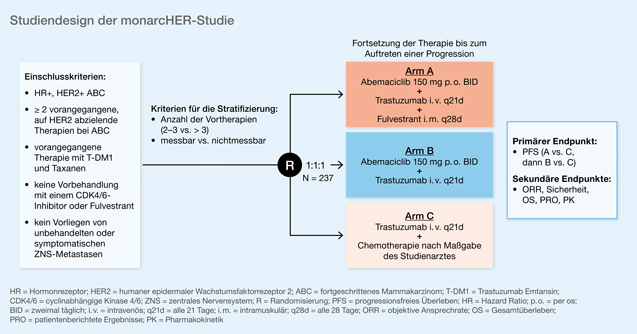
Abb. 3: monarcHER-Studie: Abemaciclib+Trastuzumab+Fulvestrant versus Abemaciclib+Trastuzumab versus Trastuzumab+Chemotherapie beim tripelpositiven metastasierten Mammakarzinom (modifiziert nach [5])
Der primäre Endpunkt der Studie, das mediane progressionsfreie Überleben (mPFS), war mit 8,3 Monaten im Dreifachtherapiearm mit Abemaciclib+Fulvestrant+Trastuzumab (Arm A) signifikant verlängert im Vergleich zum vordefinierten Kontrollarm, der Kombination von Trastuzumab+Chemotherapie nach Wahl des Studienarztes (8,3 Monate versus 5,7 Monate; HR: 0,673; 95-%-KI: 0,451–1,003; p = 0,0253). Der explorative Arm aus Abemaciclib+Trastuzumab (Arm B) dürfte klinisch keine relevante Rolle spielen. Zwischen Arm B und Arm C konnte kein Vorteil beim PFS festgestellt werden.
Die wahrscheinlich interessanteste Gruppe an Patientinnen, für welche diese Therapie einen Nutzen bringen könnte, sind die Patientinnen mit Hirnmetastasen, deren Anzahl mit der Zahl der Therapielinien zunimmt. Hier ist oft die vorbestehende Neuropathie therapielimitierend und die Knochenmarkreserve eingeschränkt. Insofern kann hier eine chemotherapiefreie Option bis zur Erholung von vorbestehenden Nebenwirkungen gewählt werden.
Endlich: Der Marathonlauf der CDK4/6-Inhibitoren geht mit überzeugenden Überlebensdaten ins Ziel
Mit den Überlebensdaten der MONARCH-2-Studie mit Abemaciclib [6] und der MONALEESA3-Studie mit Ribociclib [7] wurde die bereits vorliegende, ausgezeichnete Datenlage zu den CDK4/6-Inhibitoren beim hormonrezeptorpositiven metastasierten HER2- Mammakarzinom nachhaltig erweitert.
In der randomisierten, doppelt verblindeten Phase-III-MONARCH-2-Studie (NCT02107703) [6] wurde der Therapiearm mit Abemaciclib+Fulvestrant im Vergleich zum Placeboarm mit Placebo+Fulvestrant bei endokrin resistenten Patientinnen mit einem Hormonrezeptor(HR)-positiven, HER2-negativen metastasierten Mammakarzinom eingesetzt. An dieser Stelle wurde endokrine Resistenz (ER) wie folgt definiert: Progression unter neoadjuvanter Hormontherapie oder während/innerhalb eines Jahres der adjuvanten, endokrinen Therapie sowie Progression unter Erstlinienhormontherapie für die metastasierte Situation. Abb. 4 zeigt das Studiendesign.
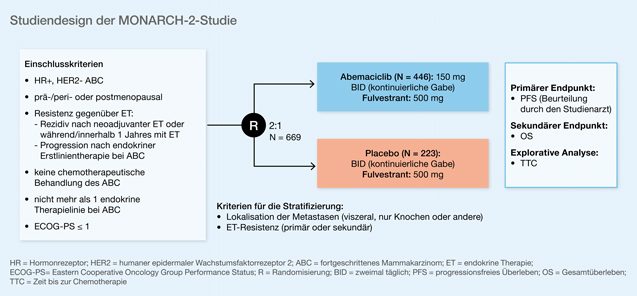
Abb. 4: MONARCH-2-Studie: Abemaciclib+Fulvestrant versus Placebo+Fulvestrant bei endokriner Resistenz beim fortgeschrittenen HR-positiven/HER2-negativen Mammakarzinom (modifiziert nach [6])
Das mediane OS lag im Abemaciclib+Fulvestrant-Arm bei 46,7 Monaten und bei 37,3 Monaten im Placebo+Fulvestrant-Arm (HR: 0,757; 95-%-KI: 0,606–0,945; p = 0,0137). Der Überlebensvorteil war über alle Stratifikationsfaktoren (Lokalisation der Metastasen, endokrine Resistenz) hinweg positiv mit einer besonders guten HR für die ungünstigen Gruppen mit viszeraler Metastasierung (HR: 0,675) und primärer endokriner Resistenz (HR: 0,686). Auch das PFS2 (PFS2 = Zeit von der Randomisierung bis zur Diagnose der erneuten Progression auf die nachfolgende Systemtherapie) war unter der Therapie mit Abemaciclib+Fulvestrant signifikant verbessert (HR: 0,675; 95-%-KI: 0,558–0,816). Parallel dazu war auch die Zeit bis zur ersten Chemotherapie in der Folge im Abemaciclib+Fulvestrant-Arm deutlich verbessert (HR: 0,622; 95-%-KI: 0,499–0,775).
Für ein der MONARCH-2-Studie sehr ähnliches Kollektiv wurde auch das Konzept der Phase-III-MONALEESA3-Studie (NCT02422615) entwickelt. Hier wurde das OS unter einer Therapie mit Ribociclib+Fulvestrant versus Placebo+Fulvestrant als Erstlinien- oder auch als Zweitlinientherapie bei postmenopausalen Patientinnen und männlichen Patienten mit HR-positivem, HER2-negativem fortgeschrittenem Mammakarzinom untersucht [7]. Das Studiendesign ist in Abb. 5 dargestellt.
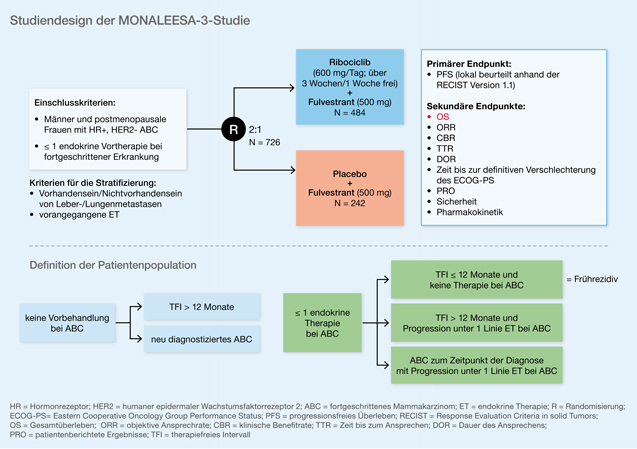
Abb. 5: MONALEESA-3-Studie: Ribociclib+Fulvestrant versus Placebo+Fulvestrant bei postmenopausalen Patientinnen mit fortgeschrittenem, HR-positivem/HER2-negativem Mammakarzinom (modifiziert nach [7])
In der MONALEESA3-Studie liegt die mediane Follow-up-Zeit bei 39,4 Monaten. Ribociclib+Fulvestrant zeigten einen signifikanten Überlebensvorteil gegenüber Placebo+Fulvestrant (HR: 0,724; 95-%-KI: 0,568–0,924; p = 0,00455). Per Protokoll handelt es sich bei den Daten zum OS um eine finale Analyse. Der Überlebensvorteil galt für alle Subgruppen. Für Patientinnen unter einer Erstlinientherapie lag das mediane PFS bei 33,6 Monaten für die Kombination aus Ribociclib+Fulvestrant versus 19,2 Monate für die Monotherapie mit Fulvestrant (HR: 0,546; 95-%-KI: 0,415–0,718). Es ist damit das längste PFS, das für Erstlinienpatientinnen in allen CDK4/6-Inhibitorstudien berichtet wurde.
Fazit
- Die Immuntherapie mit Checkpointinhibitoren beim metastasierten tripelnegativen Mammakarzinom bleibt vorerst die Domäne der Erstlinientherapie. Signale zugunsten einer Wirksamkeit bei vorbehandelten Patientinnen gibt es auch beim HER2-positiven Mammakarzinom.
- Patientinnen mit tripelpositivem metastasiertem Mammakarzinom können von einer optimierten Anti-HER2- und Anti-ER-Therapie profitieren. Gerade für zerebral metastasierte Patientinnen könnte dieser chemotherapiefreie Ansatz sehr entlastend sein.
- CDK4/6-Inhibitoren zeigen in der Behandlung des ER-positiven und HER2-negativen Mammakarzinoms einen Siegeszug mit eindrucksvollen Überlebensdaten.
“Die endokrine Monotherapie ist in der Behandlung des rezeptorpositiven metastasierten Mammakarzinoms nicht mehr der Standard. Es dürfte in der Zukunft sehr schwer werden, argumentativ zu untermauern, warum einer Patientin eine biologisch modifizierte Hormontherapie mit einem CDK4/6-Inhibitor vorenthalten werden sollte. Dies ist ethisch nicht mehr vertretbar.” Prof. Dr. med. Diana Lüftner
Quellen
- Schmid P et al. KEYNOTE-522: Phase III study of pembrolizumab (pembro) + chemotherapy (chemo) vs placebo (pbo) + chemo as neoadjuvant treatment, followed by pembro vs pbo as adjuvant treatment for early triple-negative breast cancer (TNBC). Presented at Presidential symposium II, ESMO Congress 2019, Barcelona, abstract LBA8_PR.
- Schmid P et al. Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. New England Journal of Medicine 2018; 379: 2108-2121.
- Rugo H et al. Performance of PD-L1 immunohistochemistry (IHC) assays in unresectable locally advanced or metastatic triple-negative breast cancer (mTNBC): Post-hoc analysis of IMpassion130. Presented at Proffered paper session - Breast cancer, metastatic, ESMO Congress 2019, Barcelona, abstract LBA20.
- Emens L et al. Overall survival (OS) in KATE2, a phase II study of programmed death ligand 1 (PD-L1) inhibitor atezolizumab (atezo)+trastuzumab emtansine (T-DM1) vs placebo (pbo)+T-DM1 in previously treated HER2+ advanced breast cancer (BC). Presented at Proffered paper session - Breast cancer, metastatic, ESMO Congress 2019, Barcelona, abstract 305O.
- Tolaney S et al. MonarcHER: A randomized phase II study of abemaciclib plus trastuzumab with or without fulvestrant versus trastuzumab plus standard-of-care chemotherapy in women with HR+, HER2+ advanced breast cancer (ABC). Presented at Proffered paper session - Breast cancer, metastatic, ESMO Congress 2019, Barcelona, abstract LBA23.
- Sledge G et al. MONARCH 2: Overall survival of abemaciclib plus fulvestrant in patients with HR+, HER2- advanced breast cancer. Presented at Presidential symposium II, ESMO Congress 2019, Barcelona, abstract LBA6_PR.
- Slamon D et al. Overall survival (OS) results of the phase III MONALEESA-3 trial of postmenopausal patients (pts) with hormone receptor-positive (HR+), human epidermal growth factor 2-negative (HER2−) advanced breast cancer (ABC) treated with fulvestrant (FUL) ± ribociclib (RIB). Presented at Presidential symposium II, ESMO Congress 2019, Barcelona, abstract LBA7_PR.
- Bildnachweis: „BARCELONA, SPAIN - AUGUST 12: Hotel Arts and Mapfre Tower and Pe”: © anko_ter/Adobe Stock
ESMO-Kongress 2019: Update zur Thoraxonkologie
Dr. med. Nikolaj Frost, Med. Klinik m. S. Infektiologie/Pneumologie, Charité
Universitätsmedizin Berlin
 Auf dem diesjährigen Kongress der European Society for Medical Oncology (ESMO) war die Thoraxonkologie stark vertreten. 2 wichtige Studien dazu (FLAURA, Checkmate-227) wurden in der ersten Presidential Session vorgestellt. Ein weiteres wichtiges Thema war die Immunonkologie mit all ihren Facetten. Schwerpunkte waren die Behandelbarkeit von Hirnmetastasen und der prädiktive Nutzen der Tumormutationslast-Testung.
Auf dem diesjährigen Kongress der European Society for Medical Oncology (ESMO) war die Thoraxonkologie stark vertreten. 2 wichtige Studien dazu (FLAURA, Checkmate-227) wurden in der ersten Presidential Session vorgestellt. Ein weiteres wichtiges Thema war die Immunonkologie mit all ihren Facetten. Schwerpunkte waren die Behandelbarkeit von Hirnmetastasen und der prädiktive Nutzen der Tumormutationslast-Testung.
Therapie des lokal fortgeschrittenen NSCLC
Simultane Radiochemoimmuntherapie mit Nivolumab
Die NICOLAS-Studie untersuchte den Wert einer simultanen Immuntherapie mit dem Checkpointinhibitor Nivolumab in Kombination mit einer Radiochemotherapie beim lokal fortgeschrittenen, nichtresektablen nichtkleinzelligen Lungenkarzinom (NSCLC) im Stadium IIIA/B [1]. In die einarmige Phase-II-Studie wurden 74 Patienten eingeschlossen. Nach PET-Staging und einem Zyklus Induktionschemotherapie erfolgte die simultane Radiochemoimmuntherapie (RCT). Nivolumab wurde in den ersten 4 Zyklen alle 3 Wochen in einer Dosis von 360 mg appliziert (die ersten 2 Applikationen erfolgten simultan zur RCT). Daran schloss sich eine Erhaltung mit 480 mg alle 4 Wochen bis zum Ablauf eines Jahres an. Die primären Endpunkte waren das Auftreten schwergradiger Pneumonitiden (mindestens G3) in den ersten 6 Monaten nach der RCT und das 1-Jahres-PFS (PFS = progressionsfreies Überleben). Nachdem die Sicherheitsdaten mit positivem Ergebnis bereits veröffentlicht worden sind [2], wurden aktuell nun die Daten zum PFS präsentiert. Dieses belief sich auf 12,7 Monate, was einem 1-Jahres-PFS von 50,7% entspricht. Allerdings ist die Rate der für eine statistische Signifikanz notwendigen Ereignisse bislang nicht erreicht (37 PFS-Ereignisse sind aufgetreten, 41 sind aber notwendig, um die Nullhypothese einer 1-Jahres-PFS-Rate von ≤ 45% zu widerlegen).
Radiochemotherapie: Langzeitdaten
Die 3-armige Studie WJTOGO105 der West Japan Thoracic Oncology Group untersuchte die Wirksamkeit verschiedener Chemotherapieregime bei einer simultanen Radiochemotherapie im Stadium IIIA/B [3]. Auf der Tagung der ESMO wurden jetzt die 10-Jahresdaten vorgestellt. Jeweils 150 Patienten wurden randomisiert auf eine Behandlung mit Cisplatin/Vindesin/Mitomycin C (Arm A), Carboplatin/Irinotecan (Arm B) beziehungsweise Carboplatin/Paclitaxel (Arm C) verteilt. Unter den gegebenen Präliminarien einer zum Behandlungszeitpunkt nicht implementierten PET-Diagnostik ergab sich eine 10-Jahres-Gesamtüberlebenswahrscheinlichkeit von 13,6% (Arm A), 7,5% (Arm B) und 15,2% (Arm C).
PACIFIC: Subset der Patienten mit Durvalumab und Pneumonitis
Im letzten Jahr wurden auf der ESMO-Tagung die Überlebensdaten der PACIFIC-Studie vorgestellt. Hierbei zeigte sich, dass der PD-L1(Programmed Cell Death Ligand 1)-Inhibitor Durvalumab die Überlebenszeit bei Patienten mit lokal fortgeschrittenem, nichtresezierbarem Lungenkrebs im Stadium III signifikant im Vergleich zu Placebo verlängert [4]. Aktuell wurden jetzt die Effizienzdaten einer Behandlung mit Durvalumab bei den Patienten vorgestellt, die unter oder nach einer Behandlung mit Radiochemotherapie+Durvalumab-Erhaltung eine Pneumonitis entwickelt hatten [5]. Von den initial 713 (2 : 1) randomisierten Patienten entwickelten 219 eine Pneumonitis (161 im Durvalumab-Arm, 58 im Placeboarm). Der überwiegende Anteil der Pneumonitiden im Durvalumab-Arm war mild (G1) oder moderat (G2) ausgeprägt (86,3%), 10,6% entwickelten eine G3/4-Toxizität. Eine durch eine Pneumonitis bedingte Behandlungsunterbrechung war bei 60 (37,3%), ein Behandlungsabbruch bei 30 Patienten notwendig (18,6%). 101 Patienten (62,7%) erhielten eine Behandlung mit systemischen Glukokortikoiden. Die Rate der Pneumonitistodesfälle war in der Durvalumab-Gruppe niedriger als in der Placebogruppe (3,1 vs. 8,6%), womöglich auch durch ein effektiveres Behandlungsansprechen mit vollständiger Restitution bedingt (49,1% vs. 36,2%). Das Auftreten einer Pneumonitis hatte verglichen mit der Intention-to-treat(ITT)-Population auch nach der Adjustierung für zeitabhängige Kovariaten keinen Einfluss auf das progressionsfreie Überleben und das Gesamtüberleben.
Fazit
- Eine simultane Radiochemoimmuntherapie mit Nivolumab ist den Ergebnissen der NICOLAS-Studie zufolge sicher durchführbar. Das darunter erzielte mediane PFS von 12,7 Monaten liegt jedoch unterhalb der Erwartungen an eine kombinierte Radiochemoimmuntherapie. Zur Effektivität der Kombination sind daher die Ergebnisse aktuell rekrutierender Studien zur Radiochemoimmuntherapie abzuwarten (z. B. KEYNOTE-799).
- Die Langzeitergebnisse der WJTOGO105-Studie sind wohl eher von akademischem Interesse. Denn die verwendeten Therapieregime finden teils keine Verwendung mehr, teils ändert sich die Behandlungslandschaft im Stadium III derzeit sowieso grundlegend dahingehend, die Immuntherapie bereits in die früheren Stadien zu integrieren.
- Einer Subgruppenauswertung der PACIFIC-Studie zufolge sind Pneumonitiden unter einer Durvalumab-Erhaltungstherapie zwar häufiger als in der Placebogruppe aufgetreten, 86,3% davon waren jedoch mit G1/2 mild ausgeprägt. Zudem sprachen diese zumeist gut auf Steroide an. Ein durch eine Pneumonitis bedingter Behandlungsabbruch war lediglich in 18,6% der Fälle notwendig.
“Pneumonitiden als Nebenwirkung der Immuntherapie sind ein wichtiger Fokus, zumal sie häufig schwierig zu behandeln sind. Die niedrige Rate schwergradiger Pneumonitiden unter einer Erhaltungstherapie mit Durvalumab nach einer Radiochemotherapie ist ermutigend und sollte keinesfalls davon abhalten, Patienten eine Erhaltungstherapie mit Immuntherapeutika zu ermöglichen. Wichtig ist hier jedoch die enge interdisziplinäre Zusammenarbeit zwischen Thoraxonkologen und Pneumologen.” Dr. med. Nikolaj Frost
Therapie des metastasierten NSCLC
Update zur Immuntherapie
Die Phase-III-Studie IMpower110 untersuchte die Effektivität einer Monotherapie mit dem PD-L1-Inhibitor Atezolizumab versus Chemotherapie bei 572 PD-L1-positiven Patienten mit NSCLC (ohne Mutation des epidermalen Wachstumsfaktorrezeptors [EGFR] bzw. ohne Translokation der anaplastischen Lymphomkinase [ALK]) [6]. Der primäre Endpunkt war das Gesamtüberleben. Die sekundären Endpunkte waren das progressionsfreie Überleben sowie die Ansprechrate und -dauer. Die Besonderheit der Studie war die Stratifizierung anhand des SP142-Antikörpers, der neben den Tumorzellen auch die Immunzellen markiert. Als hoch positiv gewertet wurden Patienten mit einer PD-L1-Expression von mindestens 50% auf den Tumorzellen (TC3) beziehungsweise von 10% auf den Immunzellen (IC3). Dies betraf 107 Patienten in der Interventionsgruppe (38,6%) und 98 in der Kontrollgruppe (35,4%). Das Gesamtüberleben (OS) lag in der TC/IC3-Gruppe unter der Atezolizumab-Behandlung bei 20,2 Monaten, die Kontrollgruppe erzielte 13,1 Monate, was einer Hazard Ratio (HR) von 0,59 (95-%-KI: 0,40−0,89; p = 0,011) entspricht (Abb.1). Die Subgruppenanalyse zeigte abgesehen von Patienten, die niemals geraucht hatten, konsistente Vorteile für die Immuntherapie mit Atezolizumab. Auch das PFS für die Subgruppe der TC/IC3 war mit 8,1 versus 5,0 Monaten (HR 0,63, 95-%-KI: 0,45−0,88; p = 0,007) deutlich besser unter der Behandlung mit Atezolizumab. Dies spiegelte sich auch in höheren Ansprechraten (38,3% vs. 28,6%) und einer längeren Ansprechdauer wider (NE vs. 5,7 Monate). PFS und OS waren bei geringerer PD-L1-Expression zwar ebenfalls besser unter Atezolizumab, da die Gesamtkohorte jedoch deutlich durch die Gruppe der PD-L1-Hochexprimierer getragen wurde und keine Einzelgruppenanalysen für PD-L1 < 50% vorgestellt wurden, steht der Nachweis einer Überlegenheit von Atezolizumab bei diesen Patienten noch aus. Die Sicherheitsanalyse erbrachte keine neuen unerwarteten Signale. Therapieassoziierte Grad-3/4-Nebenwirkungen traten bei 12,9% beziehungsweise 44,1% der Patienten, G3/4-immunvermittelte Nebenwirkungen bei 6,6% und 1,5% der Patienten auf.
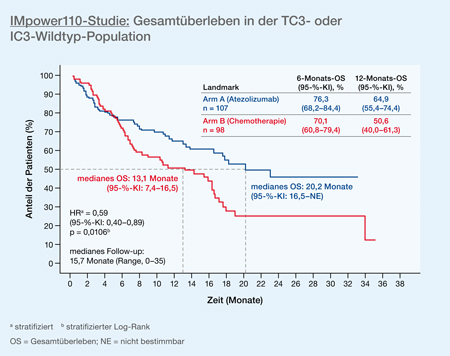 Abb. 1: Gesamtüberleben bei Patienten mit NSCLC ohne ALK- oder EGFR-Mutation (WT) und hoher PD-L1-Expression (TC3/IC3) unter Atezolizumab im Vergleich zur Chemotherapie (modifiziert nach [6]).
Abb. 1: Gesamtüberleben bei Patienten mit NSCLC ohne ALK- oder EGFR-Mutation (WT) und hoher PD-L1-Expression (TC3/IC3) unter Atezolizumab im Vergleich zur Chemotherapie (modifiziert nach [6]).Die CheckMate-227-Studie (Teil 1) untersuchte die Wirkung von Nivolumab und dem CTLA-4-Inhibitor Ipilimumab beziehungsweise Nivolumab versus Chemotherapie (Abb. 2) [7]. 1.166 therapienaive Patienten ohne EGFR-Mutationen und ALK-Rearrangement wurden anhand ihrer PD-L1-Expression (negativ vs. mind. 1%) und nach Histologie stratifiziert auf jeweils 3 Behandlungsarme (Nivolumab+Ipilimumab, Nivolumab (+Chemotherapie bei PD-L1-Negativität), Chemotherapie) aufgeteilt. Co-primäre Endpunkte waren das PFS in der Subgruppe der Patienten mit hoher Tumormutationslast (hohe Tumormutationslast [TMB] = mindestens 10 Mutationen/Megabase [Mut/Mb]) und das Gesamtüberleben unter den PD-L1-positiven Patienten. Die Daten zum ersten Endpunkt wurden bereits 2018 veröffentlicht und waren positiv [8]. Allerdings stellte sich bei der Auswertung der Patienten mit niedriger TMB (< 10 Mut/Mb) heraus, dass der Faktor in der Studie zwar einen prognostischen, aber keinen prädiktiven Wert besaß, da die HR für das OS unabhängig vom TMB-Status war (0,77 bzw. 0,78). Aktuell wurden nun nach einer Nachbeobachtungszeit von mindestens 29,3 Monaten die Überlebensdaten abhängig von der PD-L1-Expression vorgestellt. Bei PD-L1-positiven Patienten wurde mit der Kombinationsimmuntherapie verglichen mit der Chemotherapie ein deutlich verlängertes medianes Gesamtüberleben erzielt (17,1 vs. 14,9 Monate, HR 0,79, 95-%-KI: 0,65−0,96; p = 0,007). Mit einer Nivolumab-Monotherapie war das Überleben im Vergleich zur Chemotherapie statistisch nicht signifikant verlängert (HR 0,88, 95-%-KI: 0,75−1,04). Bei numerisch nicht allzu groß differierenden Ansprechraten (Nivolumab/Ipilimumab 35,9%, Nivolumab 27,5%, Chemotherapie 30,0%) war die Dauer des Ansprechens mit der (Doppel-)Immuntherapie jedoch deutlich verlängert (23,2 vs. 15,5 vs. 6,2 Monate). In der explorativen Analyse der Patienten mit hoher PD-L1-Expression (mindestens 50%) schnitt die Immuntherapie im Gesamtüberleben nochmals etwas besser ab (HR 0,70 für Nivolumab/Ipilimumab vs. Chemotherapie bzw. 0,79 für Nivolumab vs. Chemotherapie. Bei den PD-L1-negativen Patienten wurde mit der Doppelimmuntherapie ein numerisch gleiches Überleben wie bei den PD-L1-positiven Patienten erzielt (17,2 Monate). Aufgrund des schlechteren Outcomes in der Chemotherapiegruppe (12,2 Monate) zeigte sich eine nochmals zugunsten von Nivolumab/Ipilimumab verschobene HR (HR für OS 0,62, 95-%-KI: 0,48−0,78). Nivolumab plus Chemotherapie war erneut statistisch nicht signifikant besser als die Chemotherapie alleine (HR 0,78, 95-%-KI: 0,60−1,02). In dieser Kohorte wurde bei den PD-L1-negativen Patienten die höchste Ansprechrate erzielt (37,9%), allerdings war die Dauer des Therapieansprechens erneut mit der Doppelimmuntherapie am längsten (18,0 vs. 8,3 (Nivolumab+Chemotherapie) vs. 4,8 (Chemotherapie) Monate). Für das Überleben der Gesamtkohorte ergab sich unabhängig von der PD-L1-Expression eine HR von 0,73 zugunsten der Doppelimmuntherapie (95-%-KI: 0,64−0,84). Das gute Abschneiden wurde jedoch um den Preis relativ hoher Toxizitäten erkauft. Die Rate der Grad-3/4-Nebenwirkungen war mit Nivolumab/Ipilimumab mit 33% fast doppelt so hoch wie mit Nivolumab alleine (19%) und vergleichbar mit der Chemotherapiegruppe (36%).
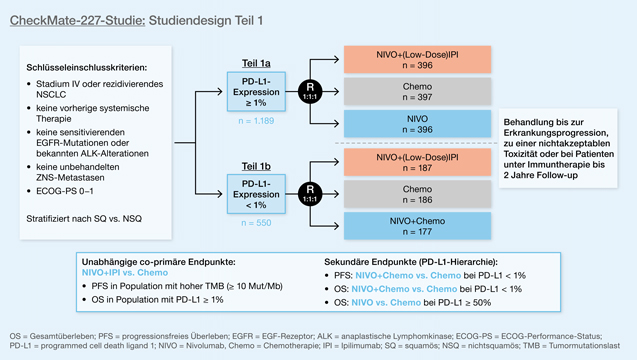 Abb. 2: Studiendesign von Teil 1 der Phase-III-CheckMate-227-Studie, die eine duale Immuntherapie mit Nivolumab+Low-Dose-Ipilimumab bei Patienten mit einer PD-L1-Expression von ≥ 1% und einer PD-L1-Expression < 1% untersuchte (modifiziert [7])
Abb. 2: Studiendesign von Teil 1 der Phase-III-CheckMate-227-Studie, die eine duale Immuntherapie mit Nivolumab+Low-Dose-Ipilimumab bei Patienten mit einer PD-L1-Expression von ≥ 1% und einer PD-L1-Expression < 1% untersuchte (modifiziert [7])Die KEYNOTE-407-Studie untersuchte den Benefit einer Behandlung mit Carboplatin/nab-Paclitaxel und dem PD-1-Rezeptorblocker Pembrolizumab versus alleinige Chemotherapie bei 559 Patienten mit metastasiertem NSCLC mit plattenepithelialer Histologie [9]. Die primären Endpunkte PFS und OS sind bereits 2018 publiziert worden [10]. Aktuell wurde nun das zweite progressionsfreie Überleben (PFS2) berichtet, also die Zeitspanne zwischen der Randomisierung und einem Progress nach der Zweitlinienbehandlung beziehungsweise Tod. Dieser Parameter stellt einen zunehmend verwendeten soliden Zwischenparameter zwischen PFS und OS dar und füllt die Lücke zwischen der Erstlinientherapie und dem Gesamtüberleben. Konsistent zu den Vorergebnissen zeigte sich erneut ein deutlicher Vorteil für die Tripeltherapie aus Carboplatin/nab-Paclitaxel und Pembrolizumab mit einem PFS2 von 13,8 versus 9,1 Monaten (HR 0,59, 95-%-KI: 0,49−0,72). Dieser war unabhängig von der PD-L1-Expression (mindestens 50%: HR 0,61, 1−49%: HR 0,51, < 1%: 0,61).
In der Phase-II-Studie B-F1RST wurde der prädiktive Nutzen von im Blut gemessener Tumormutationslast (bTMB) für eine Behandlung mit Atezolizumab als Erstlinientherapie untersucht [11]. Die primären Endpunkte waren das Therapieansprechen und das progressionsfreie Überleben. In der ITT-Population (n = 152) lag die objektive Ansprechrate (ORR) bei 17,1%, während sich in der Gruppe der bTMB-auswertbaren Patienten (n = 119) ein mit steigenden TMB-Cut-offs zunehmender prädiktiver Wert zeigte. Bei einem Schwellenwert von 16 lag die ORR bei 35,7 vs. 5,5% (p < 0,0001) für die TMB-hoch-Patienten versus die Subgruppen mit niedriger TMB. Dies übersetzte sich auch in ein (statistisch nicht signifikant) verlängertes PFS für die TMB-hoch-Patienten von 5,0 Monaten vs. 3,5 Monate (HR 0,80, 95-%-KI: 0,54−1,18). Das OS ist zwar numerisch ebenfalls deutlich zugunsten der TMB-hoch-Gruppe verschoben (23,9 vs. 13,4 Monate), allerdings sind die Daten für eine belastbare Auswertung noch nicht reif genug.
TMB-Testung
In einer Auswertung der Pembrolizumab-Studien KEYNOTE(KN)-010 und -042 [12] sowie -021, -189 und -407 [13] wurde der prädiktive Nutzen einer Messung der Tumormutationslast (TMB) im Gewebe untersucht, welche mittels Whole-Exome-Sequencing (WES) bestimmt wurde. Als Cut-off wurde ein aus Vorstudien ermittelter Wert von 175 Mutationen/Exom festgelegt. Dabei handelte es sich um eine explorative Analyse. Aus den Studien zur Monotherapie (KN-010 und -042) war eine Auswertung bei 1.046 von 2.300 Patienten möglich. Bei unveränderten Baselinecharakteristika konnte der prädiktive Nutzen in der Gruppe der TMB-hochexprimierenden Patienten in beiden Studien gut belegt werden (KN-010: HR für OS 0,56, KN-042: HR für OS 0,62), während bei < 175 Mut/Exom die Immuntherapie und die Chemotherapie ähnliche Ergebnisse erbrachten (HR 0,85 und 1,09). Erwartungsgemäß lagen die Ansprechraten bei den Patienten mit einer hohen TMB-Expression unter einer Behandlung mit Pembrolizumab deutlich höher. Mit einer Kombinationstherapie (KN-021, -189, -407) wurden 1.322 Patienten behandelt, bei 675 war eine TMB-Bestimmung möglich. Auch hier lag eine hohe Übereinstimmung der Baselinecharakteristika vor. Interessanterweise war nun der prädiktive Wert der TMB-Bestimmung nicht mehr nachweisbar. In allen Studien gab es keine Korrelation zwischen PD-L1-Expression und TMB.
Behandlung von Hirnmetastasen
Hirnmetastasen stellen eine Achillesferse in der Behandlung des Lungenkarzinoms dar. In der klinischen Routine treten sie bei circa 30% der Neudiagnosen auf und sie sind im Krankheitsverlauf bei etwa der Hälfte aller Patienten nachweisbar [14]. Auf dem diesjährigen ESMO-Kongress wurden mehrere Studien zur intrakraniellen Effektivität der jeweiligen Therapien vorgestellt.
Die ASCEND-7-Phase-II-Studie untersuchte die intrakraniellen Effekte einer Therapie mit dem Tyrosinkinaseinhibitor Ceritinib bei insgesamt 156 Patienten mit ALK-transloziertem NSCLC und aktiven Hirnmetastasen [15]. Die Patienten wurden in Abhängigkeit von einer ALK-wirksamen Vortherapie, einer zerebralen Strahlentherapie beziehungsweise dem Nachweis einer Leptomeningeosis carcinomatosa randomisiert auf 5 Kohorten verteilt und mit der Standarddosis Ceritinib (750 mg/d) behandelt. Der primäre Endpunkt war das Therapieansprechen insgesamt, ein sekundärer Endpunkt war die intrakranielle Effektivität. Aktuell wurden jetzt die Daten aus den Kohorten 1−4 präsentiert. Die Ergebnisse zur Meningeosis stehen noch aus. Wie im Rahmen von Studien zu treibermutierten Lungenkarzinomen zu erwarten, waren die Patienten im Median deutlich jünger (47,5−53,5 Jahre) und hatten überwiegend niemals geraucht (50−73,8%). Das beste Therapieansprechen war in der Gruppe der therapienaiven Patienten ohne vorherige Strahlentherapie zu verzeichnen (ORR 59,1%), gefolgt von der Gruppe der vorbestrahlten Patienten (ORR 50,0%). Demgegenüber lag die ORR bei mit Crizotinib vorbehandelten Patienten mit 30% (ohne Strahlentherapie) beziehungsweise 35,7% (mit Strahlentherapie) deutlich niedriger. Die Dauer des Therapieansprechens lag bei 9,2 bis 12,8 Monaten. Allerdings sprachen die therapienaiven, vorbestrahlten Patienten deutlich länger an (die mediane Dauer des Ansprechens [DoR] bislang nicht erreicht). Das mediane Gesamtüberleben lag in der Gruppe der vorbehandelten und bestrahlten Patienten bei 24,0 Monaten, die restlichen Kohorten sind aufgrund fehlender Datenreife bislang nicht auswertbar. Die höchste intrakranielle Ansprechrate wurde – bei insgesamt über alle 4 Kohorten hinweg hohen intrakraniellen Tumorkontrollraten (75,0−85,7%) – mit 51,5% ebenfalls bei den therapienaiven, nicht bestrahlten Patienten erreicht.
Eine weitere Studie aus China untersuchte potenzielle Zusammenhänge zwischen Hirnmetastasen und somatischen Mutationen sowie spezifischen Methylierungsmustern bei 60 Patienten in Abhängigkeit des Vorhandenseins von Hirnmetastasen beziehungsweise einer Meningeosis [16]. Bei einer hohen Konkordanz zwischen Primarius und Metastase konnten jedoch keine eindeutigen (prädiktiven) Muster identifiziert werden.
2 gepoolte Auswertungen der KEYNOTE-Studien untersuchten die Effizienz einer Behandlung mit Pembrolizumab auf das Outcome bei Patienten mit Hirnmetastasen entweder als Mono- (KN-001, -010, -024, -042; Gruppe 1) [17] oder Immunchemotherapie (KN-021, -189 und -407; Gruppe 2) [18]. Von den insgesamt 3.170 in Gruppe 1 behandelten Patienten wiesen 9,2% Hirnmetastasen auf (n = 293). Verglichen mit Patienten ohne Hirnmetastasen zeigte sich eine Verbesserung des PFS lediglich bei hoher PD-L1-Expression (mindestens 50%: HR 0,70 vs. 0,69; PD-L1 mind. 1%: HR 0,96 vs. 0,91), während das OS unabhängig vom PD-L1-Status durch eine Behandlung mit Pembrolizumab verbessert werden konnte (PD-L1 mind. 1%: HR 0,83 vs. 0,78).
Von insgesamt 1.300 in Gruppe 2 behandelten Patienten wiesen 13,2% (n = 171) Hirnmetastasen auf. Bei insgesamt schlechterer Prognose bei vorhandenen Hirnmetastasen verbesserte die Hinzunahme von Pembrolizumab das Überleben gegenüber der Chemotherapie deutlicher als bei den Patienten ohne Hirnmetastasen (18,8 vs. 7,6 Monate mit Hirnmetastasen, HR 0,48, 95-%-KI: 0,32−0,70; bzw. 22,5 vs. 13,5 Monate ohne Hirnmetastasen, HR 0,63, 95-%-KI: 0,53−0,75).
Fazit
- Atezolizumab als Monotherapie zeigte in der IMpower110-Studie in der Gruppe der PD-L1-Hochexprimierer eine mit Pembrolizumab vergleichbare Effektivität (OS 20,2 Monate, HR 0,59). Da aufgrund der besonderen PD-L1-Testung auch Patienten mit mindestens 10% PD-L1-Expression auf den Immunzellen als hoch positiv gewertet wurden, könnte sich bei entsprechender Zulassung das Spektrum der mittels Monotherapie behandelbaren Patienten künftig erweitern.
- Eine Doppelimmuntherapie mit Nivolumab und Ipilimumab verbessert das Überleben gegenüber einer Chemotherapie unabhängig vom PD-L1-Status (HR 0,73), scheint jedoch insbesondere bei PD-L1-Negativität sehr effektiv zu sein (HR 0,62). Insgesamt ist die Behandlung jedoch deutlich toxischer als eine Monoimmuntherapie.
- In gepoolten Analysen multipler Studien mit Pembrolizumab zeigte sich eine gute Wirksamkeit auch bei Patienten mit Hirnmetastasen. Trotz beeindruckender Patientenzahlen ist der klinische Nutzen der Auswertung fraglich, da die Studienpopulation die klinische Realität nicht widerspiegelt. 9 beziehungsweise 13% der Patienten mit Hirnmetastasen liegen deutlich unterhalb der in der klinischen Realität zu erwartenden Raten. Zudem mussten Hirnmetastasen vor Studieneinschluss vorbestrahlt und stabil sein. Steroide waren großteils nicht zugelassen und die Patienten mussten hinsichtlich der Hirnmetastasen asymptomatisch sein. Insgesamt ist in den beiden Auswertungen eine prognostisch günstige Patientenselektion anzunehmen, die die Übertragbarkeit der Ergebnisse auf die Alltagsrealität zweifelhaft erscheinen lässt.
- Die Frage nach einem additiven Nutzen einer TMB-Bestimmung für das Ansprechen auf eine Immuntherapie kann weiterhin nicht endgültig beantwortet werden. Aktuell zeigte eine Untersuchung multipler Studien mit Pembrolizumab zwar einen prädiktiven Wert in der Monotherapie, nicht jedoch in Kombination mit einer Chemotherapie. Demgegenüber war in der (bereits 2018 vorgestellten) Checkmate-227-Studie mittels TMB (Cut-off 10 Mutationen/Megabase) bei unverändertem Ansprechen auf eine Doppelimmuntherapie mit Nivolumab und Ipilimumab keinerlei Prädiktion möglich (HR für OS: TMB hoch 0,77, TMB niedrig 0,78), es zeigte sich jedoch ein prognostischer Wert mit längerem Überleben in der TMB-hoch-Kohorte. Aufgrund der widersprüchlichen Ergebnisse der einzelnen Studien ist nicht mit einer baldigen Verwendung der TMB-Testung im klinischen Alltag zu rechnen.
- Hirnmetastasen treten im klinischen Alltag häufig auf, sind in klinischen Studien jedoch zumeist unterrepräsentiert. Ceritinib zeigt eine sehr gute intrakranielle Aktivität bei aktiven Hirnmetastasen, allerdings ist die Wirksamkeit bei jeglicher Vorbehandlung (entweder mittels ALK-Tyrosinkinase-Inhibitoren und/oder Strahlentherapie) deutlich geringer ausgeprägt.
“Eine Erweiterung des Spektrums der in der Erstlinienbehandlung chemotherapiefrei behandelbaren Patienten ist aus Patientensicht absolut wünschenswert. Die Ergebnisse der CeckMate-227-Studie füllen hier eine vorhandene Lücke. Es bleibt jedoch abzuwarten, in welcher Form die EMA das Regime zulässt.” Dr. med. Nikolaj Frost
Zielgerichtete Therapien
EGFR-mutiertes NSCLC: Update zur FLAURA-Studie
In die FLAURA-Studie wurden 556 therapienaive Patienten mit EGFR-Mutationen (Exon-19-Deletionen und L858R-Punktmutationen im Exon 21) aufgenommen und 1 : 1 randomisiert auf eine Behandlung mit Osimertinib beziehungsweise die Standardbehandlung mittels Erstgenerations-EGFR-TKI (Gefitinib oder Erlotinib) verteilt [19]. Die Ergebnisse zum primären Endpunkt PFS wurden bereits veröffentlicht [20]). Aktuell wurden nun die Gesamtüberlebensdaten vorgestellt. Der bereits beim PFS gezeigte Vorteil für Osimertinib (18,9 vs. 10,2 Monate, HR 0,46, 95-%-KI: 0,37−0,57, p < 0,001) setzte sich auch beim Gesamtüberleben fort. Mit Osimertinib wurde ein OS von 38,6 Monaten, mit der Standardbehandlung von 31,8 Monaten erzielt (HR 0,80, 95-%-KI: 0,64-0,99; p = 0,0462). Die Subgruppenanalyse zeigte zwar konsistent Vorteile für Osimertinib, im Hinblick auf die spezifische Mutation aber nur für Exon-19-Deletionen (HR 0,68, 95-%-KI: 0,51−0,90), nicht jedoch für die L858R-Punktmutation (HR 1,0, 95-%-KI: 0,71−1,40). Weiterhin profitierten insbesondere nichtasiatische Patienten von der Substanz (HR 0,54, 95-%-KI: 0,38−0,77 vs. HR 1,0, 95-%-KI: 0,75−1,32). Nach einer medianen Nachbeobachtung von 36 Monaten war die Rate der noch unter Therapie stehenden Patienten mit Osimertinib deutlich höher (28 vs. 9%), was sich analog zu den bereits publizierten PFS-Daten auch in einer deutlich längeren Zeit bis zur Zweitlinienbehandlung übersetzte (25,5 vs. 13,7 Monate, HR 0,48, 95-%-KI: 0,39−0,58, p < 0,0001). Bei zu Studienbeginn nicht möglichem Cross-over ermöglichte ein Amendment im Verlauf den Wechsel von Standard zu Osimertinib. Zum Zeitpunkt der aktuellen Auswertung (25.06.2019) waren 95% der Patienten unter der Standardtherapie progredient, 65% erhielten eine Zweitlinientherapie, davon 47% Osimertinib (Abb. 03). Auch nach einem längeren Follow-up (36 Monate) zeigte sich ein für Osimertinib günstiges Sicherheitsprofil mit 18 versus 29% bei Grad-3/4-Therapie-assoziierten Nebenwirkungen.
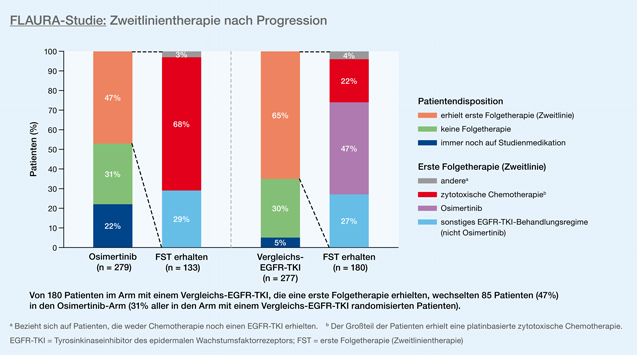 Abb. 3: Zweitlinientherapie nach Progression bei Patienten mit NSCLC unter Osimertinib und einer Standardbehandlung mittels Vergleichs-EGFR-TKI (Gefitinib oder Erlotinib) in der FLAURA-Studie (modifiziert nach [19]).
Abb. 3: Zweitlinientherapie nach Progression bei Patienten mit NSCLC unter Osimertinib und einer Standardbehandlung mittels Vergleichs-EGFR-TKI (Gefitinib oder Erlotinib) in der FLAURA-Studie (modifiziert nach [19]).Was die klinische Einordnung dieser Studienergebnisse möglicherweise einschränkt, ist die Tatsache, dass in beiden Therapiearmen 1/3 der Patienten keinerlei Zweitlinienbehandlung erhielt. Das schmälert zwar nicht die dargelegte Überlegenheit von Osimertinib verglichen mit den Erstgenerations-TKIs, kann jedoch die Frage nach einer sinnvollen Therapiesequenz nicht ausreichend beantworten.
ALK-positives NSCLC: Update zur ALEX-Studie
In die ALEX-Studie wurden 303 Patienten mit ALK-positivem, nicht vorbehandeltem metastasiertem NSCLC eingeschlossen [21]. Der primäre Endpunkt PFS war unter Alectinib deutlich verlängert [22] [23]. Aktuell wurden nach einem medianen Follow-up von 37,8 Monaten bei mit Alectinib behandelten Patienten beziehungsweise 23,0 Monaten in der Crizotinib-Gruppe nun das finale PFS und ein Update des OS präsentiert. Für das PFS zeigte sich ein unveränderter Vorteil für eine Erstlinienbehandlung mit Alectinib (34,8 vs. 10,9 Monate, HR 0,43, 95-%-KI: 0,32−0,58, p < 0,0001), der in der Gruppe der Patienten mit ZNS-Metastasen nochmals verbessert war (HR 0,37, 95-%-KI: 0,23−0,58). Nach 4 Jahren Nachbeobachtung waren noch 43,7% der Alectinib-Patienten ohne Progress. Die OS-Daten sind weiterhin bei lediglich 32% der Ereignisse nicht reif genug, hier zeigt sich eine vorläufige HR von 0,69 zugunsten von Alectinib (95-%-KI: 0,47−1,02).
Eine weitere Studie zum ALK-positiven NSCLC untersuchte die Effektivität von Lorlatinib bei zielgerichtet vorbehandelten Patienten. Dafür wurden 139 mit mindestens einem ALK-TKI (1−3, davon mindestens 1 TKI der 2. Generation) vorbehandelte Patienten ausgewertet [24]. 67,6% der Patienten wiesen Hirnmetastasen auf. Die Gesamtansprechrate lag bei 43,0%, das PFS zwischen 5,5 und 7,4 Monaten. ORR wie PFS waren weitgehend unabhängig von der Anzahl der ALK-Vortherapien. Konsistent mit der bekannten sehr guten intrakraniellen Wirksamkeit von Lorlatinib zeigte sich eine intrakranielle ORR von 54,4% versus 37,4% extrakraniell.
Fazit
- FLAURA-Studie: Der bereits bekannte Überlebensvorteil von Osimertinib verglichen mit Erstgenerations-EGFR-TKIs (Erlotinib und Gefitinib) im PFS zeigte sich nun auch im Gesamtüberleben (HR 0,80; p = 0,05), wobei Patienten mit L858R-Punktmutation und Asiaten jedoch keinen zusätzlichen Nutzen hatten (HR jeweils 1,0). Das Nebenwirkungsspektrum von Osimertinib ist weiterhin als sehr günstig einzuschätzen.
- ALEX-Studie: Das Studienupdate zeigt einen konsistenten Vorteil für mit Alectinib behandelte Patienten gegenüber der Standardtherapie mit Crizotinib (34,8 vs. 10,9 Monate, HR 0,43). Insbesondere die intrakranielle Aktivität ist bemerkenswert (HR 0,37). Die OS-Daten sind weiterhin nicht reif.
- Die Effizienz von Lorlatinib bei zum Teil mit mehreren ALK-TKIs vorbehandelten Patienten zeigte sich unabhängig von der Anzahl der Vortherapien. Auch diese Substanz weist eine ausgesprochen hohe intrakranielle Wirksamkeit auf.
“Patienten mit Treibermutationen (EGFR, ALK) können mittlerweile langjährig hocheffektiv behandelt werden. Insbesondere die unter den Erstgenerations-TKIs kritische Achillesferse der intrakraniellen Progression ist mit den Nachfolgesubstanzen (Osimertinib, Alectinib, Lorlatinib) deutlich besser abgesichert. Dazu gesellt sich ein verglichen mit den älteren Substanzen eher als günstig einzuschätzendes Sicherheitsprofil.“ Dr. med. Nikolaj Frost
Pleuramesotheliom
Ob eine vorgezogene Zweitlinientherapie (Switch-Maintenance) mit Gemcitabin nach einer Standarderstlinienbehandlung mit Platin/Pemetrexed einen Überlebensvorteil ergibt, untersuchte die Phase-II-Studie NVALT19 aus den Niederlanden [25]. 130 Patienten wurden 1 : 1 randomisiert in eine Gemcitabin-Erhaltung versus die beste Begleitbehandlung (Best supportive care [BSC]) verteilt. Der primäre Endpunkt einer Verlängerung des PFS wurde unter Gemcitabinerhaltung erreicht (5,3 vs. 2,8 Monate, HR 0,43, 95-%-KI: 0,29−0,64; p < 0,0001).
In der internationalen multizentrischen Phase-III-PROMISE-meso-Studie wurden 144 unter Platin-Pemetrexed progrediente Patienten randomisiert auf eine Behandlung mit Pembrolizumab versus eine Monochemotherapie mit Gemcitabin oder Vinorelbin verteilt [26]. Der primäre Endpunkt war das PFS. Das mediane Follow-up betrug 11,8 Monate. Beide Studienarme ergaben gleichwertige Ergebnisse im Hinblick auf das PFS mit einem numerischen Vorteil für die Chemotherapie (Pembrolizumab 2,5 Monate, Chemotherapie 3,4 Monate, HR 1,06). Die Subgruppenanalyse ergab bei Patienten mit nichtepitheloidem Mesotheliom ein deutlich schlechteres Abschneiden unter Pembrolizumab (HR 1,76) bei allerdings recht geringer Fallzahl (n = 16). Ansonsten konnten keine Signale detektiert werden. Das Gesamtüberleben war ebenfalls nicht wesentlich unterschiedlich (10,7 vs. 11,7 Monate, HR 1,04). Auch hier zeigte sich ein tendenziell schlechteres Abschneiden bei nichtepitheloider Histologie (HR 1,34). PD-L1 konnte in der Studie nicht als prädiktiver Biomarker identifiziert werden.
Das Update der IFCT-1501-MAPS-2-Studie mit Nivolumab oder Nivolumab/Ipilimumab beim vorbehandelten Pleuramesotheliom zeigte die 2-Jahresüberlebensdaten und eine explorative Analyse von Patienten mit Hyperprogression (HPD) [27]. Das 2-Jahres-OS lag mit Nivolumab bei 11,9, mit der Kombination bei 15,9 Monaten. Aufgrund der anatomischen Besonderheiten des Mesothelioms ist eine Volumetrie schwieriger als beim Lungenkarzinom. Von 114 eingeschlossenen Patienten wiesen dennoch 6 Studienteilnehmer Zeichen einer Hyperprogression auf. Damit konnte das Auftreten einer HPD erstmals auch beim Mesotheliom nachgewiesen werden, wenngleich die Rate insgesamt niedriger liegen dürfte als beim NSCLC.
Fazit
- Eine Switch-Maintenance mit Gemcitabin verlängert das PFS verglichen mit BSC deutlich (HR 0,43). Um diese Ergebnisse valide einschätzen zu können, sind jedoch OS-Daten notwendig.
- Der Stellenwert einer Immuntherapie beim Mesotheliom ist weiterhin nicht eindeutig belegt. Insbesondere fehlen randomisierte Studien mit einem Chemotherapie-Vergleichsarm. Eine Hyperprogression kommt unter einer Immuntherapie − wenngleich auch seltener als beim NSCLC − auch beim Mesotheliom vor.
“Das Pleuramesotheliom ist weiterhin ein Sorgenkind der Thoraxonkologie. Nach einer Standarderstlinientherapie mit Platin/Pemetrexed existiert keine validierte Zweitlinienbehandlung. Insbesondere mit einer Immuntherapie konnten bislang keine überzeugenden Ergebnisse aufgezeigt werden, allerdings sind noch Ergebnisse im Erstliniensetting (verglichen mit Platindoublette) zu erwarten.“ Dr. med. Nikolaj Frost
Quellen
- Peters S et al. Efficacy evaluation of concurrent nivolumab addition to a first-line, concurrent chemo-radiotherapy regimen in unresectable locally advanced NSCLC: Results from the European Thoracic Oncology Platform (ETOP 6-14) NICOLAS phase II trial. Presented at Poster Discussion - Non-metastatic NSCLC and other thoracic malignancies, ESMO Congress 2019, Barcelona, abstract 1457PD.
- Peters S et al. Safety evaluation of nivolumab added concurrently to radiotherapy in a standard first line chemo-radiotherapy regimen in stage III non-small cell lung cancer-The ETOP NICOLAS trial. Lung Cancer 2019; 133: 83–87.
- Zenke Y et al. Phase III study comparing second- and third-generation regimens with concurrent thoracic radiotherapy in patients with unresectable stage III non-small cell lung cancer: 10-year follow-up of West Japan thoracic oncology group WJTOG0105. Poster Discussion - Non-metastatic NSCLC and other thoracic malignancies, ESMO Congress 2019, Barcelona, abstract 1458PD.
- Antonia SJ et al. Overall Survival with Durvalumab after Chemoradiotherapy in Stage III NSCLC. N Engl J Med 2018; 379: 2342–2350.
- Vansteenkiste JF et al. Efficacy of durvalumab in patients with stage III NSCLC who experience pneumonitis (PACIFIC). Presented at Poster Discussion - Non-metastatic NSCLC and other thoracic malignancies, ESMO Congress 2019, Barcelona, abstract 1459PD.
- Spigel D et al. IMpower110: Interim overall survival (OS) analysis of a phase III study of atezolizumab (atezo) vs platinum-based chemotherapy (chemo) as first-line (1L) treatment (tx) in PD-L1–selected NSCLC. Presented at Proffered Paper 1 - NSCLC, metastatic, ESMO Congress 2019, Barcelona, abstract LBA78.
- Peters S et al. Nivolumab (NIVO) + low-dose ipilimumab (IPI) vs platinum-doublet chemotherapy (chemo) as first-line (1L) treatment (tx) for advanced non-small cell lung cancer (NSCLC): CheckMate 227 part 1 final analysis. Presented at Presidential Symposium 1, ESMO 2019, Barcelona, abstract LBA4_PR.
- Hellmann MD et al. Nivolumab plus Ipilimumab in Lung Cancer with a High Tumor Mutational Burden. N Engl J Med 2018; 378: 2093–2104.
- Paz-Ares L et al. Pembrolizumab (pembro) + chemotherapy (chemo) in metastatic squamous NSCLC: Final analysis and progression after the next line of therapy (PFS2) in KEYNOTE-407. Presented at Poster Discussion – NSCLC, metastatic, ESMO 2019, Barcelona, abstract LBA82.
- Paz-Ares L et al. Pembrolizumab plus Chemotherapy for Squamous Non-Small-Cell Lung Cancer. N Engl J Med 2018; 379: 2040–2051.
- Socinski M et al. Final efficacy results from B-F1RST, a prospective phase II trial evaluating blood-based tumour mutational burden (bTMB) as a predictive biomarker for atezolizumab (atezo) in 1L non-small cell lung cancer (NSCLC). Presented at Poster Discussion – NSCLC, metastatic, ESMO 2019, Barcelona,abstract LBA83.
- Herbst RS et al. Association between tissue TMB (tTMB) and clinical outcomes with pembrolizumab monotherapy (pembro) in PD-L1-positive advanced NSCLC in the KEYNOTE-010 and -042 trials. Presented at Proffered Paper 1 - NSCLC, metastatic, ESMO Congress 2019, Barcelona, abstract LBA79.
- Paz-Ares L et al. Pembrolizumab (pembro) plus platinum-based chemotherapy (chemo) for metastatic NSCLC: Tissue TMB (tTMB) and outcomes in KEYNOTE-021, 189, and 407. Presented at Proffered Paper 1 - NSCLC, metastatic, ESMO Congress 2019, Barcelona, abstract LBA80.
- Sperduto PW et al. Summary report on the graded prognostic assessment: an accurate and facile diagnosis-specific tool to estimate survival for patients with brain metastases. J Clin Oncol 2012; 30: 419-425.
- Chow LQ et al. Results of the ASCEND-7 phase II study evaluating ALK inhibitor (ALKi) ceritinib in patients (pts) with ALK+ non-small cell lung cancer (NSCLC) metastatic to the brain. Presented at Proffered Paper 1 - NSCLC, metastatic, ESMO 2019, Barcelona, abstract 1478O.
- Fan Y et al. Integrated genomic and DNA methylation analyses of non-small cell lung cancer patients with brain metastases. Proffered Paper 1 - NSCLC, metastatic , ESMO 2019, Barcelona, abstract 14790.
- Mansfield AS et al. Outcomes with pembrolizumab (pembro) monotherapy in patients (pts) with PD-L1–positive NSCLC with brain metastases: Pooled analysis of KEYNOTE-001, -010, -024, and -042. Presented at Proffered Paper 1 - NSCLC, metastatic, ESMO Congress 2019, Barcelona, abstract 1482O.
- Powell SF et al. Pembrolizumab (pembro) plus platinum-based chemotherapy (chemo) in NSCLC with brain metastases: Pooled analysis of KEYNOTE-021, 189, and 407. Presented at Poster Discussion – NSCLC, metastatic, ESMO 2019, Barcelona, abstract 1483PD.
- Ramalingam SS et al. Osimertinib vs comparator EGFR-TKI as first-line treatment for EGFRm advanced NSCLC (FLAURA): Final overall survival analysis. Presidential Symposium, ESMO 2019, Barcelona, abstract LBA5_PR.
- Soria JC et al. Osimertinib in Untreated EGFR-Mutated Advanced Non-Small-Cell Lung Cancer. N Engl J Med 2018; 378: 113–125.
- Mok TSK et al. Final PFS, updated OS and safety data from the randomised, phase III ALEX study of alectinib (ALC) versus crizotinib (CRZ) in untreated advanced ALK+ NSCLC. Poster Discussion – NSCLC, metastatic, ESMO 2019, Barcelona, abstract 1484PD.
- Peters S et al. Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med 2017; 377: 829–838.
- Camidge DR et al. Updated Efficacy and Safety Data and Impact of the EML4-ALK Fusion Variant on the Efficacy of Alectinib in Untreated ALK-Positive Advanced Non-Small Cell Lung Cancer in the Global Phase III ALEX Study. J Thorac Oncol; 14: 1233–1243.
- Camidge DR et al. Intracranial and extracranial efficacy of lorlatinib in the post second-generation ALK tyrosine kinase inhibitor (TKI) setting. Presented at Poster Discussion – NSCLC, metastatic, ESMO 2019, Barcelona, abstract 1487PD.
- Burgers SA et al. Switch maintenance gemcitabine after first-line chemotherapy in patients with malignant mesothelioma: A multicenter open label phase II trial (NVALT19). Presented at Poster Discussion - Non-metastatic NSCLC and other thoracic malignancies, ESMO 2019; Barcelona, abstract LBA92.
- Popat S et al. A multicentre randomized phase III trial comparing pembrolizumab (P) vs single agent chemotherapy (CT) for advanced pre-treated malignant pleural mesothelioma (MPM): Results from the European Thoracic Oncology Platform (ETOP 9-15) PROMISE-meso trial. Presented at Proffered Paper 2 – Non-metastatic NSCLC and other thoracic malignancies (mesothelioma and thymic carcinoma), ESMO 2019, Barcelona, abstract LBA91_PR.
- Zalcman G et al. Second/third-line nivolumab vs nivo plus ipilimumab in malignant pleural mesothelioma: Long-term results of IFCT-1501 MAPS2 phase IIR trial with a focus on hyperprogression (HPD). abstract 1841O.
- Bildnachweis: „Nativity facade of Sagrada Familia cathedral in Barcelona”: © valeryegorov/Adobe