EHA 2015
11. bis 14. Juni, Wien
Lymphome – brauchen wir noch die Chemotherapie?
 Vom 11. bis 14. Juni 2015 fand in Wien die diesjährige Jahrestagung der European Hematology Association (EHA) statt. Lesen Sie hier die neuesten Informationen zu wichtigen Studien vom EHA-Kongress.
Vom 11. bis 14. Juni 2015 fand in Wien die diesjährige Jahrestagung der European Hematology Association (EHA) statt. Lesen Sie hier die neuesten Informationen zu wichtigen Studien vom EHA-Kongress.
Themenschwerpunkte dieses EHA-Berichtes sind das multiple Myelom, das myelodysplastische Syndrom (MDS) und die akute myeloische Leukämie (AML) sowie Lymphome.
Für uns waren Herr Dr. med. Christian Jakob aus Potsdam, Frau Dr. med. Catharina Müller-Thomas aus München sowie Herr Prof. Dr. med. Kai Hübel aus Köln vor Ort.
Liebe Kolleginnen und Kollegen,
der Kongress der European Hematology Association (EHA) fand vom 11. bis 14. Juni in Wien statt. In diesem Jahr stand er ganz im Zeichen seines 20-jährigen Jubiläums. Dementsprechend gab es neben den wissenschaftlichen Veranstaltungen auch viele Festakte, bei denen dieses Ereignis gebührend gefeiert wurde.
Die zunehmende Bedeutung der präklinischen Erkenntnisse spiegelte sich im umfangreichen Tagungsprogramm wider. Die erfolgreiche Übertragung dieser Erkenntnisse aus der Grundlagenforschung in die klinische Realität ermöglichte in den letzten Jahren eine Vielzahl an neuen Therapiemöglichkeiten für die Behandlung von hämatoonkologischen Erkrankungen. Mit 2.200 eingereichten Abstracts, von denen 262 als besondere Höhepunkte in insgesamt 37 Oral Sessions vorgestellt wurden, gab es wieder eine fast unüberschaubare Vielzahl an neuen wissenschaftlichen Publikationen.
Wir haben für Sie die unserer Meinung nach wichtigsten Veranstaltungen und Posterpräsentationen zu den drei Schwerpunktindikationen "Multiples Myelom", "Myelodysplastische Syndrome/akute myeloische Leukämie" und "Lymphome" besucht und die dort vorgestellten Forschungsergebnisse in diesem Kongressbericht zusammengefasst. Dabei war uns besonders wichtig, dass wir diese neuen Erkenntnisse auch im Hinblick auf die Situation im deutschen Praxisalltag bewerten und einordnen, um Ihnen die klinische Arbeit am Patienten zu erleichtern.
Wir wünschen Ihnen viel Spaß bei der Lektüre dieses Berichtes und hoffen, dass wir Sie in Kürze wieder einmal auf hematooncology.com antreffen.
Mit kollegialen Grüßen
 Dr. med. Christian Jakob, Klinikum Ernst von Bergmann, Potsdam
Dr. med. Christian Jakob, Klinikum Ernst von Bergmann, Potsdam Dr. med. Catharina Müller-Thomas, Klinikum rechts der Isar, München
Dr. med. Catharina Müller-Thomas, Klinikum rechts der Isar, München Prof. Dr. med. Kai Hübel, Klinik I für Innere Medizin, Universitätsklinikum Köln
Prof. Dr. med. Kai Hübel, Klinik I für Innere Medizin, Universitätsklinikum KölnMultiples Myelom – Einzug der neuen Substanzen der nächsten Generation in die Klinik steht unmittelbar bevor
Dr. med. Christian Jakob, Klinikum Ernst von Bergmann, Potsdam

Der 20. Kongress der European Hematology Association (EHA), der vom 11. bis 14. Juni 2015 in Wien stattfand, stand – wie schon die internationalen Kongresse der letzten Jahre – im Zeichen der zielgerichteten, molekularen und immunologischen Therapieansätze, die nun nicht mehr nur an der Schwelle zur klinischen Anwendung stehen, sondern sich anschicken, die klassischen Zytostatika mehr und mehr zu ersetzen. Mit dem multiplen Myelom beschäftigten sich 98 der 733 vor Ort präsentierten Beiträge. Es war damit erneut eines der herausragenden Themen des Kongresses. Im Mittelpunkt standen die neuen Substanzen der nächsten Generation – oder auch „post novel agents“. Die aktuell klinisch relevanten Vertreter, deren Zulassung auch in Europa unmittelbar bevorsteht, sind der Proteasominhibitor (PI) der zweiten Generation Carfilzomib, der Histondeacetylasehemmer (HDACi) Panobinostat sowie die monoklonalen Antikörper (mAbs) Elotuzumab und Daratumumab. Nachdem die Daten aus den abgeschlossenen Phase-I/II- beziehungsweise Phase-III-Studien zum Einsatz beim rezidivierten und refraktären multiplen Myelom (rrMM) bereits in den letzten Monaten vorgestellt und zum Teil publiziert wurden, wurden beim EHA-Kongress noch einmal Update- und Subgruppenanalysen präsentiert und der aktuelle und zukünftige Stellenwert der neuen Therapieansätze im Zusammenhang mit den verfügbaren Optionen und unter den Gegebenheiten in den europäischen Ländern diskutiert.
Proteasominhibitor der zweiten Generation – Carfilzomib
Aus der Phase-III-Studie zur Wirksamkeit des Zweitgenerations-PI Carfilzomib in Kombination mit Lenalidomid und Dexamethason (KRd) beim rrMM (ASPIRE-Studie) [1] wurde eine Subgruppenanalyse präsentiert, in der die Effektivitätsdaten in Abhängigkeit von der Zahl der Vortherapien ausgewertet wurden [2]. Es zeigte sich kein Unterschied in den Gesamtansprechraten (ORR) auf KRd bei Patienten mit 1 versus >= 2 Vortherapien (ORR: 87,0 % versus 87,3 %), bei einer allerdings höheren Rate an stringenten kompletten Remissionen (sCR), kompletten Remissionen (CR) und sehr guten partiellen Remissionen (VGPR) (75,9 % versus 64,6 %) und einer Verlängerung des progressionsfreien Überlebens (PFS (12 Monate versus 9 Monate) für Patienten mit 1 versus >= 2 Vortherapien. Die Toxizitäten <= Grad 3, insbesondere kardiovaskuläre Ereignisse, waren in beiden Gruppen vergleichbar.
Eine weitere Studie zum Einsatz von Carfilzomib (ENDEAVOR-Studie) ebenfalls beim rrMM wurde in der „Late-Breaking Abstracts Session“ präsentiert [3]. In der randomisierten Phase-III-Studie wurde der Einsatz von Carfilzomib in Kombination mit Dexamethason versus Bortezomib + Dexamethason, also der Ersatz des PI der ersten Generation gegen einen neuen PI der zweiten Generation, geprüft. Für Bortezomib war eine subkutane Applikation erlaubt. Es zeigten sich deutlich höhere Ansprechraten (ORR: 77 % versus 63 %, >= VGPR: 54 % versus 29 %) und ein signifikant verlängertes PFS (18,7 Monate versus 9,4 Monate) für die Kombination mit Carfilzomib. Klinisch relevant ist die Tatsache, dass sich eine nahezu gleiche Effektivität in Bezug auf das PFS sowohl bei Bortezomib-vorbehandelten wie auch bei Bortezomib-naiven Patienten zeigte. Ebenfalls sehr bemerkenswert ist die deutliche Reduktion der Polyneuropathierate (>= Grad 2), mit 6 % im Carfilzomib- versus 32 % im Bortezomib-Arm. An relevanten Grad-3/4-Toxizitäten im Carfilzomib-Arm sind auch hier kardiovaskuläre Ereignisse wie Hypertonie, Dyspnoe und Herzinsuffizienz zu nennen. Die Abbruchrate aufgrund von unerwünschten Ereignissen (AEs) war in beiden Armen gleich (14 % versus 16 %).
Fazit
Carfilzomib ist der in der klinischen Entwicklung am weitesten fortgeschrittene PI der neueren Generation und hält bereits Einzug in die Erstlinientherapie. Erste Daten aus verschiedenen Phase-II- und Phase-III-Studien zum Einsatz von Carfilzomib in der Erstlinie in Kombination mit Lenalidomid + Dexamethason (KRd) oder mit Cyclophosphamid + Dexamethason (KCd) oder auch in der Vierfachkombination mit Thalidomid + Cyclophosphamid + Dexamethason (KCTD) liegen bereits vor und zeigen Ansprechraten von bis zu 95 %. Daten zu einer weiteren Viererkombination mit Carfilzomib, Cyclophosphamid, Lenalidomid und Dexamethason (KCRD) wurden ebenfalls bei der EHA-Tagung präsentiert [4].
Carfilzomib wird aller Voraussicht nach Bortezomib in den frühen Therapielinien ersetzen und eröffnet die Option, die oft therapielimitierende Neurotoxizität weitgehend eliminieren zu können. Carfilzomib ist bereits von der amerikanischen Gesundheitsbehörde FDA zugelassen und hat von der Europäischen Arzneimittel-Agentur (EMA) den „orphan drug“-Status erhalten. Die Zulassung wird für Ende 2015/Anfang 2016 erwartet.
„Carfilzomib ist derzeit sowohl hinsichtlich der Effektivität als auch im Hinblick auf die Toxizität als „best in class”-Proteasominhibitor anzusehen.“ Dr. Christian Jakob
HDAC-Inhibition – Panobinostat
Aus der Phase-III-PANORAMA-Studie [5] zum Einsatz des HDAC-Inhibitors Panobinostat (PAN) in Kombination mit Bortezomib (BTZ) + Dexamethason beim rrMM wurde ebenfalls eine Subgruppenanalyse nach Art der Vortherapien präsentiert [6]. Hier wurden die Effektivitätsdaten in den Subgruppen von Patienten ausgewertet, die zuvor eine Therapie mit einem IMiD, mit Bortezomib und einem IMiD oder mit >= 2 Vortherapien unter Einschluss von Bortezomib und einem IMiD erhalten hatten. Es zeigte sich bei insgesamt etwas geringeren Gesamtansprechraten und kürzerem PFS mit zunehmender Zahl an Vortherapien eine konsistente Verbesserung des PFS von circa fünf Monaten zugunsten der Therapie mit Panobinostat gegenüber der alleinigen Therapie mit BTZ + Dexamethason über alle Subgruppen hinweg. Bemerkenswert auch die CR/nCR-Rate von circa 22 % bei mit BTZ + IMiD vorbehandelten Patienten (Tab. 1). Zu erwähnen sind allerdings auch die Raten an Grad-3/4-Diarrhoen (26 %) und Fatigue (25 %) im Panobinostat-Arm.
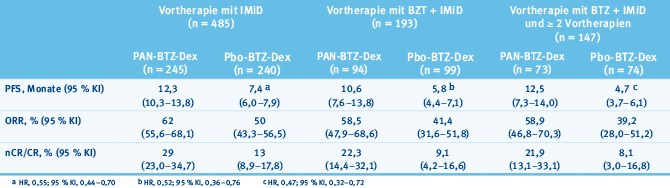 Tab. 1: PANORAMA-Studie, Panobinostat (PAN) + Bortezomib (BTZ) + Dexamethason (Dex) versus BTZ + Dex. Ansprechen und PFS unter PAN + BTZ in Abhängigkeit von der Vortherapie (modifiziert nach Einsele H et al. Haematologica 2015;100(s1),1[6]).
Tab. 1: PANORAMA-Studie, Panobinostat (PAN) + Bortezomib (BTZ) + Dexamethason (Dex) versus BTZ + Dex. Ansprechen und PFS unter PAN + BTZ in Abhängigkeit von der Vortherapie (modifiziert nach Einsele H et al. Haematologica 2015;100(s1),1[6]).Die Daten zeigen die Wirksamkeit von Panobinostat in den in der klinischen Realität relevanten Subgruppen und bestätigen die bereits frühzeitig generierte Hypothese von einer synergistischen Aktivität beziehungsweise einer Resistenzüberwindung bei der Kombination eines PI mit einem HDAC-Inhibitor (HDACi). Dies bestätigt auch eine aktuell publizierte Phase-I/II-Studie zur Kombination von Panobinostat mit Carfilzomib [7]. Panobinostat ist bereits von der FDA zugelassen und hat von der EMA den „orphan drug“-Status erhalten.
Monoklonale Antikörper nun auch in der Therapie des multiplen Myeloms
Die erste Phase-III-Studie zu einer Antikörpertherapie beim multiplen Myelom, die ELOQUENT-2-Studie, wurde in der Plenarsitzung vorgestellt [8]. In der Studie wurde die Behandlung mit Lenalidomid und Dexamethason (Ld) +/- dem Anti-CS1-Antikörper Elotuzumab beim rrMM mit einer bis drei Vortherapien untersucht. Es zeigte sich ein signifikant verbessertes Ansprechen für die Elotuzumab-Kombination (ELd) (ORR: 79 % versus 66 %, p = 0,0002) und eine deutliche Verlängerung des PFS (median 19,4 Monate versus 14,9 Monate) (Abb. 1). Bemerkenswert ist, dass sich die Verlängerung des PFS auch bei den zytogenetischen Hochrisikogruppen zeigt (Del.17p: 21,1 Monate versus 14,3 Monate; t4;14: 15,5 Monate versus 5,6 Monate). Die PFS-Kurve für die Elotuzumab-Kombination zeigt nach 30 Monaten ein gewisses Plateau, sodass man auf einen Anteil von circa 25 % der Patienten mit einer längerfristigeren Remission hoffen darf. Die Daten wurden erst vor wenigen Tagen, kurz nach ihrer Präsentation beim ASCO-Kongress, als elektronische Publikation im New England Journal of Medicine freigeschaltet [9].
Ebenfalls vielversprechend erscheint die Kombination von Elotuzumab mit Bortezomib + Dexamethason (VD). Hierzu wurden Daten einer randomisierten Phase-II-Studie ebenfalls beim rrMM vorgestellt [10]. Sie zeigten eine Verlängerung des PFS nach zwei Jahren von 24 % für die Elotuzumab-Kombination versus 6 % für VD allein.
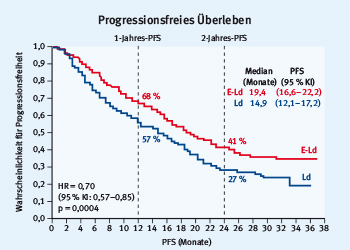 Abb. 1: ELOQUENT-2-Studie: Progressionsfreies Überleben (PFS) unter Elotuzumab + Lenalidomid + Dexamethason (E-Ld) versus Placebo + Lenalidomid + Dexamethason (Ld) (modifiziert nach Dimopoulos M et al. Presented at Presidential Symposium, EHA 2015, Vienna, abstract S471 [8]).
Abb. 1: ELOQUENT-2-Studie: Progressionsfreies Überleben (PFS) unter Elotuzumab + Lenalidomid + Dexamethason (E-Ld) versus Placebo + Lenalidomid + Dexamethason (Ld) (modifiziert nach Dimopoulos M et al. Presented at Presidential Symposium, EHA 2015, Vienna, abstract S471 [8]).Ein weiterer Höhepunkt war die Präsentation der Daten aus einer Phase-I/II-Studie (SIRIUS) zum Einsatz des monoklonalen Anti-CD38-Antiköpers Daratumumab beim rrMM [11]. Hier wurden Patienten mit mindestens drei Vortherapien eingeschlossen. Die Behandlung erfolgte mit Daratumumab als Monotherapie in einer Dosiseskalation von 8 auf 16mg/kg. Es zeigte sich bei den intensiv vorbehandelten Patienten (median fünf Vortherapien) eine ORR von 29 % mit einer Rate an sCR von 3 % und einem VGPR von 9 %. Das Ansprechen war konsistent über alle klinisch relevanten Subgruppen (Abb. 2). Wesentliche Nebenwirkungen der Antikörpergabe waren infusionsbedingte Reaktionen, die jedoch zu 90 % während der ersten beiden Gaben und ab den Folgegaben nur noch sporadisch auftraten.
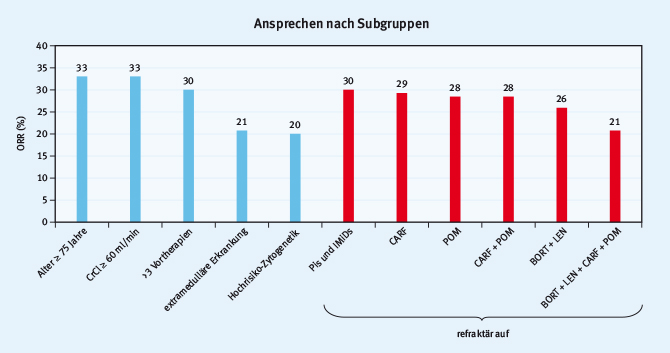 Abb. 2: SIRIUS-Studie, Daratumumab-Monotherapie bei rrMM. Ansprechen nach Subgruppen. Presented at Oral Presentation: Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S430 [11]).
Abb. 2: SIRIUS-Studie, Daratumumab-Monotherapie bei rrMM. Ansprechen nach Subgruppen. Presented at Oral Presentation: Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S430 [11]).Interessant erscheint auch der zweite monoklonale Anti-CD38-Antikörper MOR202. Hierzu wurden Daten aus einer Phase-I/IIa-Studie präsentiert [12]. Vorläufige Effektivitätsdaten zeigen eine Aktivität in der Dosiskohorte 8 mg in Kombination mit Dexamethason. In einer Posterpräsentation konnte darüber hinaus gezeigt werden, dass IMiDs eine verstärkte Expression von CD38 in Myelomzelllinien induzieren und den zytotoxischen Effekt von MOR202 in vitro steigern [13], sodass sich hieraus eine Rationale für die Kombination von CD38-Antikörpern mit IMiD-basierten Therapien ableiten lässt.
Fazit
Die neuen Substanzen der nächsten Generation stellen erneut einen Meilenstein in der Therapie des multiplen Myeloms dar. Mit den monoklonalen Antikörpern gegen CS1 und CD38 stehen neuartige Therapieansätze zur Verfügung, die sich aufgrund ihres andersartigen, zum Teil synergistischen Wirkmechanismus besonders gut für eine Kombinationstherapie sowohl mit PIs und IMiDs als auch mit klassischen Zytostatika eignen. In Anlehnung an die Lymphomtherapie kann man schon von einer Art R-CHOP für das multiple Myelom sprechen.
Daratumumab und Elotuzumab haben den „breakthrough therapy designation“-Status bei der FDA und befinden sich im beschleunigten Zulassungsverfahren. Eine Zulassung wird für 2016 erwartet.
„Um die neuen Therapieoptionen und Wirkprinzipien in optimaler Sequenz einsetzen zu können, sollte der Therapiealgorithmus in Zukunft von Anfang an eine Strategie für das mögliche Vorgehen im 1. und 2. Rezidiv mit einbeziehen.” Dr. Pieter Sonneveld
Neuer Therapieansatz mit dem monoklonalen Antikörper NEOD001 bei der AL-Amyloidose
Für viel Aufmerksamkeit sorgte die Präsentation zum Einsatz des neuen monoklonalen Antikörpers NEOD001 bei der AL-Amyloidose [14]. Der Antikörper ist gegen „fehlgefaltete“ Proteine gerichtet und offensichtlich in der Lage, ein Abräumen auch nicht löslicher, im Organgewebe abgelagerter Proteinkomplexe durch Makrophagen zu vermitteln. Das genaue Epitop ist allerdings bisher nicht in den Veröffentlichungen beschrieben. Es wurden Daten aus einer Phase-I/II-Studie bei 27 Patienten mit AL-Amyloidose, die mit mindestens einer Therapie vorbehandelt waren und einen persistierenden Organbefall (66 % >= 2 Organe befallen) hatten, präsentiert. Die Patienten wurden mit monatlichen Antikörpergaben in der finalen Dosiskohorte mit 27 mg/m² behandelt. Es zeigte sich eine Rate von 50 % kardialem (> 30 % Reduktion des Pro-BNP) und 43 % renalem Ansprechen (30 % Verbesserung der glomerulären Filtrationsrate (GFR) oder 30 % Rückgang der Proteinurie). Bemerkenswert ist auch, dass die Remissionen über Monate anhaltend waren und sich mit zunehmender Therapiedauer noch vertieften. Es traten keine relevanten antikörperassoziierten Toxizitäten und keine toxizitätsbedingten Therapieabbrüche auf.
Fazit
Die Daten zu NEOD001 sind außerordentlich vielversprechend und kündigen einen echten Durchbruch an. Damit würde bei der bisher sehr schwer therapierbaren Patientengruppe mit Organbefall erstmals eine gezielte Therapieoption zur Verfügung stehen, die gegen die Amyloidablagerungen im Gewebe gerichtet ist. NEOD001 wurde von der FDA der „fast track designation“-Status erteilt.
Neues zu den etablierten Substanzen
Neben den vielen neuen Substanzen gab es auf dem EHA-Kongress auch noch ein paar interessante Aspekte zu den bereits etablierten Therapien.
So wurden noch einmal eine Update- und zwei Subgruppenanalysen zur der bereits im letzten Jahr publizierten FIRST-Studie [15] zum Einsatz von Lenalidomid + Dexamethason (Ld) in der Primärtherapie bei Patienten, die nicht für eine Stammzelltransplantation geeignet sind, vorgestellt [16]. In der Studie wurde eine Therapie mit Rd bis zur Progression (Rd) versus Rd über 18 Monate (Rd18) versus Melphalan + Prednison + Thalidomid (MPT) verglichen. Der primäre Endpunkt der Studie war das PFS. Die Analyse zum Gesamtüberleben (OS) war von den Zulassungsbehörden gefordert worden. Nach einer medianen Nachbeobachtungszeit von 45,5 Monaten lag das OS bei 58,9 Monaten (Rd) versus 56,7 Monate (Rd18) versus 48,5 Monate (MPT). Für den Vergleich zwischen Rd und MPT ergab sich eine Risikoreduktion für das Ereignis OS um 25 %, während sich im Vergleich zwischen Rd und Rd18 keine signifikante Verlängerung des OS ergab.
Zur gleichen Studie wurden außerdem Subgruppenanalysen zur Effektivität bei Patienten <= 75 Jahre versus > 75 Jahre [17] und bei Patienten mit Nierenfunktionseinschränkungen präsentiert [18]. In der Subgruppenanalyse zum Einfluss des Alters zeigte sich ein Vorteil bezüglich des PFS für Rd versus MPT in beiden Altersgruppen =< 75 Jahre und > 75 Jahre. Die Risikoreduktion für das Ereignis Progression war jedoch deutlicher in der Altersgruppe =< 75 Jahre für Rd versus MPT (HR: 0,64 versus 0,80) und für Rd versus Rd18 (HR: 0,68 versus 0,78). Die Risikoreduktion für den sekundären Endpunkt OS war in beiden Altersgruppen zugunsten von Rd versus MPT (HR: 0,76 und 0,72), fiel für Rd versus Rd18 allerdings, wie in der oben genannten Update-Analyse der Gesamtpopulation gezeigt, gering aus (HR: 0,9 und 0,91).
In der Subgruppenanalyse zur Effektivität bei einer Nierenfunktionseinschränkung (NI) [18] zeigte sich, dass auch Patienten mit milder (GFR >= 50 und < 80ml/min) oder moderater (GFR >= 30 und < 50ml/min) NI von der Therapie mit Rd beziehungsweise Rd18 profitieren. In der Studie galten die bekannten Dosisreduktionsempfehlungen bei NI für Lenalidomid und für Melphalan. Es ergab sich eine Risikoreduktion für PFS gegenüber MPT von circa 30 % (HR: 0,66–0,76) für Rd und für Rd18 (HR: 0,66–0,82) für alle Subgruppen mit NI. Darüber hinaus war in 20 % (Rd) beziehungsweise 27 % (Rd18) ein komplettes renales Ansprechen zu verzeichnen.
Fazit
Die Update- und Subgruppenanalysen zur FIRST-Studie bestätigen die Effektivität und den Nutzen einer Therapie mit Rd in der Erstlinie auch bei ansonsten schwer zu behandelnden, jedoch in der klinischen Realität regelmäßig anzutreffenden Patientenkollektiven.
Auch aus der bereits lange publizierten Zulassungsstudie zur Rezidivtherapie mit Pomalidomid [19] wurde noch einmal ein interessanter Aspekt herausgearbeitet. In einer von Katja Weisel aus Tübingen präsentierten Post-hoc-Analyse aus der MM-003-Studie zur Rezidivtherapie mit Pomalidomid versus Dexamethason bei rrMM wurde der Frage nachgegangen, welche Bedeutung das Erreichen einer „nur“ stabilen Erkrankung (SD) für das OS unter Therapie mit Pomalidomid hat [20]. Es zeigte sich, dass Patienten, die zu den Zeitpunkten vor Zyklus 3, 5 oder 7 eine SD hatten, ein vergleichbares OS hatten wie Patienten, die mindestens eine partielle Remission (>= PR) erreicht hatten. Ein signifikanter Unterschied im OS bestand zwischen Patienten mit OR (>= PR) oder SD gegenüber Patienten mit progredienter Erkrankung (PD) zu allen Zeitpunkten (Abb. 3). Einige Patienten mit SD nach drei Zyklen erreichten im Verlauf von sieben Zyklen noch eine PR (12/73 Patienten von Zyklus #3 zu #5, 12/69 Patienten von #3 zu #7).
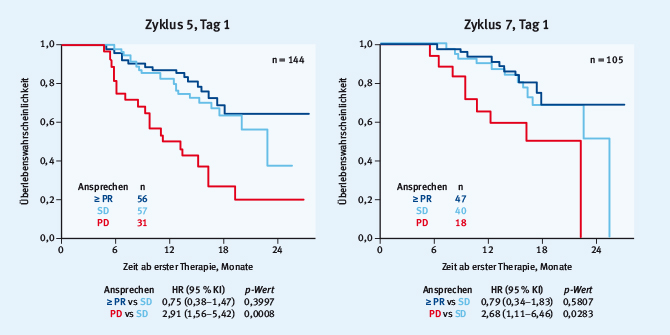 Abb. 3 MM-003-Studie, Pomalidomid versus Dexamethason. Gesamtüberleben in Abhängigkeit vom Ansprechen (≥ PR versus SD versus PD) zum Zeitpunkt Zyklus 5, Tag 1 und Zyklus 7, Tag 1 (modifiziert nach Moreau et al. Presented at Oral Presentation: Multiple myeloma: Clinical studies 3, EHA 2015, Vienna, abstract 788 [20]).
Abb. 3 MM-003-Studie, Pomalidomid versus Dexamethason. Gesamtüberleben in Abhängigkeit vom Ansprechen (≥ PR versus SD versus PD) zum Zeitpunkt Zyklus 5, Tag 1 und Zyklus 7, Tag 1 (modifiziert nach Moreau et al. Presented at Oral Presentation: Multiple myeloma: Clinical studies 3, EHA 2015, Vienna, abstract 788 [20]).Fazit
Der Befund, dass Patienten auch bei Nichterreichen einer möglichst tiefen Remission von einer Therapie mit Pomalidomid profitieren, scheint aus klinisch-praktischer Sicht sehr bedeutsam. Die Daten verdeutlichen noch einmal, dass das Erreichen einer CR oder MRD-Negativität lediglich ein Surrogatparameter ist, der jedoch insbesondere im Rezidiv oder bei älteren Patienten nicht das oberste Therapieziel definiert. Für den klinischen Alltag kann man hieraus schlussfolgern, die Therapie mit Pomalidomid nicht zu früh, das heißt vor Auftreten einer Progression, zu beenden.
Quellen
- Stewart AK et al. Carfilzomib, lenalidomide, and dexamethasone for relapsed multiple myeloma.N Engl J Med. 2015;372(2):142–152
- Dimopoulos M et al. Effect of carfilzomib, lenalidomide, and dexamethasone vs. lenalidomide and dexamethasone in patients with relapsed multiple myeloma by line of therapy: interim results from the phase 3 ASPIRE study. Presented at Oral Presentation, Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S427
- Dimopoulos M et al. Carfilzomib and dexamethasone improves progression-free survival and response rates vs. bortezomib and dexamethasone in patients (pts) with relapsed multiple myeloma (rMM): the phase 3 study ENDEAVOR. Presented at Late Breaking Abstracts 2, EHA 2015, Vienna, abstract LB2071
- Pawlyn C et al. The quadruplet combination of carfilzomib, cyclophosphamide, lenalidomide, and dexamethasone is safe and well tolerated as induction therapy for newly diagnosed, transplant eligible, myeloma patients. Presented at Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S428
- San Miguel JF et al. Panobinostat plus bortezomib and dexamethasone versus placebo plus bortezomib and dexamethasone in patients with relapsed or relapsed and refractory multiple myeloma: a multicentre, randomised, double-blind phase 3 trial. Lancet Oncol. 2014;15(11):1195–11206
- Einsele H et al. Subgroup analysis by prior treatment among patients with relapsed and refractory multiple myeloma in the PANORAMA 1 study of panobinostat or placebo plus bortezomib and dexamethasone. Haematologica 2015;100(s1),1, abstract S102
- Berdeja JG et al. Phase I/II study of the combination of panobinostat and carfilzomib in patients with relapsed/refractory multiple myeloma. Haematologica 2015;100(5):670–676
- Dimopoulos M et al. ELOQUENT-2: A phase 3, randomized, open-label study of lenalidomide/dexamethasone with or without elotuzumab in patients with relapsed/refactory multiple myeloma. Presented at Presidential Symposium, EHA 2015, Vienna, abstract S471
- Lonial et al. Elotuzumab Therapy for Relapsed or Refractory Multiple Myeloma. N Engl J Med. 2015. [Epub ahead of print].
- Jakubowiak A et al. A randomized, open-label, phase 2 study of bortezomib an dexamethasone with or without elotuzumab in patients with relapsed/refractory multiple myeloma. Presented at Oral Presentation: Multiple myeloma: Clinical studies 1, EHA 2015, Vienna, abstract S103
- Lonial S et al. Phase 2 study of daratumumab monotherapy in patients with ≥ 3 lines of prior therapy or double refactory multiple myeloma: 54767414MMY2002 (SIRIUS). Presented at Oral Presentation: Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S430
- Boxhammer R et al. Effect of IMiD compounds on CD38 expression on multiple myeloma cells: MOR202, a human CD38 antibody in combination with pomalidomide. Presented at Poster Presentation: Multiple myeloma - Biology 2, EHA 2015, Vienna, abstract P636
- Raab M et al. A phase I/II study of the human anti-CD38 antibody MOR202 (MORO3087) in relapsed or refractory multiple myeloma. Presented at Oral Presentation: Multiple myeloma: Clinical studies 3, EHA 2015, Vienna, abstract S789
- Liedtke M et al. NEODOO1 demonstrates cardiac and renal biomarker responses in a phase ½ study in patients with AL amyloidosis and persistent organ dysfunction. Presented at Oral Presentation: Multiple myeloma: Clinical studies 1, EHA 2015, Vienna, abstract S104
- Benboubker L et al. Lenalidomide and dexamethasone in transplant-ineligible patients with myeloma.N Engl J Med. 2014;371(10):906-917
- Facon T et al. Updated overall survival analysis of the FIRST study: Continuous lenalidomide plus low-dose dexamethasone vs melphalan, prednisone, and thalidomide in patients with newly diagnosed multiple myeloma. Presented at Oral Presentation: Multiple myeloma: Clinical studies 1, EHA 2015, Vienna, abstract S105
- Hulin C et al. Effect of age on efficacy and safety outcomes in patients with newly diagnosed multiple myeloma receiving lenalidomide and low-dose dexamethasone (Rd): The FIRST trial. Presented at Oral Presentation: Multiple myeloma: Clinical studies 2, EHA 2015, Vienna, abstract S429
- Dimopoulos M et al. Impact of renal impairment on outcomes after treatment with lenalidomide and low-dose dexamethasone in patients with newly diagnosed multiple myeloma: FIRST trial results. Presented at Poster Presentation: Multiple myeloma - Clinical 1, EHA 2015, Vienna, abstract P274
- San Miguel J et al. Pomalidomide plus low-dose dexamethasone versus high-dose dexamethasone alone for patients with relapsed and refractory multiple myeloma (MM-003): a randomised, open-label, phase 3 trial. Lancet Oncol. 2013;14(11):1055–1066
- Moreau P et al. Impact of stable disease as response to pomalidomide plus low-dose dexamethasone on survival outcomes in patients with refractory or relapsed and refractory multiple myeloma in the MM-003-trial. Presented at Oral Presentation: Multiple myeloma: Clinical studies 3, EHA 2015, Vienna, abstract 788
- Bildnachweis: „The statue of Johann Strauss in City park of Vienna.”: © geothea/Fotolia; "Fiaker vor der Alten Hofburg": © pure-life-pictures/Fotolia
MDS/AML – Genmutationen und ihre klinische, prognostische und therapeutische Relevanz stehen weiterhin im Mittelpunkt der Forschung
Dr. med. Catharina Müller-Thomas, Klinikum rechts der Isar, München

Auf der in Wien abgehaltenen 20. Jahrestagung der European Hematology Association (EHA) gab es wieder eine Vielzahl von interessanten Vorträgen zu den myelodysplastischen Syndromen (MDS) und zur akuten myeloischen Leukämie (AML). Anlässlich des 20. Geburtstages wurde das Kongressprogramm umgestaltet und ein größeres Augenmerk auf die Grundlagenforschung gelegt. Viele Vorträge widmeten sich deshalb den somatischen Genmutationen und der klonalen Hämatopoese bei MDS und AML. Ein klinisches Highlight bei EPO-refraktärem Niedrigrisiko-MDS stellt die neue Substanz Luspatercept dar. Bei älteren AML-Patienten stehen die hypomethylierenden Substanzen im Mittelpunkt.
Niedrigrisiko-MDS – Lenalidomid zeigt Wirksamkeit bei MDS non-del(5q), und Luspatercept bahnt sich seinen Weg in der Anämiebehandlung bei ESA-refraktären MDS-Patienten
Für ESA-refraktäre MDS-Patienten gibt es nach wie vor keine zugelassene Therapie. Auf dem letzten ASH-Kongress im Dezember 2014 wurden die Ergebnisse der MDS-005-Studie von Valeria Santini präsentiert [1]. In dieser Phase-3-Studie wurde die Wirksamkeit von Lenalidomid bei ESA-refraktären, transfusionspflichtigen Patienten mit Niedrigrisiko-MDS (IPSS niedrig/intermediär-1) ohne Deletion 5q untersucht. Unter Therapie mit Lenalidomid (10 mg tgl.) wurden signifikant mehr Patienten ›= 56 Tage transfusionsfrei als unter Placebo (26,9 % vs. 2,5 %, p < 0,001). Die mediane Dauer der Transfusionsfreiheit ›= 56 Tage lag bei 8,2 Monaten. Auf dem EHA-Kongress 2015 wurden jetzt von Valeria Santini aktuelle Daten der MDS-005-Studie zur Lebensqualität als Poster vorgestellt [2]. Dabei wurden unter Verwendung des QLQ-C30-Fragebogens die Aspekte ”Fatigue”, ”Dyspnoe”, ”physische Fähigkeit”, ”emotionale Fähigkeit” und ”allgemeine Lebensqualität” zunächst bei Studienbeginn, dann in den Wochen 12 und 24, anschließend alle drei Monate und schließlich noch einmal nach Therapieende evaluiert. Aufgrund der geringen Patientenzahl nach Woche 24 war ein Vergleich zwischen den Lenalidomid-Patienten und den Placebo-Patienten nur in den Wochen 12 und 24 möglich. Während sich in Woche 12 kein Unterschied zwischen den beiden Gruppen zeigte, wiesen in Woche 24 die Lenalidomid-Patienten in allen Aspekten eine deutlich bessere Lebensqualität auf als die Placebo-Patienten; insbesondere die transfusionsfreien Patienten erfreuten sich einer statistisch signifikanten (p < 0,01) besseren Lebensqualität.
Für ESA-refraktäre MDS-Patienten könnte der modifizierte Activin-Rezeptor Typ IIB (ActRIIB) ACE-536 (= Luspatercept) künftig die therapeutischen Optionen erweitern. Bereits auf dem EHA-Kongress 2014 hatte Prof. U. Platzbecker die vorläufigen Ergebnisse einer Phase-1/2-Studie mit Luspatercept vorgestellt [3]. Auf der diesjährigen EHA-Tagung in Wien präsentierte Prof. U. Platzbecker jetzt die offiziellen Ergebnisse der PACE-MDS-Studie [4]. In die PACE-MDS-Studie konnten Patienten mit Niedrigrisiko-MDS (IPSS niedrig/intermediär-1), die ESA-refraktär und nicht mit hypomethylierenden Substanzen vorbehandelt waren, eingeschlossen werden. Vortherapien mit Lenalidomid, G-CSF und natürlich EPO waren erlaubt. Als primäre Endpunkte wurden Hb-Anstieg ›= 1,5 g/dl für über zwei Wochen und Abnahme des Transfusionsbedarfs um 50 % über acht Wochen definiert. Insgesamt wurden 49 Patienten in die PACE-MDS-Studie eingeschlossen. Luspatercept wurde über drei Monate alle drei Wochen subkutan appliziert. In den Dosisgruppen ”0,125–0,5 mg/kg KG” (n = 9) wurden die primären Endpunkte nur in 33 % erreicht, in den Dosisgruppen ”0,75–1,75 mg/kg KG” (n = 40) hingegen in 58 % (Abb. 1). Transfusionsfrei wurden 37 % (11/30) der Patienten, wobei Patienten mit niedriger Transfusionsfrequenz deutlich besser profitierten als Patienten mit hoher Transfusionsfrequenz (4/6 vs. 7/24). Die Subgruppenanalysen ergaben, dass Ringsideroblasten und SF3B1-Mutationen mit hohen Ansprechraten assoziiert sind.
Aktuell läuft die PACE-MDS-Extensionsstudie, die die Effektivität von Luspatercept über zwölf Monate evaluiert.
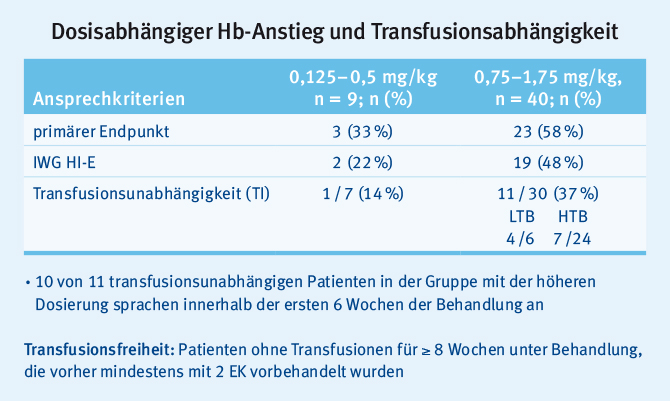 Abb. 1: Hb-Anstieg und Abnahme des Transfusionsbedarfs unter einer Therapie mit Luspatercept in unterschiedlichen Dosierungen bei ESA-refraktären MDS-Patienten (modifiziert nach Platzbecker U et al. Presented at Oral Presentation: MDS Clinical, EHA 2015, Vienna, Abstract S509 [4]).
Abb. 1: Hb-Anstieg und Abnahme des Transfusionsbedarfs unter einer Therapie mit Luspatercept in unterschiedlichen Dosierungen bei ESA-refraktären MDS-Patienten (modifiziert nach Platzbecker U et al. Presented at Oral Presentation: MDS Clinical, EHA 2015, Vienna, Abstract S509 [4]).Fazit
Lenalidomid ist bei Niedrigrisiko-MDS non-del(5q) wirksam und stellt eine mögliche Therapieoption für ESA-refraktäre transfusionspflichtige Patienten dar. Mit Luspatercept bereichert eine neue Substanzgruppe die Anämiebehandlung in der MDS-Therapie.
„Luspatercept ist auf dem Weg zur neuen Therapieoption in der Anämiebehandlung für ESA-refraktäre MDS-Patienten.“ Dr. Catharina Müller-Thomas
Hochrisiko-MDS – Azacitidin ist nach wie vor Goldstandard
Für Patienten, die nicht für eine allogene Stammzelltransplantation infrage kommen, ist Azacitidin die einzige zugelassene Therapie. G. Garcia-Manero präsentierte jetzt auf dem EHA-Kongress auf einem Poster die Ergebnisse einer Ad-hoc-Analyse zur Effektivität von oralem Azacitidin (CC-486) bei Hochrisiko-MDS (IPSS intermediär-2/hoch [5]). Es wurden insgesamt 26 Patienten in verschiedenen Dosisgruppen behandelt. Die Gesamtansprechrate (ORR) lag bei 56 %; Patienten mit Vortherapien erreichten in 40 % ein Therapieansprechen (ORR), Patienten ohne Vortherapie in 67 %. Eine Verbesserung des Blutbilds (HI) zeigten 52 % der Patienten.
Fazit
In der Therapie des Hochrisiko-MDS bleibt Azacitidin weiterhin der Goldstandard.
AML bei jungen und fitten Patienten – MRD-Monitoring anhand NMT3A-Mutationen
Zur AML-Therapie bei jungen und fitten Patienten gab es nichts wesentlich Neues. Verena Gaidzik von der Deutsch-Österreichischen Studiengruppe Akute Myeloische Leukämie (AMLSG) stellte Daten zum MRD-Monitoring von DNMT3A-Mutationen vor [6]. DNMT3A-Mutationen kommen bei 15–25 % aller AML-Patienten vor und gelten als prognostisch ungünstig. 1.168 Proben (Blut und Knochenmark) von 159 DNMT3Amut-Patienten wurden bei Diagnosestellung, während der Therapie und im Follow-up analysiert. Das DNMT3Amut-Transkriptlevel bei AML-Diagnose hatte weder Einfluss auf das Gesamtüberleben noch auf das rezidivfreie Überleben; auch der Abfall des DNMT3Amut-Transkriptlevels unter Therapie blieb ohne prognostische Relevanz. DNMT3A-Mutationen persistierten unabhängig vom Erreichen einer kompletten Remission (CR) bei den meisten Patienten. In weiteren Studien sollen DNMT3A-Mutationen als Marker für klonale Hämatopoese untersucht werden.
Fazit
Im Gegensatz zu NPM1-Mutationen eignen sich DNMT3A-Mutationen derzeit noch nicht als MRD-Marker
AML bei älteren und unfitten Patienten – hypomethylierende Substanzen
In einem Übersichtsvortrag auf einem Satelittensymposium beschäftigte sich Frau Prof. K. Götze mit der AML-Therapie beim älteren Menschen [7]. Die unbefriedigenden Therapieresultate ergeben sich unter anderem durch Patientenfaktoren – insbesondere die Komorbiditäten – und durch Krankheitsfaktoren. Hier spielen die im Alter zunehmenden, ungünstigen Chromosomenaberrationen eine große Rolle. In der AML-Therapie der älteren Patienten haben sich die hypomethylierenden Substanzen Decitabin und Azacitidin etabliert.
In der DACO-016-Studie wurden Patienten ›= 65 Jahre entweder mit Decitabin (20 mg/m², d1–5, q28) oder einer Supportivtherapie beziehungsweise niedrig dosiertem AraC behandelt [8]. Das verlängerte mediane Gesamtüberleben und die besseren Ansprechraten im Decitabin-Arm führten zur Zulassung von Decitabin für die Behandlung älterer AML-Patienten. In der AZA-AML-001-Studie wurden ältere Patienten mit neu diagnostizierter AML und > 30 Blasten mit Azacitidin oder mit einer ”konventionellen” Therapie (CCR) behandelt. Die Ergebnisse dieser Studie wurden auf dem EHA-Kongress 2014 von Prof. Hervé Dombret präsentiert und kürzlich publiziert [9]. Das mediane Überleben (OS) der mit Azacitidin behandelten AML-Patienten lag bei 10,4 Monaten, während es bei den ”konventionell” behandelten (CCR) Patienten bei 6,5 Monaten lag (p = 0,083). Frau Prof. K. Götze fokussierte sich in ihrem Vortrag auf die Subgruppenanalysen der AZA-AML-001-Studie, die zum Teil auch als Poster auf der EHA-Tagung 2015 vorgestellt wurden [10,11,12,13]. Beim Vergleich der Therapie mit Azacitidin (AZA) mit Supportivtherapie (BSC) beziehungsweise niedrig dosiertem AraC (LDAC) oder intensiver Chemotherapie (IC) wiesen die mit Azacitidin behandelten Patienten in allen Therapiegruppen einen Überlebensvorteil auf: OS (AZA vs. BSC) 5,8 vs. 3,7 Monate; OS (AZA vs. LDAC) 11,2 vs. 6,4 Monate; OS (AZA vs. IC) 13,3 vs. 12,2 Monate (Abb. 2). Bei AML mit dysplastischen Veränderungen erreichten die mit Azacitidin behandelten Patienten ein medianes Gesamtüberleben von 12,7 Monaten (CCR-Patienten: 6,3 Monate, p = 0,036). Auch Patienten ohne komplette Remission erreichten unter Azacitidin ein medianes Gesamtüberleben von 6,9 Monaten (CCR-Patienten: 4,2 Monate, p = 0,0170) (Abb. 3). Insgesamt zeigt Azacitidin auch bei AML mit > 30 % Blasten eine gute Wirksamkeit und ein günstiges Nebenwirkungsprofil.
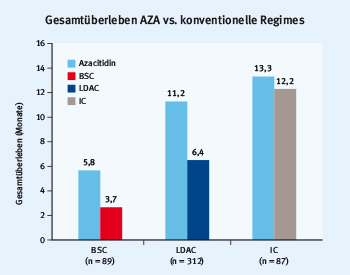 Abb. 2: Gesamtüberleben bei Patienten, die mit Azacitidin (AZA) oder einer Supportivtherapie (BSC) beziehungsweise. niedrig dosiertem AraC (LDAC) oder intensiver Chemotherapie (IC) therapiert wurden (modifiziert nach Dombret H et al. Blood 2015 [9]).
Abb. 2: Gesamtüberleben bei Patienten, die mit Azacitidin (AZA) oder einer Supportivtherapie (BSC) beziehungsweise. niedrig dosiertem AraC (LDAC) oder intensiver Chemotherapie (IC) therapiert wurden (modifiziert nach Dombret H et al. Blood 2015 [9]).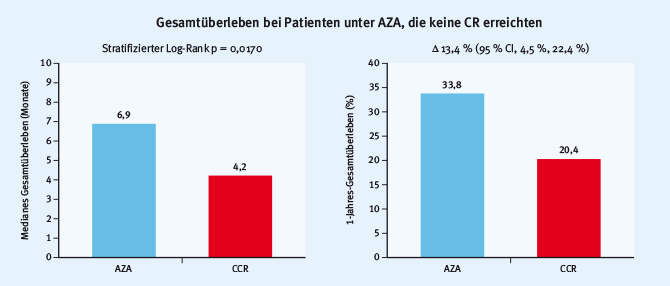 Abb. 3: Medianes Gesamtüberleben und 1-Jahres-Gesamtüberleben bei Patienten unter einer Therapie mit Azacitidin (AZA) im Vergleich zu einer konventionellen Therapie, die keine komplette Remission (CR) aufweisen (modifiziert nach Dombret H et al. Blood 2015 [9]).
Abb. 3: Medianes Gesamtüberleben und 1-Jahres-Gesamtüberleben bei Patienten unter einer Therapie mit Azacitidin (AZA) im Vergleich zu einer konventionellen Therapie, die keine komplette Remission (CR) aufweisen (modifiziert nach Dombret H et al. Blood 2015 [9]).Auf dem EHA-Kongress 2014 wurden die positiven Ergebnisse einer Phase-2-Studie mit der hypomethylierenden Substanz der 2. Generation SGI-110 bei älteren Patienten mit AML vorgestellt [14]. Zu dieser Studie gab es in diesem Jahr ein Poster mit einem Update der Daten [15]. SGI-110 (Guadecitabin) ist ein Dinukleotid, das subkutan verabreicht wird. Es schützt das Decitabin vor der Deaminierung und verlängert so dessen Halbwertszeit. Es wurden insgesamt 51 Patienten >= 65 Jahre mit AML und mindestens einem Risikofaktor (sAML, ungünstige Zytogenetik, kardiale und/oder pulmonale Komorbidität, EGOG 2) in die Studie eingeschlossen. Die Rate an kompletten Remissionen (CR) lag bei 37 %, die CRc bei 57 %. Das mediane Gesamtüberleben lag bei 10,5 Monaten. Zurzeit wird Guadecitabin in der Phase-3-Studie ASTRAL-1 evaluiert.
Fazit
Die beiden hypomethylierenden Substanzen Azacitidin und Decitabin sind eine gute Therapieoption für ältere oder unfitte Patienten mit AML. Mit Guadecitabin steht bald die zweite Generation der hypomethylierenden Substanzen in der AML-Therapie älterer Patienten zur Verfügung.
”In der Behandlung des älteren oder unfitten Patienten mit AML spielen die hypomethylierenden Substanzen eine wichtige Rolle. Neben Decitabin wird wahrscheinlich bald Azacitidin für die AML-Therapie zugelassen sein.” Dr. Catharina Müller-Thomas
MDS und AML – Genmutationen im Mittelpunkt des wissenschaftlichen Interesses
Im Zuge des Next-Generation-Sequencing (NGS) wurden speziell bei MDS del(5q) CSNK1A1-Mutationen (kodierend für Caseinkinase 1a1) entdeckt. Manja Meggendorfer untersuchte die Häufigkeit von CSNK1A1- und anderen typischen MDS-Mutationen bei 115 Patienten mit MDS del(5q) [16]. CSNK1A1 liegt auf Chromosom 5 (5q32) und ist meistens (91 %, 102/112) deletiert. Die Analysen ergaben eine hohe Mutationsfrequenz von DNMT3A > TP53 > SF3B1 > TET2 > CSNK1A1 > ASXL1 > JAK2. Überraschend war die Häufung von TP53-Mutationen bei MDS del(5q) im Vergleich zu anderen MDS (18 % vs. 6 %, p < 0,001). CSNK1A1-Mutationen waren häufig mit Mutationen des Splicing-Apparates assoziiert. Für die Prognose von Patienten mit MDS del(5q) ist die Anzahl an Genmutationen ausschlaggebend; das mediane Gesamtüberleben lag bei ‹= 1 Mutation bei 91 Monaten und bei > 1 Mutation bei nur noch 36 Monaten (p = 0,061).
Im AML-Educational gab George Vassiliou einen Überblick über AML mit normalem Karyotyp (AML-NK) [17]. AML-NK ist aufgrund der vielfältigen Genmutationen eine sehr heterogene Erkrankung. Die wissenschaftliche Herausforderung der nächsten Jahre wird es sein, den Stellenwert der verschiedenen Mutationen im Hinblick auf den Erkrankungsverlauf und die Prognose zu evaluieren und maßgeschneiderte Therapien zu entwickeln.
Fazit
Genmutationen bei hämatologischen Neoplasien, vor allem ihre Bedeutung für Prognose und Therapie, stehen derzeit besonders im wissenschaftlichen Interesse.
„Genmutationen spiegeln die Heterogenität von MDS und AML wider. Die große Herausforderung besteht darin, irgendwann Therapiekonsequenzen aus ihnen ziehen zu können.” Dr. Catharina Müller-Thomas
Quellen
- Santini V. et al., Efficacy and safety of lenalidomide versus placebo in RBC-transfusion dependent patients with IPSS low/intermediate-1-risk myelodysplastic syndromes without del(5q) and unresponsive or refractory to erythropoiesis-stimulating agents: Results from a Randomized Phase 3 Study (CC-5013-MDS-005). Blood 2014; 124: abstract 409
- Santini V. et al., The effect of lenalidomide on health-related quality of life in patients with myelodysplastic syndromes: Results from the MDS-005 trial. Presented at Poster Presentation, Myelodysplastic syndromes -Clinical 1, EHA 2015, Vienna, abstract P242
- Platzbecker U et al. ACE-536 increases hemoglobin levels in patients with low or intermediate-1 risk myelodysplastic syndromes (MDS):preliminary results from a phase 2 study. Presented at Simultaneous Sessions: Myelodysplastic Syndromes – Clinical, EHA 2014, Milano, abstract s1296
- Platzbecker U. et al. Luspatercept increases hemoglobin and reduces transfusion burden in patients with low or intermediate-1 risk myelodysplastic syndromes: Preliminary results from the phase 2 PACE-MDS study. Presented at Oral Presentation MDS Clinical, EHA 2015, Vienna, Abstract S509
- Garcia-Manero G. et al. Efficacy of CC-486 (oral azacitidine) treatment in patients with higher-risk myelodysplastic syndromes. Presented at Poster Presentation, Myelodysplastic syndromes - Clinical 2, EHA 2015, Vienna, abstract P618
- Gaidzik V. et al., DNMT3A mutations in acute myeloid leukemia: Monitoring of minimal residual disease. A study of the AML Study Group. Presented at Oral Presentation, Molecular markers in AML, EHA 2015, Vienna, abstract S451
- Götze K., Current non-curative treatment options in AML. Presented at Celgene Satellite Symposium, Practical Insights on the diagnosis and initial management of AML, EHA 2015, Vienna
- Kantarjian HM. Multicenter, randomized, open-label, phase III trial of decitabine versus patient choice, with physician advice, of either supportive care or low-dose cytarabine for the treatment of older patients with newly diagnosed acute myeloid leukemia. J Clin Oncol 2012;30 (21):2670–2677
- Dombret H et al. International phase 3 study of azacitidine vs conventional care regimens in older patients with newly diagnosed AML with >30% blasts. Blood 2015 pii: blood-2015-01-621664. [Epub ahead of print]
- Schuh A. et al., Overall survival without complete remission in older patients with acute myeloid leukemia: Azacitidine vs conventional care regimens in the AZA-AML-001 Study. Presented at Poster Presentation, Acute myeloid leukemia - Clinical 4, EHA 2015, Vienna, abstract P575
- Seymour J. et al. Overall survival and clinical outcome in older patients with acute myeloid leukemia treated with azacitidine or low-dose cytarabine in the AZA-AML-001 Study. Presented at E-poster, EHA 2015, Vienna, abstract E954
- Döhner H. et al., Overall survival and clinical outcomes in older patients with acute myeloid leukemia treated with azacitidine or intensive chemotherapy in the AZA-AML-001 Study. Presented at Poster Presentation, Acute myeloid leukemia - Clinical 3, EHA 2015, Vienna, abstract P566
- Minden M. et al., The effect of azacitidine on health-related quality of life in older patients with newly diagnosed acute myeloid leukemia: Results from the AZA-AML-001 Trial. Presented at Poster Presentation, Acute myeloid leukemia - Clinical 3, EHA 2015, Vienna, abstract P184
- Yee K. et al., Results of a randomized multicenter phase 2 study of a 5-day regimen of SGI-110, a novel hypomethylating agent, in treatment naïve elderly acute myeloid leukemia not eligible for intensive therapy. Presented at Simultaneous Sessions: Acute Myeloid Leukemia– Clinical 1, EHA 2014, Milano, abstract s647
- Kropf P. et al., Late responses and overall survival from long term follow up of a randomized phase 2 study of SGI-110 (Guadecitabine) 5-day regimen in elderly AML who are not eligible for intensive chemotherapy. Presented at Poster Presentation, Acute myeloid leukemia - Clinical 4, EHA 2015, Vienna, abstract P571
- Meggendorfer M. et al., CSNK1A1 behaves like a tumor suppressor gene and mutations in CSNK1A1associate with mutations in spliceosomal genes in myelodysplastic syndrome with isolated del(5q). Presented at Oral Presentation: Biology in MDS, EHA 2015, Vienna, abstract S135
- Vassiliou G., Unraveling molecular biology normal karyotype AML. Presented at Education Session: Acute myeloid leukemia, EHA 2015, Vienna
- Bildnachweis: „Belvedere Palace, garden and fountains, Vienna, Austria”: © Jenifoto/Fotolia
Lymphome – brauchen wir noch die Chemotherapie?
Prof. Dr. med. Kai Hübel, Klinik I für Innere Medizin, Universitätsklinikum Köln
 Bereits seit einigen Jahren zeichnet sich ein dramatischer Umbruch bei der Therapie maligner Lymphome ab. Neue zielgerichtete Substanzen stellen bewährte Zytostatikaregime infrage oder bieten eine sinnvolle Ergänzung. Mit Spannung wurde erwartet, ob sich diese Entwicklung durch die auf dem EHA präsentierten Daten fortsetzt und wie sich neue Therapieoptionen in die Behandlungsalgorithmen einfügen.
Bereits seit einigen Jahren zeichnet sich ein dramatischer Umbruch bei der Therapie maligner Lymphome ab. Neue zielgerichtete Substanzen stellen bewährte Zytostatikaregime infrage oder bieten eine sinnvolle Ergänzung. Mit Spannung wurde erwartet, ob sich diese Entwicklung durch die auf dem EHA präsentierten Daten fortsetzt und wie sich neue Therapieoptionen in die Behandlungsalgorithmen einfügen.
Lymphombehandlung – neue Daten, neue Entwicklungen
In den USA und der EU bereits zugelassen ist der orale PI3K-Inhibitor Idelalisib (PI3K = Phosphoinositid-3-Kinase) für die Behandlung der Chronischen Lymphatischen Leukämie (CLL) in Kombination mit Rituximab und als Monotherapie bei rezidivierten Follikulären Lymphomen (FL). Wichtig ist die weitere Beobachtung der Substanz auch unter Sicherheitsaspekten. Coutre und Kollegen werteten dafür acht klinische Studien mit über 760 Patienten aus, die Idelalisib bei rezidivierten indolenten Lymphomen einschließlich CLL als Monotherapie oder Teil einer Kombination erhielten (Coutre, P588) [1]. Die häufigsten Nebenwirkungen Grad 3/4 in der Monotherapie waren Neutropenie (23 %), Thrombopenie (11 %), Erhöhung der Transaminasen (16 %), Diarrhö/Kolitis (11 %, Auftreten meist erst nach 6–12 Monaten Behandlung) und Pneumonie (11 %). Als Teil einer Kombinationsbehandlung kam es außerdem häufig zu Fieber (12 %). Eine Therapiepause ermöglichte bei den meisten Patienten eine spätere Wiederaufnahme der Behandlung. Die gute Lebensqualität von CLL-Patienten unter Idelalisib in Kombination mit Rituximab wurde auch in einer weiteren Studie auf dem EHA bestätigt [2].
Eine innovative Substanz für die Therapie maligner Lymphome stellt der orale BCL-2-Inhibitor Venetoclax (ABT-199/GDC-0199) dar, der bereits in mehreren klinischen Studien als Monotherapie erfolgversprechend geprüft wurde. In einer Phase-I-Studie wurde die Substanz in Kombination mit Bendamustin (2d, 90 mg/m²) und Rituximab (1d, 375 mg/m²) bei rezidivierten indolenten und aggressiven Lymphomen eingesetzt [3]. Venetoclax wurde in einer Dosiseskalation verabreicht. Das Ansprechen der insgesamt 35 eingeschlossenen Patienten zeigt Tab. 1. Besonders gut profitierten Patienten mit einem indolenten Lymphom von der Substanz. Die häufigsten Nebenwirkungen Grad 3/4 waren Lymphozytenabfall (34 %), Neutropenie (31 %), Thrombopenie (20 %) und Anämie (17%). Die häufigste schwere Nebenwirkung war febrile Neutropenie (9 %). Die maximale tolerable Dosis konnte noch nicht ermittelt werden.
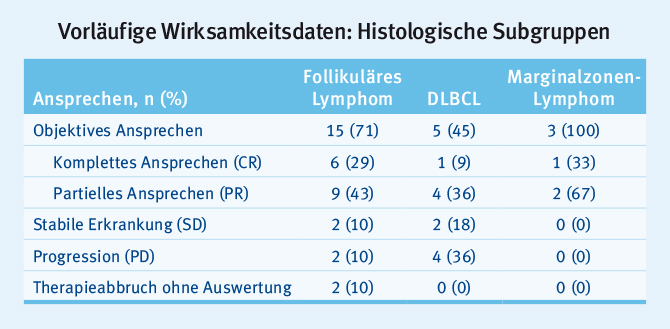 Tab. 1: Wirksamkeit von Venetoclax (ABT-199/GDC-0199) in Kombination mit Bendamustin und Rituximab bei rezidivierten indolenten und aggressiven Lymphomen (modifiziert nach [3]).
Tab. 1: Wirksamkeit von Venetoclax (ABT-199/GDC-0199) in Kombination mit Bendamustin und Rituximab bei rezidivierten indolenten und aggressiven Lymphomen (modifiziert nach [3]).Nivolumab ist ein humaner, monoklonaler PD-1-blockierender Antikörper, der zu einer Aktivierung von T-Zellen führt und für den bereits bei verschiedenen Lymphomen eine Wirksamkeit gezeigt wurde. In der präsentierten Studie wurde nun ein Update einer Phase-I-Studie mit 105 Patienten vorgestellt [4]. Alle Patienten waren mehrfach vorbehandelt. Gut profitierten Patienten mit klassischem Hodgkin-Lymphom (HL) von der Substanz (n = 20; 4 komplette Remissionen [CR]; 12 partielle Remissionen [PR]), sowie Patienten mit diffus großzelligem B-Zell-Lymphom (DLBCL; n = 11; 2 CR; 2 PR) und FL (n = 10; 1 CR; 3 PR). Häufigste Nebenwirkungen (> 10 %) waren Fatigue (15 %) und Rash (11 %). Häufigste schwere Nebenwirkung war die Pneumonitis (5 %).
In der frühen klinischen Entwicklung befindet sich der monoklonale Antikörper MOR208, der gegen CD19 gerichtet ist und in einer Phase-IIa-Studie bei rezidivierten und refraktären B-Zell-Non-Hodgkin-Lymphomen mit einer Dosis von 12 mg/kg/Woche eingesetzt wurde [5]. Der Antikörper wurde als Monotherapie über mindestens zwei Monate bei 92 Patienten mit verschiedenen Histologien eingesetzt. Je nach Ansprechen war im Anschluss eine Erhaltungstherapie alle 2–4 Wochen möglich. 87 % der Patienten wiesen ein Krankheitsstadium III/IV auf und hatten im Median 2 Vortherapien erhalten. Das beste Ansprechen zeigten Patienten mit DLBCL mit einer Gesamtansprechrate (ORR) von 26 % (n = 35) sowie FL-Patienten mit einer ORR von 27 % (n = 45). Die längste Remissionsdauer betrug bisher bei DLBCL 15,4 Monate und bei FL 14,2 Monate. Die Verträglichkeit der Substanz war gut, auch fanden sich keine signifikanten Infusionsreaktionen.
„Während die meisten zielgerichteten Substanzen in der Monotherapie bei aggressiven Lymphomen nur eine geringe Wirksamkeit zeigen, scheint der monoklonale Antikörper MOR208 auch beim DLBCL besonders wirksam zu sein.“ Prof. Dr. Kai Hübel
Fazit
- Idelalisib und Venetoclax belegen mit diesen Studien erneut die gute Wirksamkeit und Tolerabilität bei der Behandlung ausgewählter maligner Lymphome.
- Nivolumab zeigt insbesondere beim klassischen HL eine gute Wirksamkeit.
- Mit dem monoklonalen Antikörper MOR208 erscheint eine weitere vielversprechende Substanz am Horizont.
Diffus großzelliges B-Zell-Lymphom (DLBCL)
Eine besondere Herausforderung bei der Therapie der DLBCL sind alte Patienten, die einer intensiven Therapie mit kurativer Zielsetzung nicht mehr zugänglich sind. In einer italienischen Studie an 24 Zentren wurden insgesamt 49 DLBCL-Patienten mit einer Kombination aus Bendamustin (90 mg/m² Tag 1–2) und Rituximab (Tag 1, alle 28 Tage bis zu 6 Zyklen) behandelt, die aufgrund ihres Alters und Allgemeinzustands nicht mehr für eine Therapie mit R-CHOP geeignet waren [6]. Das mediane Alter lag bei 82 Jahren, 25 Patienten erhielten alle 6 Therapiezyklen. Die häufigste Nebenwirkung, die zu einem Therapieabbruch führte, war eine persistierende Zytopenie (3 Patienten). Die ORR betrug 64 %, davon 55 % CR. Das 2-Jahres-progressionsfreie Überleben (PFS) lag bei 44 %, das 2-Jahres-Gesamtüberleben (OS) bei 59 %. Abb. 1 zeigt die zugehörigen Überlebenskurven.
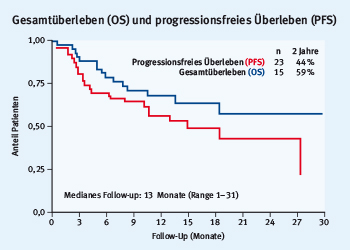 Abb. 1: Bendamustin+Rituximab: Überlebenskurven bei DLBCL-Patienten, die nicht für eine Therapie mit R-CHOP geeignet waren (modifiziert nach [6]).
Abb. 1: Bendamustin+Rituximab: Überlebenskurven bei DLBCL-Patienten, die nicht für eine Therapie mit R-CHOP geeignet waren (modifiziert nach [6]).Neben älteren und komorbiden Patienten ist auch die Therapie von Patienten mit mehrfach rezidiviertem DLBCL eine Herausforderung. In dieser Situation werden dringend neue wirksame Substanzen benötigt. Bereits auf dem letzten ASH-Kongress wurde über Selinexor berichtet, eine oral verfügbare Substanz, die über die Antagonisierung des Proteins XPO1 die Transportmechanismen in der Lymphomzelle blockiert. Auf dem EHA wurde nun ein Update zur Wirksamkeit dieser Substanz präsentiert (Phase I; n = 31; mediane Anzahl an Vortherapien: 3; Dosis: 3–80 mg/m², 8–10 Dosen in 4-Wochen-Zyklen) [7]. Als Nebenwirkungen Grad 3/4 fanden sich insbesondere Thrombopenie (62 %), Neutropenie (24 %) und Anämie (24 %) sowie Fatigue, Hyponatriämie, synkopale Ereignisse und Verwirrtheit (jeweils 10 %). Diese Toxizitäten waren aber gut beherrschbar. Die ORR lag bei 39 % (PR: 26 %, CR: 4 %). Die mediane Dauer des Ansprechens betrug 7 Monate.
Eine nach wie vor intensiv geführte Diskussion betrifft den Einsatz von subkutanem Rituximab anstelle der intravenösen Applikation. In der sogenannten „MABEASE“-Studie erhielten 576 Patienten mit der Erstdiagnose DLBCL 6–8 Zyklen CHOP14/21, kombiniert mit intravenösem (i.v.) oder subkutanem (s.c.) Rituximab (1.400 mg ab Zyklus 2), die Randomisierung erfolgte 1:2 [8]. Es zeigten sich bzgl. Effektivität und Nebenwirkungen keine Unterschiede zwischen beiden Armen.
Fazit
- Ältere und komorbide Patienten, für die eine Therapie mit R-CHOP zu toxisch erscheint, haben mit einer Kombination aus Bendamustin und Rituximab eine realistische Chance auf eine mehrmonatige Lymphomkontrolle bei erhaltener Lebensqualität.
- Mit Selinexor könnte zukünftig auch mehrfach rezidivierten Patienten eine sinnvolle Therapie angeboten werden.
- Die Vergleichbarkeit von Rituximab s.c. gegenüber Rituximab i.v. wurde abermals bestätigt.
Follikuläres Lymphom (FL)
Das Risiko der Transformation eines FL in ein DLBCL wird in der Literatur sehr unterschiedlich angegeben. In einer umfangreichen retrospektiven Erhebung der spanischen Studiengruppe GELTAMO wurden die Daten von 1.096 Patienten mit FL bzgl. der Transformationsrate nach exakt festgelegten Kriterien analysiert [9]. Nach einem medianen Follow-Up von 6 Jahren zeigten 6,5 % der Lymphome eine Transformation, die kumulative Inzidenz nach 5, 10 und 15 Jahren lag bei 5 %, 8 % und 14 %.
In einer univariaten Analyse wurden folgende signifikanten Risikofaktoren für eine Transformation identifiziert:
- Hoher Risikoscore (FLIPI >= 2)
- Alter > 60 Jahre
- Keine Rituximab-Vorbehandlung
- Therapielinie > 1
In der multivariaten Analyse fanden sich die beiden folgemden signifikanten Risikofaktoren: FLIPI >= 2 und Therapielinie > 1.
Ein interessanter Ansatz beim rezidivierten FL ist die Gabe von Polatuzumab Vedotin (POV), eines Anti-CD79b-Antikörper-Wirkstoff-Konjugats, in der Kombination mit Rituximab. In der vorgestellten Arbeit wurden zwei POV-Dosierungen verglichen (2,4 mg/kg oder 1,8 mg/kg; jeweils mit Rituximab; alle 21 Tage; insgesamt 45 Patienten) [10]. Es zeigte sich eine ORR von 73 %, wobei Patienten mit der höheren Dosierung eine höhere CR-Rate erreichten (44 % versus 20 %). Das PFS nach einem Jahr lag in beiden Gruppen bei über 60 %, Hauptnebenwirkung in beiden Gruppen war die periphere Neuropathie.
Fazit
- Die Rate an DLBCL-transformierten FL liegt mit deutlich unter 10 % zehn Jahre nach Erstdiagnose wesentlich niedriger als vielfach angenommen.
- Mit Polatuzumab Vedotin (POV) steht hoffentlich zukünftig ein wirkungsvolles Antikörper-Wirkstoff-Konjugat beim rezidivierten FL zur Verfügung.
Mantelzelllymphom (MCL)
Mit Lenalidomid steht ein oraler Immunmodulator zur Verfügung, der bereits bei verschiedenen Lymphomentitäten eine sehr gute Wirksamkeit und Verträglichkeit gezeigt hat. In der auf dem letzten ASH vorgestellten SPRINT-Studie [11] wurde Lenalidomid (25 mg/Tag, Tag 1–21, alle 28 Tage) bei insgesamt 254 Patienten mit rezidiviertem MCL gegen eine Einzelsubstanz nach Wahl des Arztes („investigator choice“) randomisiert. Es zeigte sich eine hochsignifikante Verbesserung des medianen PFS durch Lenalidomid (8,7 Monate versus 5,2 Monate, p = 0,004). Auf dem EHA wurde nun in einer Subgruppenanalyse über den Einfluss der Vortherapie auf das PFS berichtet [12]. Dabei zeigte sich auch in folgenden Subgruppen eine statistisch signifikante Verbesserung des PFS durch Lenalidomid:
- Patienten mit zwei oder mehr Vortherapien
- Patienten mit mehr als einem Rezidiv
- Therapierefraktäre Patienten
- Patienten mit Rituximab-Vorbehandlung
- Patienten ohne vorherige Hochdosistherapie
- Patienten mit mindestens 6 Monaten seit der letzten Therapie, aber weniger als drei Jahren seit Diagnosestellung
„Die SPRINT-Studie belegt eindrucksvoll die Überlegenheit einer chemotherapiefreien Therapie gegenüber einer Chemotherapie – auch bei rezidivierten Lymphomen mit typischerweise aggressivem Verlauf, wie zum Beispiel dem MCL.“ Prof. Dr. Kai Hübel
Eine neuartige vielversprechende Form der Immuntherapie besteht in der Infusion autologer T-Zellen, die mit einem chimären Antigenrezeptor gegen CD19 modifiziert wurden (sogenannte CAR-T-Zellen). In einer präklinischen Arbeit wurden jetzt MCL-Zelllinien nach Vorbehandlung und parallel zu Ibrutinib mit CAR-T-Zellen behandelt, und zwar sowohl Ibrutinib-sensitive als auch Ibrutinib-resistente Zellen [13]. Durch die CAR-T-Zellen konnte die Tumorkontrolle wesentlich verbessert werden, auch bei Ibrutinib-refraktären Zellen.
Fazit
- Die SPRINT-Studie zeigt die gute Wirksamkeit von Lenalidomid beim rezidivierten MCL auch in problematischen Subgruppen.
- Die Kombination von Ibrutinib und CAR-T-Zellen könnte darüber hinaus zukünftig eine weitere Therapieoption darstellen.
Chronische Lymphatische Leukämie (CLL)
Frühere Studien haben bereits die Wirksamkeit von Lenalidomid bei der rezidivierten oder refraktären CLL belegt. Eine aktuelle Arbeit definierte in einer Phase-I/II-Studie die optimale Dosierung einer Kombination von Lenalidomid mit Rituximab anhand von 29 Patienten mit einem medianen Alter von 75 Jahren und im Median zwei Vortherapien [14]. In diesem Setting lag die maximal tolerable Dosis für Lenalidomid bei 15 mg/Tag. Hierunter erreichten 53 % der Patienten ein Ansprechen, das mediane OS betrug 21,9 Monate. Die wichtigste Nebenwirkung war Neutropenie.
Mit Duvelisib befindet sich ein weiterer Inhibitor des PI3K-Signalwegs in der klinischen Testung. Auf dem EHA wurde jetzt über den Einsatz von Duvelisib bei insgesamt 18 nicht vorbehandelten CLL-Patienten berichtet [15]. Duvelisib wurde in einer Dosierung von 25 mg p.o. zweimal täglich appliziert. Die ORR betrug 82 %, bei einer medianen Therapiedauer von 53 Wochen. Die häufigsten Nebenwirkungen Grad 3/4 waren Neutropenie (39 %) sowie eine Erhöhung der Transaminasen (17 %).
Fazit
- Die Kombination von Lenalidomid mit Rituximab bei rezidivierter CLL zeigt eine gute Wirksamkeit und Verträglichkeit.
- Mit Duvelisib zeichnet sich eine wirksame Erstlinientherapie der CLL ab, allerdings sind noch weitere Studien erforderlich.
Hodgkin-Lymphom (HL)
Abschließend sollen zwei wichtige Studien zum HL erwähnt werden, die auf dem EHA als Vortrag präsentiert wurden. Walewski und Kollegen berichteten über eine weitere Auswertung der „AETHERA-Studie“, die einen deutlichen PFS-Vorteil einer Therapie mit Brentuximab-Vedotin (BV) nach Hochdosisbehandlung gegenüber Placebo nachgewiesen hat [16]. In einer multivariaten Analyse wurden nun folgende Faktoren ermittelt, die signifikant mit einem verlängerten PFS einhergehen [17]:
- Behandlung mit Brentuximab
- Erreichen einer CR vor der Hochdosistherapie
- Weibliches Geschlecht
- Maximal 2 Vortherapien
- Vortherapie mit ABVD (Doxorubicin, Bleomycin, Vinblastin, Dacarbazin)
- Keine B-Symptome
- Gewicht von maximal 100 kg
Die Deutsche Hodgkin-Lymphom Studiengruppe präsentierte ihre Ergebnisse einer Phase-I-Studie zum Therapieregime AVD-Rev (Doxorubicin, Vinblastin, Dacarbazin und Lenalidomid) bei 25 Patienten zwischen 60 und 75 Jahren mit Erstdiagnose eines fortgeschrittenen HL [18]. Die Patienten erhielten zwischen 4 und 8 Zyklen plus Bestrahlung, die maximal tolerable Dosis von Lenalidomid wurde mit 25 mg ermittelt. Die ORR lag bei Patienten, die 25 mg Lenalidomid erhalten hatten, bei 94 %, davon 88 % CR. PFS und OS nach drei Jahren zeigt Abb. 2. Alle Patienten mit 20 oder 25 mg Lenalidomid entwickelten eine Grad 3/4 hämatologische Toxizität (v. a. Anämie (76 %) und Leukopenie (56 %)). Respiratorische Nebenwirkungen entwickelten 21 % der Patienten mit 25 mg Lenalidomid.
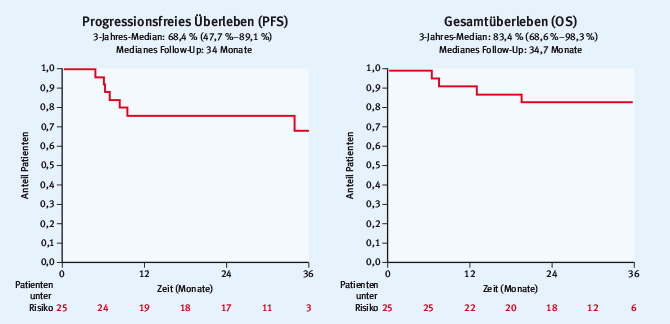 Abb. 2: Progressionsfreies Überleben und Gesamtüberleben unter AVD-Rev (Doxorubicin, Vinblastin, Dacarbazin und Lenalidomid) bei Patienten mit Erstdiagnose eines fortgeschrittenen HL (modifiziert nach [18]).
Abb. 2: Progressionsfreies Überleben und Gesamtüberleben unter AVD-Rev (Doxorubicin, Vinblastin, Dacarbazin und Lenalidomid) bei Patienten mit Erstdiagnose eines fortgeschrittenen HL (modifiziert nach [18]).Fazit
- Auch unter Einbeziehung verschiedener klinischer Faktoren beweist Brentuximab in einer multivariaten Analyse den Stellenwert bzgl. Verbesserung des PFS nach Hochdosistherapie beim HL.
- Der Verzicht auf Bleomycin im ABVD-Regime und die Hinzunahme von Lenalidomid zeigt eine sehr gute Wirksamkeit beim HL, sodass Phase-II/III-Studien geplant werden sollten.
„Auch dieser EHA-Kongress zeigte eindrucksvoll die Richtung, in die sich die Therapie maligner Lymphome entwickelt: immuntherapeutische Therapieansätze in allen Therapielinien, unter Verzicht oder als Ergänzung zur klassischen Chemotherapie.“ Prof. Dr. Kai Hübel
Quellen
- Coutre S et al. Safety of idelalisib in B-cell malignancies: integrated analysis of eight clinical trials. Haematologica, 2015; 100(s1); S433.
- Perard R et al. Quality of life benefits of idelalisib with rituximab for patients with previously treated chronic lymphocytic leukaemia. Haematologica 2015; 100(s1); P214.
- de Vos S et al. A dose-escalation study of the BCL-2 inhibitor venetoclax (ABT-199/GDC-0199) plus bendamustine (B) and rituximab (R) in patients with relapsed/refractory (R/R) non-hodgkin’s lymphoma (NHL). Haematologica 2015; 100(s1); S109.
- Armand P et al. Nivolumab in patients with relapsed or refractory lymphoid malignancies and classical hodgkin lymphoma: updated safety and efficacy results of a phase 1 study (CA209-039). Presented at Oral presentation: Progess in Hodgkin lymphoma therapy: Incorporation of novel agents and reduction of side effects, EHA 2015, Vienna, abstract S808.
- Jurczak W et al. A phase IIa study of single-agent MOR208, an FC-optimized anti-CD19 antibody, in patients with relapsed or refractory B-cell non-hodgkin’s lymphoma. Haematologica 2015; 100(s1); E990.
- Storti S et al. Bendamustine combined with rituximab (BR) in elderly frail patients with newly diagnosed DLBCL. Haematologica 2015; 100(s1); P328.
- Kuruvilla J et al. Patients with heavily pretreated diffuse large B-cell lymphoma (DLBCL) who respond to oral selinexor therapy show prolonged survival: udpated phase 1 results. Haematologica 2015; 100(s1); S485.
- Lugtenburg P et al. Subcutaneous versus intravenous rituximab in combination with CHOP for previously untreated diffuse large B-cell lymphoma: efficacy and safety results from the phase IIIb mabease study. Haematologica 2015; 100(s1); S483.
- Alonso S et al. Incidence of transformation in follicular lymphoma: multicentre retrospective analysis of the spanish group of lymphoma and autologous stem-cell transplantation (GELTAMO). Haematologica 2015; 100(s1); P682.
- Sharman J et al. Two doses of polatuzumab vedotin (POV, anti-C79b antibody-drug conjugate) plus rituximab (R) in patients with relapsed/refractory (R/R) follicular lymphoma (FL): durable responses at lower dose level. Haematologica 2015; 100(s1); P688.
- Trneny M et al. Phase II randomized, multicenter study of lenalidomide vs best investigator’s choice in relapsed/refractory mantle cell lymphoma: results of the MCL-002 (SPRINT) Study. Presented at Session: 624. Lymphoma: Therapy with Biologic Agents, excluding Pre-Clinical Models: Aggressive NHL, ASH 2014, San Francisco, abstract 626.
- Trneny M et al. Impact of prior treatment on PFS for relapsed/refractory mantle cell lymphoma patients randomized to lenalidomide vs investigator’s choice: a subgroup analysis of the phase II MCL-002 (SPRINT) study. Haematologica 2015; 100(s1); S107.
- Ruella M et al. Combination of ibrutinib and anti-CD19 chimeric antigen receptor t cells for the treatment of relapsing/refractory mantle cell lymphoma (MCL). Haematologica 2015; 100(s1); P728.
- De La Fuente A et al. LLC-LENAR-08 a phase I/II study lenalidomide-rituximab in relapse/refractory chronic lymphocytic leukemia. Haematologica 2015; 100(s1); P217.
- O'Brien S et al. Early clinical activity and pharmacodynamic effects of duvelisib, a PI3K-delta,gamma inhibitor, in patients with treatment-na. Haematologica 2015; 100(s1); S434.
- Moskowitz CH et al. Brentuximab vedotin as consolidation therapy after autologous stem-cell transplantation in patients with Hodgkin's lymphoma at risk of relapse or progression (AETHERA): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2015; 385: 1853-1862.
- Walewski J et al. Multivariate analysis of PFS from the aethera trial: a phase 3 study of brentuximab vedotin consolidation after autologous stem cell transplant for HL. Haematologica 2015; 100(s1); S807.
- Böll B et al. German hodgkin study group phase I trial of doxorubicin, vinblastine, dacarbazine, and lenalidomide (AVD-REV) for elderly hodgkin lymphoma patients - Final analysis. Haematologica 2015; 100(s1); S805.
- Bildnachweis: „riesenrad in wien”: © photo 5000/Fotolia