ASH 2015
5. bis 8. Dezember, Orlando
Multiples Myelom: Neue Substanzen und bewährte Therapiestrategien ergänzen sich
Maligne Lymphome: Neue Substanzen und differenzierte Diagnostik auf dem Weg zur klinischen Routine
 Neue Substanzen, neue Wirkmechanismen, zielgerichtete Therapieansätze und Modifikationen bewährter Therapiestrategien – das waren wichtige Schwerpunkte der Vorträge und Präsentationen auf der 57. Jahrestagung der American Society of Hematology (ASH), die vom 5. bis 8. Dezember 2015 in Orlando stattfand.
Neue Substanzen, neue Wirkmechanismen, zielgerichtete Therapieansätze und Modifikationen bewährter Therapiestrategien – das waren wichtige Schwerpunkte der Vorträge und Präsentationen auf der 57. Jahrestagung der American Society of Hematology (ASH), die vom 5. bis 8. Dezember 2015 in Orlando stattfand.
Aktuelle Daten und Fakten zu den Themen Multiples Myelom, AML/MDS und Lymphome finden Sie hier in unserem Überblick vom ASH-Kongress 2015.
Liebe Kolleginnen und Kollegen,
auf dem diesjährigen Jahreskongress der American Society of Hematology (ASH), der vom 5. bis 8. Dezember im US-amerikanischen Orlando stattfand, trafen sich internationale Experten aus der Hämatologie und Hämatoonkologie zum alljährlichen Wissens- und Erfahrungsaustausch. Wir möchten Ihnen in unseren Berichten einen Überblick über die neuen Entwicklungen aus den Bereichen Multiples Myelom, Myelodysplastische Syndrome/akute myeloische Leukämie und Lymphome geben.
Den Fokus haben wir dabei auf die Relevanz der präsentierten Daten für die praktische Arbeit in Klinik und Praxis gelegt und die neu gewonnenen wissenschaftlichen Fakten für eine Anwendung am Patientenbett aufbereitet.
Wir wünschen Ihnen ein inspirierendes Leseerlebnis und freuen uns über Ihr Interesse.
Mit kollegialen Grüßen
 Priv.-Doz. Dr. med. Georg Heß, Universitätsmedizin Mainz
Priv.-Doz. Dr. med. Georg Heß, Universitätsmedizin Mainz Dr. med. Hans Salwender, Asklepios Kliniken Hamburg, Altona und St. Georg
Dr. med. Hans Salwender, Asklepios Kliniken Hamburg, Altona und St. Georg Dr. med. Thomas Schroeder, Universitätsklinikum Düsseldorf
Dr. med. Thomas Schroeder, Universitätsklinikum DüsseldorfMultiples Myelom: Neue Substanzen und bewährte Therapiestrategien ergänzen sich
Dr. med. Hans Salwender, Asklepios Kliniken Hamburg, Altona und St. Georg
 In den vergangenen 12 Monaten haben sich die Möglichkeiten der Behandlung des Multiplen Myeloms (MM) gravierend geändert. Zwischen den Jahren 2000 und 2013 hatten wir zur Behandlung des MM neben den „alten“ Alkylantien und Glukokortikoiden im Wesentlichen drei „neue“ Substanzen: Thalidomid, Lenalidomid (welches zunehmend Thalidomid ersetzt) und Bortezomib. Seit 2013 kamen 6 weitere Substanzen hinzu, mit teilweise vollkommen neuen Wirkmechanismen.
In den vergangenen 12 Monaten haben sich die Möglichkeiten der Behandlung des Multiplen Myeloms (MM) gravierend geändert. Zwischen den Jahren 2000 und 2013 hatten wir zur Behandlung des MM neben den „alten“ Alkylantien und Glukokortikoiden im Wesentlichen drei „neue“ Substanzen: Thalidomid, Lenalidomid (welches zunehmend Thalidomid ersetzt) und Bortezomib. Seit 2013 kamen 6 weitere Substanzen hinzu, mit teilweise vollkommen neuen Wirkmechanismen.
Als Erstes wurde Pomalidomid (IMiD der 3. Generation) bereits vor ca. 2 Jahren in Deutschland zugelassen. Dann erschienen in diesem Jahr eine Reihe mit Erfolg abgeschlossener Phase-III-Studien, die zur Zulassung von 5 weiteren Substanzen in Deutschland oder den USA führten, die meisten in den letzten Wochen:
Panobinostat: ein Histondeacetylase-Inhibitor, der vor wenigen Monaten in Deutschland zugelassen wurde (PANORAMA-1-Studie: Panobinostat plus Bortezomib/Dexamethason (VD) vs. VD allein im 1.–3. Rezidiv) [1].
Carfilzomib: ein i.v.-Proteasominhibitor der 2. Generation, aktuelle Zulassung in Deutschland (ASPIRE-Studie: Carfilzomib plus Lenalidomid/Dexamethason (Rd) vs. Rd allein im 1.–3. Rezidiv) [2].
Elotuzumab: ein SLAMF7-Antikörper, Zulassung in den USA, in Deutschland verfügbar (ELOQUENT-2-Studie: ERd vs. Rd im 1.–3. Rezidiv) [3].
Daratumumab: ein CD38-Antikörper, Zulassung in den USA (SIRIUS- [4] und GEN501- [5] Studien: Daratumumab-Monotherapie ab dem 3. Rezidiv) [6].
Ixazomib: der erste orale Proteasominhibitor (TOURMALINE-MM1-Studie: IRd vs. Rd im 1.–3. Rezidiv) [7].
Bis auf die TOURMALINE-MM1-Studie, die für Ixazomib/Lenalidomid/Dexamethason (IRd) bei Patienten mit rezidiviertem/refraktärem MM einen Vorteil des progressionsfreien Überlebens von 6 Monaten (20,6 vs. 14,7 Monate) im Vergleich zu Rd gezeigt hatte (bei Unabhängigkeit der Wirksamkeit von genetischen Veränderungen) [7], waren die oben genannten Studien spätestens seit den ASCO/EHA-Meetings im Juni bekannt.
Was konnte der diesjährige ASH-Kongress noch Neues bringen?
Zum einen neue Kombinationsstudien, die aber oftmals nur über geringe Fallzahlen verfügten. Außerdem Updates mit längerer Nachbeobachtungszeit, sowie eine ganze Reihe interessanter – weil klinisch wichtiger – Subgruppenanalysen. Hier sei zum Beispiel die Analyse der Pomalidomid/Dexamethason-Therapie bei Patienten mit Niereninsuffizienz erwähnt, aber auch Analysen zu verschiedenen genetischen Risikogruppen, gebrechlichen Patienten oder zu unterschiedlichen Vortherapien.
Großen Raum nahm auch die Diskussion zur Untersuchung auf minimale Resterkrankung und zur Frage nach dem Stellenwert der Hochdosistherapie und autologen Stammzelltransplantation im Lichte der großen Erfolge mit den oben genannten neuen Substanzen ein.
Daratumumab-Monotherapie bei stark vorbehandelten MM-Patienten
Sehr interessant war die Präsentation von Usmani, in der die Daten von zwei Studien (SIRIUS, GEN501) zur Daratumumab-Monotherapie bei stark vorbehandelten MM-Patienten kombiniert wurden [6]. Trotz im Median fünf Vorbehandlungen (mehr als drei Vortherapien bei 76 % der Patienten) und Refraktärität gegenüber den meisten zur Verfügung stehenden Substanzen (84 % Bortezomib, 84 % Lenalidomid, 39 % Carfilzomib, 55 % Pomalidomid) zeigten die 148 Patienten ein Ansprechen von 31 % und – noch viel bemerkenswerter – ein medianes Überleben von 19,9 Monaten (Abb. 1). Und dies mit einer Monotherapie eines relativ gut verträglichen Antikörpers. Hier bietet sich eine Reihe von Kombinationsmöglichkeiten, die derzeit in mehreren Studien getestet werden.
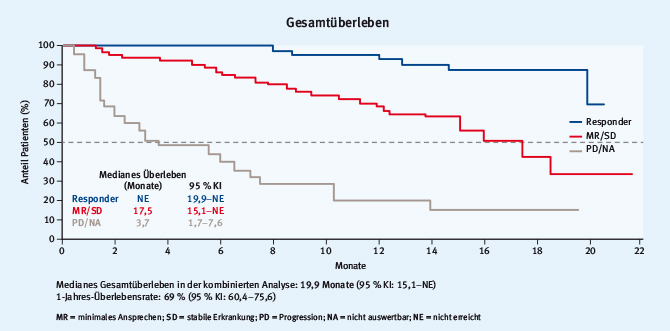 Abb. 1: Gesamtüberleben mit einer Daratumumab-Monotherapie bei stark vorbehandelten MM-Patienten. Daten aus den SIRIUS- und GEN501-Studien (modifiziert nach [6]).
Abb. 1: Gesamtüberleben mit einer Daratumumab-Monotherapie bei stark vorbehandelten MM-Patienten. Daten aus den SIRIUS- und GEN501-Studien (modifiziert nach [6]).Fazit
- Daratumumab führte bei stark vorbehandelten MM-Patienten zu einem Ansprechen von 31 % und einem medianen Überleben von 19,9 Monaten – bei relativ guter Verträglichkeit.
Elotuzumab beim rezidivierten/refraktären Multiplen Myelom
Im Update der ELOQUENT-2-Studie [8] zeigte sich bei der Hinzunahme des Antikörpers Elotuzumab zu Rd im Vergleich zu Rd – trotz nur moderatem absolutem Unterschied im 3-Jahres-PFS von 8 % – ein signifikanter Unterschied in der Zeit bis zur nächsten Behandlung von im Median 1 Jahr. Das ist ein Hinweis auf weniger aggressive Rezidive nach einer Vorbehandlung mit dieser Immuntherapie. Ein wichtiger Punkt bei der Therapie mit diesem Antikörper ist die geringe Rate an Nebenwirkungen, die nun erneut bestätigt wurde.
Fazit
- Die Kombination aus Elotuzumab und Rd führte im Vergleich mit Rd zu einer Verlängerung der Zeit bis zur nächsten Behandlung von einem Jahr.
Pomalidomid bei MM-Patienten mit Niereninsuffizienz
Eine klinisch sehr wichtige Subgruppenanalyse erbrachte Daten zu Pomalidomid bei Patienten mit Niereninsuffizienz (NI) [9] .Bei dieser Zwischenanalyse der MM-013-Studie wurden die bisher 47 Patienten in 3 Gruppen eingeteilt: Patienten mit moderater NI, mit schwerer NI ohne Dialysepflichtigkeit und mit schwerer NI mit Dialysepflichtigkeit. Unabhängig von der Schwere der NI konnte in allen drei Gruppen die Therapie mit der Standarddosis 4 mg pro Tag bei ähnlicher Plasmakonzentration durchgeführt werden. Die Rate an Nebenwirkungen im Dialyse-Arm war zwar höher, entspricht aber auch der weiter fortgeschrittenen Erkrankung der Patienten. Somit gilt die Empfehlung, Patienten unabhängig von der NI zu Beginn mit 4 mg/d Pomalidomid zu behandeln.
Fazit
- Auch bei Patienten mit fortgeschrittener Niereninsuffizienz kann Pomalidomid in einer Anfangsdosierung von 4 mg pro Tag eingesetzt werden.
Kontinuierliche Gabe von Lenalidomid/Dexamethason (Rd) bei gebrechlichen MM-Patienten
Eine weitere wichtige Frage für die Routinebetreuung von Patienten ist, ob auch gebrechliche Patienten kontinuierlich mit Rd behandelt werden können, oder ob mit Melphalan/Prednison/Thalidomid (MPT) auf eine Kombination ohne Dexamethason ausgewichen werden sollte. Hierzu präsentierte Facon eine Subgruppenanalyse der FIRST-Studie (Erstlinientherapie bei älteren Patienten mit kontinuierlich Rd vs. MPT), getrennt nach fitten, wenig fitten und gebrechlichen Patienten [10]. Darin profitierten auch die gebrechlichen Patienten von einer kontinuierlichen Rd-Therapie als Erstlinienbehandlung (Verlängerung des PFS um 21 %, Verlängerung des Gesamtüberlebens [OS] um 20 % im Vergleich zu MPT). In einer anderen Subgruppenanalyse zu dieser Studie konnte Avet-Loiseau zeigen, dass Patienten mit günstiger Zytogenetik den größten Nutzen von einer kontinuierlichen Rd-Therapie bis zum Progress gegenüber MPT haben [11]. Patienten mit ungünstiger Genetik (del(17p), t(4;14)) profitieren weit weniger.
Fazit
- Auch gebrechliche Patienten profitieren hinsichtlich PFS und OS von einer kontinuierlichen Therapie mit Lenalidomid/Dexamethason (Rd).
Lenalidomid/Dexamethason (Rd) plus Bortezomib
Im Lichte der Möglichkeiten der neuen Medikamente war eine Studie besonders beeindruckend, da sie das Potential der mittlerweile älteren Substanzen aufzeigte. Nachdem 2008 eine Phase-II-Studie von Richardson eine sehr gute Ansprechrate auf eine Kombination aus Rd mit Bortezomib gezeigt hatte [12], folgten nun die Daten der entsprechenden Phase-III-Studie bei Patienten mit neu diagnostiziertem MM, bei denen zunächst keine Hochdosistherapie geplant war [13]. Die Patienten erhielten am Anfang entweder Bortezomib + Rd (VRd) oder nur Rd über 24 Wochen und anschließend eine Erhaltungstherapie mit Rd bis zum Progress. Durch die Hinzunahme von Bortezomib wurde das PFS von 30 auf 43 Monate verlängert (p = 0,0018) und das Gesamtüberleben von 64 auf 75 Monate (p = 0,025) (Abb. 2). Das mediane Follow-up der 525 Patienten betrug 55 Monate. Die Rate an neurologischen Nebenwirkungen (NW) vom Grad 3 oder höher war zwar mit 11 % vs. 33 % und die der gastrointestinalen NW mit 8 % vs. 22 % beim Vergleich Rd ohne bzw. mit Bortezomib erhöht. Bortezomib wurde aber in dieser Studie noch intravenös eingesetzt. Es sollte heutzutage jedoch nicht mehr i.v. sondern nur noch s.c. verabreicht werden.
Fazit
- Neu diagnostizierte MM-Patienten, bei denen zunächst keine Hochdosistherapie geplant ist, profitieren hinsichtlich PFS und OS von einer Hinzunahme von Bortezomib über 24 Wochen zu einer kontinuierlichen Therapie mit Lenalidomid/Dexamethason (Rd).
„Die Hinzunahme von Bortezomib zu Rd verbessert das Therapieergebnis bei neu diagnostizierten MM-Patienten, die keine Hochdosistherapie erhalten. Es bleibt zu hoffen, dass die Kostenträger diese Therapie schnell akzeptieren.“ Dr. Hans Salwender
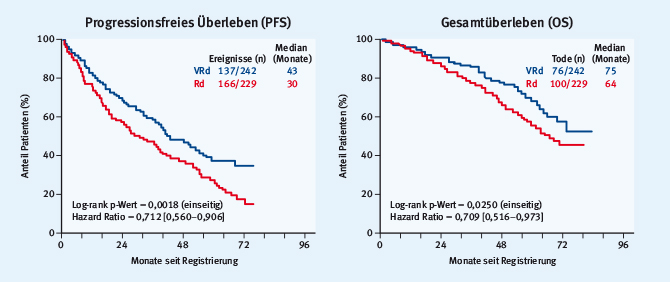 Abb. 2: Bortezomib + Rd (VRd) vs. Rd bei Patienten mit neu diagnostiziertem MM: besseres progressionsfreies Überleben (PFS) und Gesamtüberleben (OS) durch Hinzunahme von Bortezomib (modifiziert nach [13]).
Abb. 2: Bortezomib + Rd (VRd) vs. Rd bei Patienten mit neu diagnostiziertem MM: besseres progressionsfreies Überleben (PFS) und Gesamtüberleben (OS) durch Hinzunahme von Bortezomib (modifiziert nach [13]).Stellenwert der Hochdosistherapie
Bei diesen spektakulären Daten mit optimiert verabreichten älteren oder neuen Substanzen stellt sich die Frage, ob Chemotherapie – insbesondere die Hochdosis-Chemotherapie – für die Behandlung von Myelompatienten überhaupt noch benötigt wird. Kurz gesagt: alle bisherigen Daten sprechen dafür.
Attal präsentierte Daten der IFM-2009-Studie [14], in der die oben genannte hochwirksame Therapie aus Lenalidomid, Bortezomib und Dexamethason (RVD) über 8 Zyklen verglichen wurde mit 5 Zyklen RVD plus Hochdosis-Melphalan und autologer Stammzelltransplantation (ASZT), jeweils gefolgt von einem Jahr Lenalidomid-Erhaltungstherapie. Die 764 Patienten wurden von 11/2010 bis 11/2012 in die Studie eingebracht. Nach der Analyse der Daten in der zweiten geplanten Interimsanalyse mit einem medianen Follow-up von 39 Monaten empfahl das unabhängige Datamonitorboard, die Studie wegen Überlegenheit der Hochdosistherapie abzubrechen. Die Remissionsraten für komplette Remission (CR), sehr gutes partielles Ansprechen (VGPR) oder besser und Negativität für minimale Resterkrankung (MRD) waren im Hochdosisarm signifikant um 10 % (CR), 15 % (VGPR) bzw. 15 % (MRD-negativ) höher. Ebenso zeigte sich ein signifikant besseres PFS (4-Jahres-PFS 47 % vs. 35 %) (Abb. 3). Das OS war erwartungsgemäß in beiden Therapiearmen mit über 80 % noch hoch, ohne einen signifikanten Unterschied.
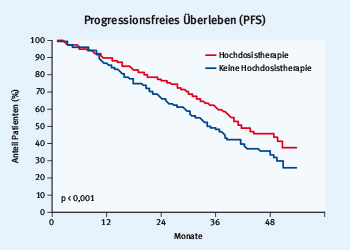 Abb. 3: Besseres progressionsfreies Überleben (PFS) nach Lenalidomid, Bortezomib und Dexamethason (RVD) mit Hochdosis-Melphalan und autologer Stammzelltransplantation (ASZT) im Vergleich zu ohne Hochdosistherapie und ASZT (modifiziert nach [14]).
Abb. 3: Besseres progressionsfreies Überleben (PFS) nach Lenalidomid, Bortezomib und Dexamethason (RVD) mit Hochdosis-Melphalan und autologer Stammzelltransplantation (ASZT) im Vergleich zu ohne Hochdosistherapie und ASZT (modifiziert nach [14]).Vergleichbare Daten zeigte auch eine italienische Studie von Gay, in der die Patienten nach einer Induktionstherapie mit Rd randomisiert entweder mit 6 Zyklen Lenalidomid/Cyclophosphamid/Dexamethason oder mit 2 Zyklen Hochdosis-Melphalan und ASZT behandelt wurden [15]. Alle Patienten erhielten anschließend eine Erhaltungstherapie mit Lenalidomid. Mit einem medianen Follow-up von 47 Monaten war das PFS im Hochdosisarm signifikant mit 43,3 vs. 28,6 Monaten verlängert (p < 0,001) und die 4-Jahres-OS-Rate von 73 % auf 86 % erhöht (p = 0,004). Auch in dieser Studie war die Rate MRD-negativer Patienten im Hochdosisarm mit 48 % vs. 28 % höher.
Sonneveld [16] präsentierte das 91-Monats-Update der GMMG/HOVON-Studie zu neu diagnostizierten, jungen Patienten. In dieser Studie erhielten die Patienten randomisiert entweder eine Induktion mit Vincristin/Adriamycin/Dexamethason (VAD), einmalige (HOVON) oder zweimalige (GMMG) Hochdosis-Melphalan-Behandlung mit ASZT und eine Erhaltungstherapie mit Thalidomid oder eine Induktion mit Bortezomib/Adriamycin/Dexamethason (PAD), Hochdosistherapie + ASZT wie oben beschrieben und eine Erhaltungstherapie mit Bortezomib über zwei Jahre. Grundsätzlich war die bortezomibhaltige Therapie bezüglich des Überlebens überlegen, der beeindruckendste Vorteil zeigte sich jedoch bei Patienten mit del(17p) oder einer Niereninsuffizienz bei Behandlungsbeginn. Der Nutzen für Patienten mit del(17p) hatte sich zwar bereits bei der ersten Publikation angedeutet, wurde aber nun – mit fast 8 Jahren Follow-up – eindrucksvoll bestätigt. Selbst nach dieser langen Zeit zeigte sich kein signifikanter Unterschied im Gesamtüberleben für Patienten mit oder ohne del(17p) (Abb. 4). Für die Gesamtgruppe der Patienten, die mit PAD-Induktion behandelt wurden, zeigte sich ein signifikanter Gesamtüberlebensvorteil nach 8 Jahren für die Doppeltransplantation im Vergleich zur einmaligen Transplantation (55 % vs. 42 % nach 96 Monaten; p = 0,018).
Fazit
- Auch in Zeiten neuer hochwirksamer Substanzen ist die Hochdosis-Chemotherapie (HD) mit nachfolgender autologer Stammzelltransplantation (ASZT) in der Lage, die Remissionsrate signifikant weiter zu erhöhen, die Remissionstiefe weiter zu verbessern und das progressionsfreie Überleben zu verlängern.
- Vom Einbezug von Bortezomib in Induktions- und Erhaltungstherapie einer ASZT profitieren insbesondere Patienten mit del(17p) oder mit einer Niereninsuffizienz, deren Überleben nicht mehr signifikant schlechter ist als das der Patienten mit Standardrisiko.
„Für Patienten mit del(17p) ist das beschriebene bortezomibhaltige Therapieregime mit PAD-Induktion, Hochdosis-Melphalan + ASZT und Bortezomib-Erhaltungstherapie als Standardtherapie zu betrachten.“ Dr. Hans Salwender
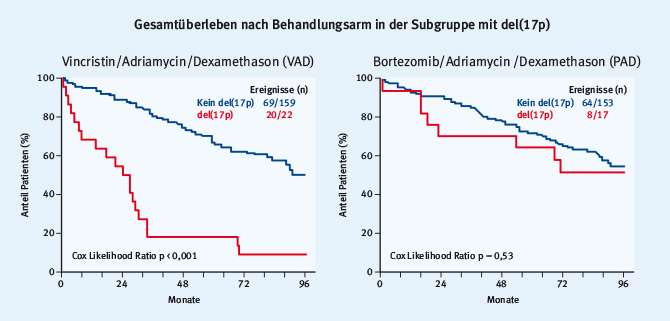 Abb. 4: Gesamtüberleben in der Subgruppe der Patienten mit del(17p): kein signifikanter Unterschied im Gesamtüberleben für Patienten mit oder ohne del(17p) in der Gruppe, die Bortezomib/Adriamycin/Dexamethason erhielt (PAD) (rechts) (modifiziert nach [16]).
Abb. 4: Gesamtüberleben in der Subgruppe der Patienten mit del(17p): kein signifikanter Unterschied im Gesamtüberleben für Patienten mit oder ohne del(17p) in der Gruppe, die Bortezomib/Adriamycin/Dexamethason erhielt (PAD) (rechts) (modifiziert nach [16]).Minimale Resterkrankung (MRD)
Zur MRD-Analyse nutzen verschiedene Arbeitsgruppen unterschiedliche Ansätze (zum Beispiel [17,18,19, 20]). Die hierzu präsentierten Daten sind beeindruckend, denn diese Gruppen sind in der Lage, eine residuelle Plasmazelle unter 10 hoch 6 Zellen aus dem Knochenmarkblut zu detektieren.
Das Problem ist, dass auch auf diesem Level immer noch Tausende von Plasmazellen vorhanden sein können. Zusammenfassend kann festgehalten werden, dass im Wesentlichen alle Untersuchungen erwartungsgemäß zeigten, dass die Reduktion der Tumorlast bzw. der Anzahl der Plasmazellen unterhalb der entsprechenden Nachweisgrenze die Prognose (hoch-)signifikant verbessert.
Es gibt jedoch Schwierigkeiten, diese Verfahren in die klinische Praxis einzuführen. Denn zum einen haben die meisten Arbeitsgruppen eigene Methoden zur Bestimmung der minimalen Resterkrankung, sodass keine Vereinheitlichung und keine direkte Vergleichbarkeit bestehen. Zum anderen stellt sich das Problem der allgemeinen Verfügbarkeit. Denn wenn diese Untersuchungen nur an einzelnen Zentren durchführbar sind, besteht beispielsweise das Risiko der Probenalterung auf dem Transport, mit – je nach Methode – der Gefahr verfälschter Ergebnisse. Weitere grundsätzliche Probleme sind, dass Untersuchungen, die auf Knochenmark(blut) basieren, einen aggressiven, extramedullären Progress nicht erfassen.
Auch gibt es bisher keine prospektiven Daten zu einem responseadaptierten Vorgehen. In einer aktuellen Studie der Deutschen Studiengruppe Multiples Myelom (DSMM) [21] wurden zwar die Patienten verschiedenen Behandlungen zugewiesen, je nachdem, ob sie eine VGPR erreicht hatten oder nicht (wobei eine VGPR weit von einer MRD entfernt ist). Aber noch nicht einmal auf dem Niveau der VGPR mit einem Rückgang des monoklonalen Proteins um gerade mal den Faktor 10 hoch 1, ist das beste Vorgehen prospektiv belegt. Verschiedene Gruppen leiten zum Beispiel ihre Empfehlung, eine zweite Hochdosistherapie nur bei Nichterreichen einer VGPR durchzuführen, von der IFM94-Studie aus Frankreich ab. Die Ergebnisse bezüglich der VGPR-Subgruppe – retrospektiv analysiert – wurde bereits vor über 10 Jahren publiziert [22].
Fazit
- Eine MRD-Negativität bei MM-Patienten verbessert zwar die Prognose, eine therapeutische Konsequenz ergibt sich daraus momentan aber nicht.
„Solange die meisten Empfehlungen dahingehen, dass man bei Erreichen einer VGPR oder bei immunfixationspositiver CR die Therapie stoppt, indem zum Beispiel keine zweite Hochdosistherapie durchgeführt wird, ist die Bestimmung der MRD eher von akademischem Interesse. Wir brauchen dringend prospektive Daten über den Nutzen einer Weiterbehandlung bei MRD-positiven Patienten.“ Dr. Hans Salwender
Quellen
- San-Miguel JF, Hungria VT, Yoon SS et al. Panobinostat plus bortezomib and dexamethasone versus placebo plus bortezomib and dexamethasone in patients with relapsed or relapsed and refractory multiple myeloma: a multicentre, randomised, double-blind phase 3 trial. Lancet Oncol 2014; 15: 1195-1206.
- Stewart AK, Rajkumar SV, Dimopoulos MA et al. Carfilzomib, lenalidomide, and dexamethasone for relapsed multiple myeloma. N Engl J Med 2015; 372: 142-152.
- Lonial S, Dimopoulos M, Palumbo A et al. Elotuzumab Therapy for Relapsed or Refractory Multiple Myeloma. N Engl J Med 2015; 373: 621-631.
- Lonial S, Weiss BM, Usmani SZ et al. Phase II study of daratumumab (DARA) monotherapy in patients with >= 3 lines of prior therapy or double refractory multiple myeloma (MM): 54767414MMY2002 (Sirius). J Clin Oncol 33, 2015 (suppl; abstr LBA8512).
- Lokhorst HM, Plesner T, Laubach JP et al. Targeting CD38 with Daratumumab Monotherapy in Multiple Myeloma. N Engl J Med 2015; 373: 1207-1219.
- Usmani S, Weiss B, Bahlis N et al. Clinical Efficacy of Daratumumab Monotherapy in Patients with Heavily Pretreated Relapsed or Refractory Multiple Myeloma. ASH 2015, Orlando, abstract 29.
- Moreau P, Masszi T, Grzasko N et al. Ixazomib, an Investigational Oral Proteasome Inhibitor (PI), in Combination with Lenalidomide and Dexamethasone (IRd), Significantly Extends Progression-Free Survival (PFS) for Patients (Pts) with Relapsed and/or Refractory Multiple Myeloma (RRMM): The Phase 3 Tourmaline-MM1 Study (NCT01564537). ASH 2015, Orlando, abstract 727.
- Dimopoulos M, Lonial S, White D et al. Eloquent-2 Update: A Phase 3, Randomized, Open-Label Study of Elotuzumab in Combination with Lenalidomide/Dexamethasone in Patients with Relapsed/Refractory Multiple Myeloma - 3-Year Safety and Efficacy Follow-up. ASH 2015, Orlando, abstract 28
- Ramasamy K, Dimopoulos A, van de Donk N et al. Safety of Treatment (Tx) with Pomalidomide (POM) and Low-Dose Dexamethasone (LoDEX) in Patients (Pts) with Relapsed or Refractory Multiple Myeloma (RRMM) and Renal Impairment (RI), Including Those on Dialysis. Presented at ASH 2015, Orlando, abstract 374.
- Facon T, Hulin C, Dimopoulos M et al. A Frailty Scale Predicts Outcomes of Patients with Newly Diagnosed Multiple Myeloma Who Are Ineligible for Transplant Treated with Continuous Lenalidomide Plus Low-Dose Dexamethasone on the First Trial. ASH 2015, Orlando, abstract 4239.
- Avet-Loiseau H, Hulin C, Benboubker L et al. Impact of Cytogenetics on Outcomes of Transplant-Ineligible Patients with Newly Diagnosed Multiple Myeloma Treated with Continuous Lenalidomide Plus Low-Dose Dexamethasone in the FIRST (MM-020) Trial. ASH 2015, Orlando, abstract 730.
- Richardson PG, Weller E, Lonial S et al. Lenalidomide, bortezomib, and dexamethasone combination therapy in patients with newly diagnosed multiple myeloma. Blood 2010; 116: 679-686.
- Durie B, Hoering A, Rajkumar S et al. Bortezomib, Lenalidomide and Dexamethasone Vs. Lenalidomide and Dexamethasone in Patients (Pts) with Previously Untreated Multiple Myeloma without an Intent for Immediate Autologous Stem Cell Transplant (ASCT): Results of the Randomized Phase III Trial SWOG S0777. Presented at ASH 2015, Orlando, abstract 25.
- Attal M, Lauwers-Cances V, Hulin C et al. Autologous Transplantation for Multiple Myeloma in the Era of New Drugs: A Phase III Study of the Intergroupe Francophone Du Myelome (IFM/DFCI 2009 Trial). Presented at ASH 2015, Orlando, abstract 391.
- Gay F, Magarotto V, Petrucci M et al. Autologous Transplantation Versus Cyclophosphamide-Lenalidomide-Prednisone Followed By Lenalidomide-Prednisone Versus Lenalidomide Maintenance in Multiple Myeloma: Long-Term Results of a Phase III Trial. ASH 2015, Orlando, abstract 392.
- Sonneveld P, Salwender H, Van Der Holt B et al. Bortezomib Induction and Maintenance in Patients with Newly Diagnosed Multiple Myeloma: Long-Term Follow-up of the HOVON-65/GMMG-HD4 Trial. ASH 2015, Orlando, abstract 27.
- Avet-Loiseau H, Corre J, Lauwers-Cances V et al. Evaluation of Minimal Residual Disease (MRD) By Next Generation Sequencing (NGS) Is Highly Predictive of Progression Free Survival in the IFM/DFCI 2009 Trial. ASH 2015, Orlando, abstract 191.
- Moreau P, Attal M, Karlin L et al. Prospective Evaluation of MRI and PET-CT at Diagnosis and before Maintenance Therapy in Symptomatic Patients with Multiple Myeloma Included in the IFM/DFCI 2009 Trial. ASH 2015, Orlando, abstract 395.
- Flores-Montero J, Paiva B, Sanoja-Flores L et al. Next Generation Flow (NGF) for High Sensitive Detection of Minimal Residual Disease (MRD) in Multiple Myeloma (MM). ASH 2015, Orlando, abstract 367.
- Arana P, Paiva B, Vidriales M et al. Comparison Between First-Generation 4-Color Vs. Second-Generation 8-Color Multiparameter Flow Cytometry (MFC) to Monitor Minimal Residual Disease (MRD) in Multiple Myeloma (MM). ASH 2015, Orlando, abstract 2963.
- Lenalidomid, Adriamycin, Dexamethason (RAD) versus Lenalidomid, Bortezomib, Dexamethason (VRD) als Induktionstherapie für Patienten mit neu diagnostiziertem Multiplem Myelom gefolgt von einer an das Ansprechen angepassten Konsolidierung und Lenalidomid Erhaltung - eine randomisierte, multizentrische Phase-III-Studie der Deutschen Studiengruppe Multiples Myelom (DSMM XIV). Verfügbar unter http://kml.clinicalsite.org/de/cat/508/trial/1926; abgerufen am 16.12.2015.
- Attal M, Harousseau JL, Facon T et al. Single versus double autologous stem-cell transplantation for multiple myeloma. N Engl J Med 2003; 349: 2495-2502.
- Bildnachweis: „Orange County Convention Center in Orlando”: © Nataliya Hora/Fotolia; "Lake Eola Fountain": © Faded Beauty/Fotolia
Akute myeloische Leukämien und Myelodysplastische Syndrome – zielgerichtete Therapieansätze rücken näher
Dr. med. Thomas Schroeder, Universitätsklinikum Düsseldorf
 In den vergangenen Jahren stand die molekulare Charakterisierung der myeloischen Neoplasien im Vordergrund der Erforschung myelodysplastischer Syndrome (MDS). Hiermit wurde zunächst versucht, neue Risikoklassifikationen und Prognosesysteme zu definieren beziehungsweise vorhandene zu optimieren. Wie stellvertretend durch Rafael Bejar in einer Arbeit der International Working Group-MDS gezeigt [1], gestaltet sich dies jedoch als komplex und ist noch nicht alltagstauglich.
In den vergangenen Jahren stand die molekulare Charakterisierung der myeloischen Neoplasien im Vordergrund der Erforschung myelodysplastischer Syndrome (MDS). Hiermit wurde zunächst versucht, neue Risikoklassifikationen und Prognosesysteme zu definieren beziehungsweise vorhandene zu optimieren. Wie stellvertretend durch Rafael Bejar in einer Arbeit der International Working Group-MDS gezeigt [1], gestaltet sich dies jedoch als komplex und ist noch nicht alltagstauglich.
Im Gegensatz hierzu machen – so das Fazit des diesjährigen ASH – zielgerichtete Therapien raschere Fortschritte. Während auf dem Gebiet der Hochrisiko-MDS noch keine neue Therapie in Sicht ist, zielen die Therapiestrategien beim Niedrigrisiko-MDS auf die Stimulation der Erythropoese und der Thrombopoese ab.
Bei den akuten myeloischen Leukämien richtet sich die Therapie mittlerweile direkt gegen den malignen Zellklon, indem genetische Veränderungen wie die IDH- und FLT3-Mutationen mit sogenannten „small molecules“ zielgerichtet angegangen werden. Dabei sind die Ergebnisse so vielversprechend, dass hier unter Umständen in den kommenden Jahren seit längerer Zeit neue Medikamente zur AML-Behandlung zugelassen werden könnten.
Verbesserung der Erythropoese als Ziel der MDS-Behandlung mit Luspatercept
Das pathophysiologische Verständnis der MDS ist in den vergangenen Jahren stetig gewachsen. Im Gegensatz hierzu liegt es mittlerweile 9 Jahre zurück, dass mit Azacitidin und Lenalidomid zunächst in Amerika und dann zeitversetzt in Europa letztmalig Substanzen mit pathophysiologischem Wirkansatz zur MDS-Behandlung zugelassen wurde. Angesichts dessen stellt sich die Frage, ob und wann die neuen wissenschaftlichen Erkenntnisse den „Bench to bedside“-Transfer ermöglichen und zu neuen Behandlungsformen führen:
Am weitesten fortgeschritten auf diesem Weg ist die Substanz Luspatercept (ACE-536), die darauf abzielt, die Erythropoese bei MDS-Patienten zu verbessern. Luspatercept ist ein Fusionsprotein, das aus der Rezeptordomäne des Activin-Rezeptor IIb und einem Fc-Teil des humanen IgG besteht und seine Wirkung durch ein sog. „ligand-trapping“ vermittelt, indem inhibitorische Signalmoleküle der TGF-beta-Familie wie GDF-11 im Knochenmarkmikromilieu gebunden werden. Erste klinische Resultate einer Dosiseskalationsstudie waren bereits auf dem letzten ASH gezeigt worden [2]. In einem aktuellen Beitrag wurden die Resultate der 32 von insgesamt 58 Niedrigrisiko-MDS-Patienten (IPSS low und intermediate-1) präsentiert, die nach der dreimonatigen Dosiseskalationsphase in eine bis zu 24-monatige Extensionsphase übergingen [3]. Wie schon in der Dosiseskalationsstudie konnten nur Patienten eingeschlossen werden, die entweder einen Serum-EPO-Spiegel > 500 U/l aufwiesen oder auf eine EPO-Therapie nicht angesprochen bzw. diese nicht vertragen hatten. Bei Patienten mit geringem Transfusionsbedarf (definiert als weniger als vier Erythrozytenkonzentrate/8 Wochen, Hb < 10 g/dl) konnte durch die Therapie mit Luspatercept bei 69 % (n = 9/13) der primäre Studienendpunkt des hämatologischen Ansprechens (Hb-Anstieg > 1,5 g/dl für mindestens 8 Wochen) erreicht werden. Ähnlich sah es bei den Patienten mit hohem Transfusionsbedarf (definiert als >= 4 Erythrozytenkonzentrate/8 Wochen) bei Studieneinschluss aus. Von diesen zeigten 68 % (n = 13/19) ein Ansprechen der Erythropoese (Reduktion des Transfusionsbedarfes um >= 4 Einheiten oder >= 50 % für mindestens 8 Wochen). Eine mindestens 8 Wochen anhaltende Transfusionsfreiheit erreichten 11 von 22 Patienten (50 %), die bei Studieneinschluss transfusionsbedürftig waren (Abb. 1). Erfreulicherweise bestätigten sich auch die Daten hinsichtlich des Nebenwirkungsprofils. Als Ausdruck der guten Verträglichkeit traten keine mit der Studienmedikation zusammenhängenden Grad-3- oder Grad-4-Nebenwirkungen auf. Wenn Nebenwirkungen auftraten, waren es vornehmlich muskuloskeletale Schmerzen und Übelkeit.
Basierend auf diesen vielversprechenden Daten wird Luspatercept nun in einer randomisierten Phase-III-Studie (MEDALIST Trial) bei 210 Niedrigrisiko-MDS-Patienten mit Transfusionsbedarf und Nachweis von Ringsideroblasten placebokontrolliert untersucht. Dies stellt auf dem Weg zu einer Zulassung den nächsten entscheidenden Schritt dar.
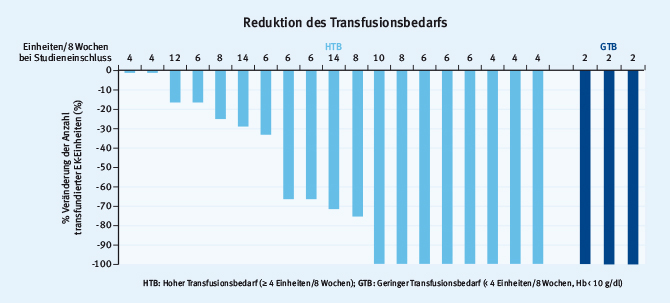 Abb. 1: Reduktion des Transfusionsbedarfs durch eine Therapie mit Luspatercept (modifiziert nach [3]).
Abb. 1: Reduktion des Transfusionsbedarfs durch eine Therapie mit Luspatercept (modifiziert nach [3]).TPO-Analoga und MDS – Neuer Versuch, diesmal mit Eltrombopag
Seit mehreren Jahren werden 2 neue Thrombopoese-stimulierenden Medikamente (TPO-Analoga; TPO = Thrombopoetin) zur Behandlung der Immunthrombopenie erfolgreich eingesetzt. Seit dieser Zeit wird auch versucht, die beiden Substanzen bei Patienten mit MDS und Thrombopenie einzusetzen. Ziel dieser Behandlung ist – vergleichbar mit der Therapie mit erythropoesestimulierenden Substanzen – die bei ca. 10 % der Niedrigrisiko-MDS-Patienten vorliegende Thrombopenie zu verbessern. Eine erste randomisierte Studie mit dem subkutan zu verabreichenden Romiplostim wurde trotz einem besseren Ansprechen als in der Placebogruppe aufgrund von Sicherheitsbedenken vorzeitig abgebrochen. Ursache hierfür war die Sorge vor einer Steigerung der Blastenzahl und der AML-Progression im Romiplostim-Arm [4].
Olivia et al. stellten nun auf dem diesjährigen ASH Daten einer prospektiven, randomisierten Multicenter-Phase-II-Studie vor, in welcher Niedrigrisiko-MDS-Patienten (low und intermediate-1 gemäß IPSS) und Thrombopenie (< 30.000/μl) mit dem oralen Thrombopoese-stimulierenden Agens Eltrombopag behandelt wurden [5]. Bis zum Zeitpunkt dieser ersten Interimsanalyse wurden 70 Patienten in die Studie eingeschlossen, von denen 46 Eltrombopag (mediane Dosis 75 mg einmal täglich) und 24 Placebo erhielten. Nach 24 Wochen sprachen insgesamt 54 % der zu diesem Zeitpunkt noch in der Studie befindlichen Patienten (n = 13) im interventionellen Arm auf die Studienmedikation an, während im Placeboarm lediglich 27 % (n = 3) ansprachen (Tab. 1). Der mediane Anstieg der Thrombozyten infolge der Eltrombopag-Einnahme betrug 53.200/μl und die mediane Zeit bis zum Ansprechen betrug 14 Tage. Eltrombopag wurde von der Mehrzahl der Patienten gut vertragen, vereinzelt traten Leberwerterhöhungen und gastrointestinale Nebenwirkungen auf. Als weiterer Endpunkt wurde in der Studie auch die Lebensqualität erfasst: auch hier zeigte sich für Eltrombopag ein Vorteil gegenüber der Placebogruppe.
Im Wissen um die Progress-Problematik, welche zum Ende der Romiplostin-Studie geführt hatte, war es umso erfreulicher, dass keine gesteigerte Progressionsrate im Eltrombopag-Arm zu beobachten war. Daher können mit Spannung die finalen Resultate dieser Studie erwartet werden, die möglicherweise eine weitere Therapieoption hervorbringen.
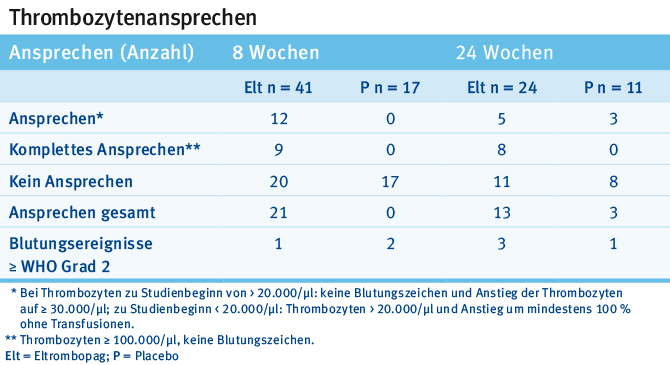 Tab. 1: Ansprechen auf eine Therapie mit Eltrombopag bei MDS-Patienten mit Thrombopenie (modifiziert nach [5]).
Tab. 1: Ansprechen auf eine Therapie mit Eltrombopag bei MDS-Patienten mit Thrombopenie (modifiziert nach [5]).„Luspatercept und Eltrombopag zielen auf eine Verbesserung der insuffizienten Hämatopoese bei MDS-Patienten ab.“ Dr. Thomas Schroeder
Fazit
- Wirksamkeit und Verträglichkeit von Luspatercept wurden erneut bestätigt. Die Substanz wird nun in einer randomisierten Phase-III-Studie bei Niedrigrisiko-MDS-Patienten geprüft.
- Erste Daten einer randomisierten Studie lassen hoffen, dass der Thrombopoese-Stimulator Eltrombopag zukünftig für MDS-Patienten verfügbar sein wird.
Molekulare Therapien bei der AML
Neue Daten zum Isocitrat-Dehydrogenase-2(IDH-2)-Inhibitor AG-221 zur Behandlung von AML-Patienten mit IDH-2-Mutation
Im vergangenen Jahr wurde auf dem ASH das Therapieprinzip der IDH-Inhibition zur Behandlung der AML und die Resultate einer Phase-1/2-Dosiseskalationsstudie mit 73 Patienten vorgestellt [6].
In diesem Jahr wurden nun die Ergebnisse einer Expansionsphase dieser Studie mit insgesamt 209 Patienten mit IDH-2-Mutation (R140Q- oder R172K-Mutation) vorgestellt [7]. Von diesen waren 159 Patienten (76 %) rezidiviert oder refraktär auf im Median 2 Vortherapien und 66 der Patienten (32 %) zum Zeitpunkt der Analyse noch aktiv in der Studie. Die Patienten erhielten 50 bis 650 mg AG-221 pro Tag, wobei die nun festgelegte Dosis im Phase-2-Teil 100 mg/Tag beträgt. In dieser prognostisch ungünstigen, mit einem medianen Alter von 69 Jahren älteren Patientengruppe war der Behandlungserfolg mit einer oral verabreichbaren AML-Monotherapie beachtlich. Die Gesamtansprechrate betrug 38 % (n = 79), wobei der Subtyp der IDH-2-Mutation keinen Einfluss auf das Ansprechen hatte: 27 % der Patienten erreichten eine komplette Remission (18 % komplette Remission [CR], 1 % CR mit inkompletter hämatopoetischer Regeneration [CRi], 1 % CR mit inkompletter Thrombozyten-Regeneration [CRp], 7 % morphologische CR [mCR]) und 11 % eine partielle Remission. Die mittlere Ansprechdauer betrug 6,9 Monate (95 % Konfidenzintervall 4,9–9,7).
Darüber hinaus liefert die Betrachtung der Resultate einige erwähnenswerte teilweise substanzspezifische Aspekte, die bei der Interpretation von Studiendaten bei älteren AML-Patienten bedacht werden müssen: Neben den genannten Ansprechraten erreichten weitere 45 % der Patienten eine Stabilisierung der Erkrankung. Bei 42 % dieser Patienten ging dies mit einem Anstieg der Neutrophilen auf über 1.000/μl und bei 63 % der Patienten mit einem Anstieg der Thrombozyten auf Werte über 25.000/μl einher. Interessanterweise kam es weder bei diesen Patienten noch bei Patienten, die eine komplette Remission erreichten, infolge der Studienmedikation zu einer Elimination des mutationtragenden Klons. Dies zeigt zwei Dinge: Erstens muss nicht zwingend eine komplette Remission erreicht werden, damit die Patienten von einer Therapie wie zum Beispiel mit AG-221 profitieren. Gerade bei älteren AML-Patienten reicht es möglicherweise, wenn eine Stabilisierung der Erkrankung zur Verbesserung der Hämatopoese und damit zu einer Verringerung zytopeniebedingter Komplikationen führt. Zweitens führt AG-221 nicht zur Elimination des malignen Zellklons, sondert führt vor allem zu einer Differenzierung der leukämischen Zellen. Neben der erwünschten Wirkung führte dies auch zu einer spezifischen Nebenwirkung von AG-221: 4 % der Patienten erlitten ein sogenanntes Differenzierungssyndrom, dessen klinisches Bild sich ähnlich wie das nach einer Therapie mit All-Trans-Retinoinsäure (ATRA) bei der akuten Promyelozytenleukämie darstellte und das auf eine Behandlung mit Steroiden reversibel war.
Andere schwerwiegende Nebenwirkungen traten im Zusammenhang mit der Studienmedikation nicht auf. Infolge dieser positiven Ergebnisse wird die Substanz nun in einer randomisierten Phase-3-Studie (IDHENTIFY-Trial) mit konventionellen Therapien verglichen.
„AG-221 ist bestätigt seine Wirksamkeit und Verträglichkeit bei einer weiter wachsenden Patientenzahl.“ Dr. Thomas Schroeder
Fazit
- AG-221 scheint seine Wirksamkeit mindestens zum Teil über einen neuartigen antileukämischen Effekt zu vermitteln.
- Basierend auf einer bisher positiven Nutzen-Risiko-Relation wird AG-221 nun in einer randomisierten Phase-III-Studie getestet.
Der Multikinaseinhibitor Midostaurin in Kombination mit konventioneller Chemotherapie verbessert das Outcome von AML-Patienten mit FLT3-Mutation
Etwa 30 % der AML-Patienten weisen zum Zeitpunkt der Erstdiagnose eine aktivierende Mutation in der FLT3-Tyrosinkinase (FLT3-ITD+ oder FLT3-TKD+; ITD = internal tandem duplication; TKD = tyrosine kinase domain) auf. Insbesondere die FLT3-ITD-Mutation geht mit einer hohen Rezidivrate und einer schlechten Prognose einher.
Als nächster Schritt hin zu einer personalisierten Therapie der AML wurden auf der Basis des molekularen Wissens Studien mit verschiedenen Tyrosinkinaseinhibitoren zur Behandlung der FLT3-positiven AML initiiert. Einer davon ist Midostaurin, das zwar im Vergleich mit anderen Molekülen nicht die höchste inhibierende Potenz gegen FLT3 aufweist, jedoch sowohl gegen die ITD- als auch die TKD-Mutation sowie gegen andere Rezeptorkinasen (vascular endothelial growth factor receptor [VEGFR], Proteinkinase C [PKC], KIT und platelet-derived growth factor receptor [PDGFR]) wirkt. In der diesjährigen Plenary-Session wurden die Resultate der bisher größten randomisierten Studie hierzu vorgestellt (RATIFY-Studie) [8]. In dieser multinationalen Studie wurden insgesamt 717 Patienten mit neudiagnostizierter FLT3-mutierter AML (Alter 18–60 Jahre) eingeschlossen. Von diesen erhielten 355 Patienten nach Randomisierung Midostaurin (50 mg 2-mal täglich p. o. für 21 bzw. 28 Tage) und 354 Patienten Placebo zusätzlich zur Standardbehandlung (bestehend aus Induktions- und Konsolidierungschemotherapien). Außerdem war eine einjährige Erhaltungstherapie mit Midostaurin oder Placebo vorgesehen. Die Datenanalyse nach 357 eingetretenen Ereignissen zeigte, dass Midostaurin trotz einer vergleichbaren Tag-60-Remissionsrate zu einem signifikant verlängerten Gesamt- (primärer Endpunkt, Abb. 2), ereignisfreien und krankheitsfreien Überleben führte. Hieraus ergab sich ein um 23 % geringeres Risiko für das Ereignis Tod im Midostaurin-Arm (Hazard Ratio 0,77; p = 0,0074). Dieser Vorteil zugunsten von Midostaurin bestand auch weiter, wenn die innerhalb der Studie transplantierten Patienten zum Zeitpunkt der Transplantation zensiert wurden. Dieser therapeutische Benefit war nicht mit einer gesteigerten Toxizität gekoppelt. Als einzige substanzspezifische Nebenwirkung wurden vermehrt Hautausschläge verzeichnet. Die Autoren schlussfolgerten zu Recht, dass Midostaurin ein neuer Bestandteil der Standardbehandlung von AML-Patienten mit FLT3-Mutation werden könnte. Basierend auf diesen Daten wird nun seitens der Firma die Zulassung angestrebt.
Bei der Interpretation dieser positiven Daten muss jedoch ein wesentlicher Punkt bedacht werden. Während der über 10-jährigen Konzeptions- und Laufzeit der RATIFY-Studie hat sich der Therapiealgorithmus für diese Patienten geändert: Mittlerweile wird die allogene Transplantation in erster Remission, und nicht mehr die in der Studie noch vorgesehene Chemotherapie als Konsolidierungstherapie der ersten Wahl angesehen. Dies hat die einarmige 16/10-Studie der deutschen AML-Studiengruppe berücksichtigt [9]. Auch in dieser Studie erhielten die AML-Patienten mit FLT3-Mutation Midostaurin additiv zur Standardbehandlung. Insgesamt zeigte auch diese Studie ein vielversprechendes Ansprechen und Gesamtüberleben für diese Hochrisiko-Patientengruppe und unterstreicht somit die Daten der RATIFY-Studie.
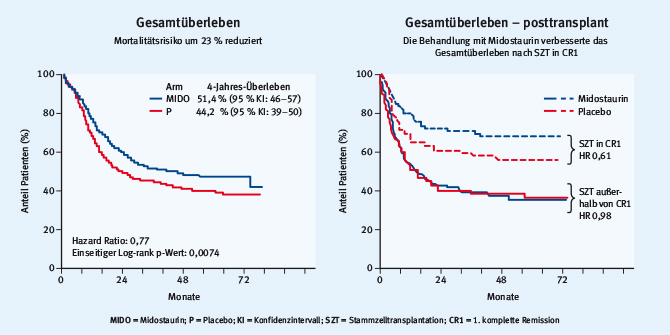 Abb. 2: Gesamtüberleben aller Patienten (links) und nach Zensierung der Patienten zum Zeitpunkt der allogenen Transplantation (rechts) bei AML-Patienten, die mit Midostaurin oder Placebo zusätzlich zur Standardbehandlung behandelt wurden (modifiziert nach [8]).
Abb. 2: Gesamtüberleben aller Patienten (links) und nach Zensierung der Patienten zum Zeitpunkt der allogenen Transplantation (rechts) bei AML-Patienten, die mit Midostaurin oder Placebo zusätzlich zur Standardbehandlung behandelt wurden (modifiziert nach [8]).
„Die Hinzunahme von Midostaurin zur Standardbehandlung von AML-Patienten mit FLT3-Mutation könnte neuer Standard werden.“ Dr. Thomas Schroeder
Fazit
- Der Tyrosinkinaseinhibitor Midostaurin ist bei guter Verträglichkeit in Kombination mit der Standardbehandlung der FLT3+ AML wirksam.
- Möglicherweise steht mit Midostaurin eine der wenigen Zulassungen auf dem Gebiet der AML an.
Quellen
- Bejar R, Papaemmanuil E, Haferlach T et al. Somatic Mutations in MDS Patients Are Associated with Clinical Features and Predict Prognosis Independent of the IPSS-R: Analysis of Combined Datasets from the International Working Group for Prognosis in MDS-Molecular Committee. ASH 2015, Orlando, abstract 907.
- Platzbecker U, Germing U, Giagounidis A et al. ACE-536 Increases Hemoglobin and Reduces Transfusion Burden in Patients with Low or Intermediate-1 Risk Myelodysplastic Syndromes (MDS): Preliminary Results from a Phase 2 Study. ASH 2014, San Franciso, abstract 411.
- Giagounidis A, Platzbecker U, Germing U et al. Luspatercept Treatment Leads to Long Term Increases in Hemoglobin and Reductions in Transfusion Burden in Patients with Low or Intermediate-1 Risk Myelodysplastic Syndromes (MDS): Preliminary Results from the Phase 2 PACE-MDS Extension Study. ASH 2015, Orlando, abstract 92.
- Giagounidis A, Mufti GJ, Fenaux P et al. Results of a randomized, double-blind study of romiplostim versus placebo in patients with low/intermediate-1-risk myelodysplastic syndrome and thrombocytopenia. Cancer 2014; 120: 1838-1846.
- Oliva EN, Santini V, Alati C et al. Eltrombopag for the Treatment of Thrombocytopenia of Low and Intermediate-1 IPSS Risk Myelodysplastic Syndromes: Interim Results on Efficacy, Safety and Quality of Life of an International, Multicenter Prospective, Randomized, Trial. ASH 2015, Orlando, abstract 91.
- Stein EM, Altman JK, Collins R et al. AG-221, an Oral, Selective, First-in-Class, Potent Inhibitor of the IDH2 Mutant Metabolic Enzyme, Induces Durable Remissions in a Phase I Study in Patients with IDH2 Mutation Positive Advanced Hematologic Malignancies. ASH 2014, San Franciso, abstract 115.
- Stein EM, DiNardo C, Altman JK et al. Safety and Efficacy of AG-221, a Potent Inhibitor of Mutant IDH2 That Promotes Differentiation of Myeloid Cells in Patients with Advanced Hematologic Malignancies: Results of a Phase 1/2 Trial. ASH 2015, Orlando, abstract 323.
- Stone RM, Mandrekar S, Sanford BL et al. The Multi-Kinase Inhibitor Midostaurin (M) Prolongs Survival Compared with Placebo (P) in Combination with Daunorubicin (D)/Cytarabine (C) Induction (ind), High-Dose C Consolidation (consol), and As Maintenance (maint) Therapy in Newly Diagnosed Acute Myeloid Leukemia (AML) Patients (pts) Age 18-60 with FLT3 Mutations (muts): An International Prospective Randomized (rand) P-Controlled Double-Blind Trial (CALGB 10603/RATIFY [Alliance]). ASH 2015, Orlando, abstract 6.
- Schlenk R, Döhner K, Salih H et al. Midostaurin in Combination with Intensive Induction and As Single Agent Maintenance Therapy after Consolidation Therapy with Allogeneic Hematopoietic Stem Cell Transplantation or High-Dose Cytarabine (NCT01477606). ASH 2015, Orlando, abstract 322.
- Bildnachweis: „Architectural detail of Modern Building in Orlando, Florida, USA”: © murmakova/Fotolia
Maligne Lymphome: Neue Substanzen und differenzierte Diagnostik auf dem Weg zur klinischen Routine
Priv.-Doz. Dr. med. Georg Heß, Universitätsmedizin Mainz
 Maligne Lymphome weisen immer noch eine hohe krankheitsbezogene Mortalität auf. Umso erfreulicher ist es, dass sich auf diesem Feld weiterhin zahlreiche innovative und vielversprechende Therapieoptionen entwickeln. Jedoch hat es in diesem Jahr keine Arbeit aus dem Bereich „maligne Lymphome“ in die Plenary Session geschafft – ein Zeichen dafür, dass sich die neuen Substanzen häufig noch in einer frühen Entwicklung befinden und bestätigende Ergebnisse noch ausstehen. Deshalb hatten viele Präsentationen Ergebnisse früher Phase-I- und -II-Studien zum Inhalt, die häufig das Potential der neuen Substanzen oder innovativer Kombinationen aufzeigten, aber auch die eine oder andere Idee endgültig von der Liste potentieller Therapieoptionen eliminierte.
Maligne Lymphome weisen immer noch eine hohe krankheitsbezogene Mortalität auf. Umso erfreulicher ist es, dass sich auf diesem Feld weiterhin zahlreiche innovative und vielversprechende Therapieoptionen entwickeln. Jedoch hat es in diesem Jahr keine Arbeit aus dem Bereich „maligne Lymphome“ in die Plenary Session geschafft – ein Zeichen dafür, dass sich die neuen Substanzen häufig noch in einer frühen Entwicklung befinden und bestätigende Ergebnisse noch ausstehen. Deshalb hatten viele Präsentationen Ergebnisse früher Phase-I- und -II-Studien zum Inhalt, die häufig das Potential der neuen Substanzen oder innovativer Kombinationen aufzeigten, aber auch die eine oder andere Idee endgültig von der Liste potentieller Therapieoptionen eliminierte.
Welche Substanzen stehen im Fokus?
Weiterhin stehen insbesondere die Tyrosinkinaseinhibitoren stark im Mittelpunkt, allerdings gab es auch sehr spannende Präsentationen zu CAR-T-Zellen, die den Weg zu echten individualisierten Therapieregimen weisen könnten. Weniger Daten fanden sich in diesem Jahr für „klassische“ monoklonale Antikörper und Immunkonjugate. Hier stehen die Ergebnisse großer Studien noch aus – insbesondere zu Zweitgeneration-anti-CD20-Antikörpern.
Zunächst aber ein kurzer Blick auf die spannendsten Daten des Kongresses:
Was waren die Highlights?
- Ibrutinib vs. Temsirolimus beim Mantelzelllymphom [1]: In dieser randomisierten Studie konnten die vielversprechenden Daten von Ibrutinib beim rezidivierten Mantelzelllymphom (MCL) bestätigt werden. Das mediane progressionsfreie Überleben (PFS) war – bei einer prognostisch etwas günstigeren Patientengruppe – mit mehr als 14 Monaten besser als in vorausgegangenen Untersuchungen.
- Venetoclax-Monotherapie [2]: Der BCL-2-Inhibitor Venetoclax scheint auch einen Stellenwert bei der Behandlung bestimmter Untergruppen nodaler Lymphome zu haben. Insbesondere die Daten zum Mantelzelllymphom sind hier interessant.
- REModl-B [3]: Diese Studie zeigte wegweisend, wie die molekulare Diagnostik in aktuelle Konzepte integriert werden kann. Für diesen Ansatz besteht Hoffnung auf eine Umsetzung im klinischen Alltag.
Was ist gescheitert?
Einige Medikamente haben sich wahrscheinlich endgültig aus der Weiterentwicklung von Behandlungsoptionen maligner Lymphome verabschiedet, zum Beispiel Alisertib bei den T-Zell-Non-Hodgkin-Lymphomen (T-NHL) [4] und Bortezomib beim diffus großzelligen Lymphom (DLBCL) [3].
Diffus großzelliges Lymphom (DLBCL)
Die höchste therapeutische Not herrscht weiterhin bei Patienten mit Rezidiv eines aggressiven Lymphoms. Eine Nachanalyse der CORAL-Studie unterstrich dies noch einmal nachdrücklich [5]. Im Rahmen dieser Studie konnten DLBCL-Patienten im transplantationsfähigen Alter nur zu 50 % einer Hochdosistherapie zugeführt werden. Von dieser Hälfte aller eingeschlossenen Patienten erlitt wiederum die Hälfte ein Rezidiv – zum Teil mit sehr kurzer Latenz (Abb. 1). Das bedeutet, dass es selbst unter Studienbedingungen nur bei einem Viertel der Patienten gelingt, im Rezidiv erfolgreich zu therapieren. Es zeigte sich, dass insbesondere bei einem frühen Rezidiv nach Hochdosistherapie das Überleben in der Regel nur noch wenige Monate betrug. Diese Resultate zeigen die Notwendigkeit, alle Optionen zur Rezidivvermeidung auszuschöpfen.
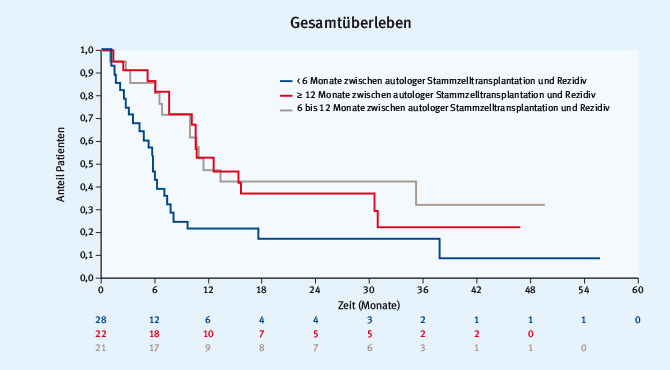 Abb. 1: Gesamtüberleben (Monate) bei DLBCL-Patienten nach autologer Stammzelltransplantation und Rezidiv (modifiziert nach [5]).
Abb. 1: Gesamtüberleben (Monate) bei DLBCL-Patienten nach autologer Stammzelltransplantation und Rezidiv (modifiziert nach [5]).Auch wenn sich die Diskussion heute hauptsächlich den neuen Substanzen widmet, bleibt die Chemotherapie das zentrale Element der Therapie aggressiver Lymphome. Die Optimierung des therapeutischen Vorgehens ist dabei noch nicht abgeschlossen. Die Ergebnisse von dosisadjustiertem EPOCH-R bei Patienten mit Burkitt-Lymphom waren vor 2 Jahren nach der Publikation im NEJM aufgrund der geringen Fallzahl und des monozentrischen Charakters der Studie noch mit einer gewissen Zurückhaltung aufgenommen worden [6].
Nun wurde ein Update der Studie mit erhöhter Patientenzahl im multizentrischen Ansatz vorgestellt [7]. In der Studie kam zusätzlich ein risikoadaptiertes Vorgehen zum Einsatz, für Patienten mit PET-Negativität im Zwischenstaging war eine verkürzte Therapie vorgesehen. Insgesamt wurden die Ergebnisse von 88 Patienten vorgestellt: medianes Alter 46 Jahre, ZNS-Befall (leptomeningeal) bei 13 % der Patienten, 24 % der Patienten waren HIV-positiv. Erneut zeigten sich sehr gute Ergebnisse für die Therapie, insbesondere bei Niedrigrisikopatienten (PFS 100 % bei Niedrigrisiko- bzw. 81 % bei Hochrisikopatienten; Gesamtüberleben [OS] 100 % bzw. 84 %). Es wurden keine Unterschiede zwischen HIV-positiven und -negativen Patienten beobachtet. Die Toxizität des Verfahrens scheint gegenüber dem in Deutschland in der Regel verwendeten B-ALL-Protokoll geringer zu sein. Ein randomisierter Vergleich der Therapien wäre insbesondere unter diesem Aspekt interessant. Fraglich scheint, ob die in der Studie verwendete niedrigdosierte intrathekale Methotrexat-Gabe als ausreichend betrachtet werden kann.
Mit der erfolgreichen Einführung von Brentuximab hat die Klasse der Immunkonjugate Einzug in die Therapie maligner Lymphome gehalten. Verschiedene weitere Konstrukte sind in der klinischen Entwicklung. Denintuzumab Mafodotin (SGN-CD19A) ist ein CD19-Antikörper, der an Monomethylauristatin F (MMAF) gekoppelt ist, einem synthetischen Mitoseinhibitor. Aufgrund der universellen Expression von CD19 ist er für die Behandlung verschiedenster Lymphomentitäten interessant.
In einer Phase-II-Studie wurden 62 Patienten mit Denintuzumab Mafodotin behandelt (85 % DLBCL, 8 % MCL, 5 % follikuläres Lymphom [FL], medianes Alter 65 Jahre, median 2 Vortherapien, 60 % refraktär auf die letzte Vortherapie) [8]. Bei diesen Patienten wurden 2 verschiedene Dosisschemata getestet, ein drei- und ein sechswöchiges Regime. Bei diesem Kollektiv zeigte sich für die Patienten mit rezidivierter Erkrankung eine Ansprechrate von 60 % (40 % komplette Remission [CR]) und bei refraktären Patienten eine – nicht überraschend – geringere Ansprechrate von 23 % (11 % CR). Die mediane Ansprechdauer lag bei 39 Wochen für rezidivierte und 41 Wochen für refraktäre Patienten. Neben den häufig zu beobachtenden Nebenwirkungen mit einer vergleichsweise geringen Rate an Zytopenien zeigten sich insbesondere ophthalmologische Probleme im Sinne einer superfiziellen mikrozystischen Keratopathie. Auch wenn die Veränderungen unter topischer Behandlung rückläufig waren, kann dies für die Einbindung in frühe Kombinationskonzepte – was durchaus attraktiv wäre – limitierend sein und muss engmaschig beobachtet werden.
CAR-T-Zellen haben in den vergangenen Jahren schon große Aufmerksamkeit erzielt. Bei diesem individualisierten Therapieverfahren werden autologe T-Zellen mit einem CD19-spezifischen chimären Antigenrezeptor versehen. Die Spezifität des Antikörpers, verbunden mit der Aktivierung der T-Zellen durch kostimulatorische Moleküle, macht die retransfundierten T-Zellen in hohem Maß aktiv gegenüber entsprechenden T-Zellen. Durch Persistenz dieser Zellen ergibt sich die grundsätzliche Möglichkeit einer langfristigen Tumorkontrolle. Frühere Ergebnisse bei der CLL oder dem MCL haben die Wirksamkeit dieses Prinzips bereits gezeigt. Problematisch bei ersten Einsätzen waren jedoch insbesondere Komplikationen wie Tumorlysesyndrom (TLS), Cytokine Release Snydrom (CRS) oder Neurotoxizitäten. Auf dem ASH wurden nun Ergebnisse laufender Therapieprotokolle vorgestellt.
In eine Studie der Gruppe der University of Pennsylvania wurden Patienten mit fortgeschrittenem Lymphom (DLBCL, FL, MCL) und fehlender kurativer Option eingeschlossen [9]. Die Patienten erhielten ein bis vier Tage nach einer lymphozytendepletierenden Chemotherapie eine einzige Infusion transfizierter T-Zellen. Ziel der Studie war die Untersuchung des Ansprechens nach 3 Monaten. Die Ergebnisse wurden nach Entität getrennt präsentiert. Insgesamt wurden 43 Patienten mit einem rezidivierten DLBC eingeschlossen (medianes Alter 54,5 Jahre, im Median 3 Vortherapien, 35 % der Patienten mit vorausgegangener Hochdosistherapie, 15 Patienten erhielten eine lymphozytendepletierende Therapie). Zum Zeitpunkt der Vorstellung lagen Ergebnisse von 15 Patienten vor. Drei Monate nach Therapie zeigte sich eine Ansprechrate von 47 %, davon erreichten 3 Patienten eine komplette Remission (Tab. 1). Interessanterweise hatte keiner dieser Patienten nach einem Jahr ein Rezidiv, was das Potential des Verfahrens zeigt. Auch für die 14 Patienten mit FL (medianes Alter 59 Jahre, 5 Vortherapien) zeigte sich eine sehr gute Ansprechrate von 73 % (CR 36 %). Das mediane progressionsfreie Überleben bei kurzer Nachbeobachtung war noch nicht erreicht. Jedoch zeigte sich erneut das mögliche Nebenwirkungsprofil: 16 Patienten hatten eine CRS und 3 Patienten zum Teil schwere neurologische Toxizitäten.
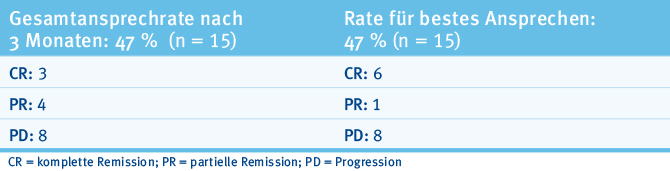 Tab. 1: Ansprechraten einer Behandlung mit CAR-T-Zellen bei Patienten mit DLBCL (modifiziert nach [9]).
Tab. 1: Ansprechraten einer Behandlung mit CAR-T-Zellen bei Patienten mit DLBCL (modifiziert nach [9]).Eine ähnliche Arbeit der Gruppe am Fred Hutchinson Cancer Center in Seattle untersuchte insbesondere den Einfluss verschiedener lymphodepletierender Strategien und unterschiedlicher T-Zell-Dosen [10]. 39 Patienten mit B-Zell-Lymphom oder CLL wurden in die Studie eingeschlossen. Vorgestellt wurden die Ergebnisse von 30 Patienten. Auch hier fand sich ein insgesamt gutes Ansprechen (ORR 63 %; CR 33 %). Interessant war insbesondere die Korrelation verbesserten Ansprechens mit der Nutzung einer Cyclophosphamid/Fludarabin-haltigen Induktion und dem Einsatz höherer T-Zell-Dosen, wobei hohe Dosen mit einer dosislimitierenden Toxizität assoziiert waren. Eine Neurotoxizität trat bei 33 % der Patienten auf.
„Insgesamt bestätigen diese Arbeiten das hohe Potential von CAR-T-Zellen zur Therapie von Lymphomen. Sie belegen aber auch die Notwendigkeit einer Anwendung in erfahrenen Behandlungszentren, der Ausarbeitung optimaler Therapieregime und den Einbezug von Supportivtherapien. In den kommenden Jahren wird das Therapieverfahren auch in Europa bzw. in Deutschland zur Verfügung stehen und für geeignete Patienten eine attraktive Therapieoption sein.“ PD Dr. Georg Heß
Kein Stellenwert für den Einsatz von Bortezomib bei aggressiven Lymphomen
Seit Jahren wurde der mögliche Stellenwert von Bortezomib für insbesondere sogenannte non-GCB-Lymphome (GCB = germinal center B-cell-like) diskutiert und in verschiedenen Studien evaluiert. Aktuell wurden nun die Ergebnisse zweier Studien vorgestellt, die dieser Fragestellung nachgingen.
Leonard [11] stellte die Ergebnisse der Pyramid-Studie vor, bei der R-CHOP +/- Bortezomib für Patienten mit non-GCB-DLBCL untersucht wurde. Die Diagnose wurde in diesem Konzept anhand der Immunhistochemie getroffen (sogenannter Hans-Classifier). Insgesamt wurden 206 Patienten in die Studie eingeschlossen, von denen 186 auswertbar waren. Kurz gefasst zeigten die Ergebnisse keinen Unterschied bei Ansprechrate, progressionsfreiem Überleben und Gesamtüberleben im Vergleich der beiden Gruppen – weder in der Gesamtgruppe noch für die ca. 50 % Hochrisikopatienten.
Die Studie der britischen und schweizerischen Lymphomgruppe wendete einen etwas anderen Ansatz an, bei dem insbesondere die Evaluation des molekularen Subtyps mithilfe des gene expression profiling (GEP) implementiert war. Davies stellte die Daten dieser „REMoDL-B“-Studie vor [3]. Alle eingeschlossenen Patienten (nicht sehr gutes Risiko, DLBCL, Erstdiagnose) wurden zunächst mit einem Zyklus R-CHOP behandelt. Während dieser Zeit erfolgte die Evaluation des molekularen Subtyps mithilfe des oben genannten Verfahrens. Von 1.132 Patienten konnten 1.085 Patienten randomisiert werden – eine beeindruckende Leistung, die Diagnostik so zuverlässig zur Verfügung zu stellen. Von den erfolgreich analysierten Patienten hatten 51 % ein GCB, 26,8 % ein ABC (activated B-cell-like) und 21,7 % ein unklassifiziertes DLBCL. Alle Patienten mit erfolgreicher molekularer Analyse wurden für 5 weitere Zyklen zwischen R-CHOP und RB-CHOP randomisiert. Diese Studie hatte somit mehrere große Vorteile: erstens ein präzises molekulares Verfahren und zweitens eine Evaluation des Effektes nicht nur in einer Gesamtkohorte, sondern auch getrennt für alle Subtypen. Die Ergebnisse waren ebenso eindeutig wie ernüchternd. Es zeigte sich kein Vorteil zugunsten der Hinzunahme von Bortezomib bezüglich Ansprechen, Progressionsrate oder Überleben.
„Die große Fallzahl und die sehr gute Studiendurchführung der REMoDL-B-Studie legen nahe, dass Bortezomib keinen Stellenwert bei der Behandlung des DLBCL hat.“ PD Dr. Georg Heß
Darüber hinaus wurden weitere interessante Resultate zu Verbesserungen der Primärtherapie präsentiert. Exemplarisch ausgewählt brachte die Kombination von Everolimus mit R-CHOP im Rahmen einer Phase-II-Studie bei DLBCL mit noch kleiner Patientenzahl (und zumeist gutem Risikoprofil) ein Ansprechen von 100 % in der MTD-Kohorte (MTD = maximal tolerable Dosis), wobei alle Patienten eine CR erreichten [12]. Mit den erwarteten Ergebnissen zu Lenalidomid, Ibrutinib und Obinotuzumab in der Primärtherapie ergeben sich hier in den kommenden Jahren Erkenntnisse, die eine Verbesserung der Primärtherapie realistisch erscheinen lassen.
Für den Bereich der DLBCL des ZNS wurden spannende Daten vorgestellt [13]. Als neues Behandlungskonzept wurde in dieser Arbeit ein Protokoll speziell für ZNS-Lymphome präsentiert, das auf DA-EPOCH basiert. Es zeichnet sich durch einen Austausch verschiedener Medikamente durch liquorgängige Substanzen und die Hinzunahme von Ibrutinib, das die Blut-Hirn-Schranke durchdringen kann, aus. Dieses sogenannte Dose adjusted TEDDIR-Protokoll zeigte eine überraschend gute Wirksamkeit mit zum Teil im Rezidiv lang anhaltenden kompletten Remissionen – bei zum Zeitpunkt der Vorstellung noch geringer Fallzahl – und soll in Zukunft in einem multizentrischen Rahmen weiter entwickelt werden. Spannend wird zu beobachten sein, ob eine zielgerichtete Substanz die Prognose der Patienten mit diesem schwierigen Krankheitsbild wirklich verbessern kann.
Fazit
- Nur bei einem Viertel der DLBCL-Patienten ist eine Rezidivtherapie erfolgreich. Es gilt daher, alle Möglichkeiten zur Vermeidung von Rezidiven auszuschöpfen.
- Eine dosisadjustierte Chemotherapie nach dem EPOCH-R-Schema zur Behandlung von Burkitt-Lymphomen ist wirksam und vielversprechend gut verträglich. Ein Vergleich mit dem in Deutschland in der Regel verwendeten B-ALL-Protokoll wäre attraktiv.
- Denintuzumab Mafodotin ist eine interessante Option zur Behandlung von B-NHL. Als ungewöhnliche Nebenwirkung ist auf eine superfizielle mikrozystische Keratopathie zu achten, die topisch therapiert werden kann.
- CAR-T-Zellen haben ein großes Potential zur Therapie von Lymphomen, sollten aber nur in erfahrenen Behandlungszentren zum Einsatz kommen.
- Bortezomib hat keinen Stellenwert bei der Behandlung des DLBCL.
- Die Verwendung liquorgängiger zielgerichteter Substanzen wie Ibrutinib kann richtungsweisend für eine Verbesserung der Therapieergebnisse bei ZNS-Lymphomen sein.
Follikuläres Lymphom (FL)
Die Inhibition von bcl-2 hat in den letzten Jahren eine zunehmende Aufmerksamkeit erlangt, insbesondere nachdem mit Venetoclax (früher ABT-199) eine Substanz zur Verfügung steht, die nicht mehr die Thrombopenierate aufweist, die bei früheren Generationen von bcl-2-Inhibitoren beobachtet wurde. Bisher zeigte sich insbesondere bei der CLL eine zum Teil überraschend gute Ansprechrate (zum Beispiel in einer aktuellen Arbeit im NEJM [14]). Auch ein Einsatz bei anderen Lymphomentitäten ist attraktiv, insbesondere auch beim FL wegen der dominanten bcl-2-Expression. In einer Phase-I-Studie wurden 70 Patienten mit rezidiviertem oder refraktärem Lymphom (20 DLBCL; 14 FL; 28 MCL; 4 Morbus Waldenström [MW]; 3 Marginalzonenlymphom [MZL]; 1 Multiples Myelom [MM] mit einer Venetoclax-Monotherapie behandelt und eine Dosiseskalation auf 1.200 mg Tagesdosis evaluiert [2]. In dieser Dosisstufe wurden nochmals 36 Patienten behandelt (21 DLBCL; 15 FL).
Die beobachteten Nebenwirkungen entsprachen bisherigen Erfahrungen: gastrointestinale Beschwerden, Anämie, Hyponatriämie und 2 Patienten mit laborbasiertem TLS. Dosislimitierend war das Auftreten von Neutropenien. Beim Ansprechen ergab sich ein differenziertes Bild: insbesondere Patienten mit MCL und MW sprachen gut an. Bei Patienten mit follikulärem Lymphom zeigte sich zwar bei 97 % der Patienten eine Krankheitsstabilisierung oder besseres Ansprechen, die objektive Ansprechrate lag jedoch nur bei 38 %, was vergleichsweise enttäuschend war. Noch schlechter waren die Ergebnisse für das DLBCL, bei dem nur 18 % der Patienten ein Ansprechen zeigten (Tab. 2). Ein wesentlicher Aspekt kann jedoch in der Auswahl der richtigen Dosis liegen, da bei höheren Dosen ein höheres Ansprechen gesehen wurde. Entsprechende weiterführende Ergebnisse sind von hohem Interesse. Beachtenswert war die lange Remissionsdauer bei Patienten, die eine CR erreichten. Mit diesen Resultaten erlangen die Ergebnisse der laufenden Kombinationsstudien, die aufgrund des Wirkmechanismus von Venetoclax besonders attraktiv erscheinen, eine besondere Bedeutung.
Die Ergebnisse einer solchen kleinen Phase-I-Kombinationsstudie bei verschiedenen Lymphomentitäten wurde bereits von de Vos vorgestellt [15]. Die Kombination bestand aus Bendamustin-Rituximab plus Venetoclax. Von den 48 Patienten in dieser Studie zeigte sich insbesondere bei den Patienten mit FL ein vielversprechendes Ansprechen (87 % CR + PR; n = 20) bei guter Verträglichkeit. Wenn die Resultate der Contralto-Studie vorliegen, können diese Ergebnisse möglicherweise bestätigt werden.
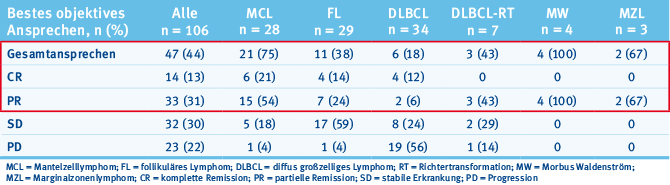 Tab. 2: Patienten mit rezidiviertem oder refraktärem Lymphom, Behandlung mit einer Venetoclax-Monotherapie: objektives Ansprechen (alle Dosierungen) nach Histologie (modifiziert nach [2]).
Tab. 2: Patienten mit rezidiviertem oder refraktärem Lymphom, Behandlung mit einer Venetoclax-Monotherapie: objektives Ansprechen (alle Dosierungen) nach Histologie (modifiziert nach [2]).Der Quervergleich zu Kombinationen mit Tyrosinkinaseinhibitoren lässt Interessantes erwarten. Für Ibrutinib wird bei verschiedenen Lymphomentitäten ein hoher Stellenwert erwartet. Erste Ergebnisse bei nodalen Lymphomen waren jedoch nicht einheitlich positiv. Deshalb ist es besonders interessant, diese Substanz in verschiedenen Kombinationen zu evaluieren.
Erste Daten zur Kombination von Ibrutinib mit Rituximab bei FL-Patienten wurden nun vorgestellt [16]. Dabei wurde Ibrutinib in einer Dosis von 560 mg eingesetzt, jedoch weitgehend bei Patienten mit niedriger Tumorlast. Insgesamt zeigte sich ein Ansprechen von 82 %, wobei eine substantielle Anzahl kompletter Remissionen erreicht wurde. Weitere Ergebnisse insbesondere randomisierter Studien bleiben abzuwarten. Interessant werden auch die Ergebnisse der von der German Low-Grade Lymphoma Study Group (GLSG) geplanten Kombination mit GA-101 sein.
Fazit
- bcl-2-Inhibition mit Venetoclax ist eine vielversprechende Option zur Behandlung verschiedener Lymphomentitäten. Die derzeitige Datenlage ist aber noch uneinheitlich.
- Kombinationstherapien mit Tyrosinkinaseinhibitoren können die Behandlungsmöglichkeiten des FL erweitern und verbessern.
Mantelzelllymphom (MCL)
Gerade beim Mantelzelllymphom haben sich in den vergangenen Jahren zahlreiche neue Therapieoptionen ergeben. Bisher lagen randomisierte Vergleiche von Temsirolimus und Lenalidomid mit Chemotherapie vor, jetzt wurde erstmals der Vergleich von 2 nicht klassischen Chemotherapien gezeigt. Diese wegweisende Studie beim Mantelzelllymphom verglich randomisiert Ibrutinib mit Temsirolimus im Rezidiv und wurde nun zeitgleich auf dem ASH vorgestellt [1] und im Lancet publiziert [17]. Insgesamt wurden 280 Patienten im Rahmen der Studie randomisiert und erhielten jeweils eine Behandlung bis zur Progression oder bis zum Absetzen aufgrund von Unverträglichkeit. Um die Ergebnisse richtig einzuordnen, muss beachtet werden, dass die Patienten in beiden Armen im Median zwei Vortherapien erhalten hatten. Es zeigte sich ein deutlicher Unterschied in der Ansprechrate und dem progressionsfreien Überleben zugunsten von Ibrutinib (71,9 % vs. 40,4 %; 14,4 Monate vs. 6,2 Monate, Abb. 2), was eindeutig die Überlegenheit von Ibrutinib belegt und die Substanz zweifelsfrei zum neuen Standard für Patienten in der Rezidivsituation bei Chemotherapieversagen macht. Interessant war, dass Patienten, die in einer früheren Therapielinie Ibrutinib erhielten, ein besseres Ansprechen zeigten als bei Behandlung in einer späteren Linie, was ggf. den Vorteil eines frühen Einsatzes weiter unterstreicht. Klinisch spannend bleibt die Frage, wie mit den Patienten im Rezidiv nach Ibrutinib umgegangen werden soll. Eine zusätzliche Analyse zeigte, dass nur ca. 20 % der Patienten im Falle eines Rezidivs auf die nächste Therapie ansprachen. Dies wird sicher in der Zukunft eine der großen Herausforderungen bleiben.
„Die Frage, welche Optionen es bei einem Rezidiv nach Ibrutinib-Therapie gibt, ist eine der großen Herausforderungen für die Zukunft. Spannend wird auch sein, ob mit alternativen BTK-Inhibitoren eine bessere Wirksamkeit und/oder eine bessere Nebenwirkungsrate erzielt werden kann. Mit ACP-106 gibt es hier einen ersten vielversprechenden Kandidaten [18].“ PD Dr. Georg Heß
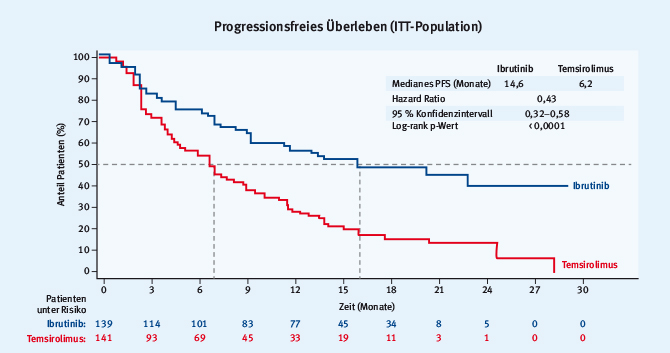 Abb. 2: Ibrutinib vs. Temsirolimus: progressionsfreies Überleben, ausgewertet durch einen unabhängigen Prüfungsausschuss (modifiziert nach [1]).
Abb. 2: Ibrutinib vs. Temsirolimus: progressionsfreies Überleben, ausgewertet durch einen unabhängigen Prüfungsausschuss (modifiziert nach [1]).Neben diesen sehr erfreulichen Daten zeigten zwei Untersuchungen, dass sich beim Einsatz von Bortezomib als Konsolidierungs-/Erhaltungstherapie nach Induktionstherapie in der Erstlinienbehandlung kein eindeutig positiver Trend ergibt. Die CALGB untersuchte in einem historischen Vergleich den Einsatz von Bortezomib bei MCL-Patienten nach einer Hochdosistherapie (HDT) als Konsolidierung oder als Erhaltungstherapie [19]. Dabei zeigte sich (bei der aufgrund der Methodik zurückhaltend zu bewertenden Analyse) ein Unterschied beim Vergleich mit einer historischen Kohorte zugunsten einer Konsolidierung, jedoch nicht beim Einsatz als Erhaltungstherapie.
Dies konnte auch die Arbeit der niederländischen Studiengruppe zeigen [20]. Hier fand sich ebenfalls kein Effekt einer zusätzlichen Bortezomib-Erhaltungstherapie beim MCL – bei allerdings kleiner Fallzahl.
„Mit der Verfügbarkeit neuer Therapieverfahren ergibt sich aus meiner Sicht kein ausreichender Stellenwert für den Einsatz von Bortezomib beim MCL als Konsolidierung oder Erhaltung. Weitere Studien in vergleichbarem Kontext sollten sich anderen Therapieansätzen widmen.“ PD Dr. Georg Heß
Mittlerweile liegen Ergebnisse zu einer Rituximab-Erhaltungstherapie für praktisch alle Patientengruppen vor, zuletzt die Daten der LyMa-Studie. Eine erste Subanalyse dieser Studie zum Stellenwert der MRD-Diagnostik zeigte verschiedene interessante Aspekte auf [21]. Zu erwarten war der positive Aussagewert einer MRD-Negativität, es scheint aber – mit noch unzureichendem Follow-up – insbesondere für MRD-positive Patienten eine Verbesserung durch eine Rituximabtherapie möglich zu sein. Die finalen Ergebnisse der Studie bleiben abzuwarten. Wenn sich diese aber bestätigen, wird eine Rituximab-Erhaltungstherapie auch nach einer HDT Standard werden.
Fazit
- Ibrutinib ist der neue Standard für MCL-Patienten in der Rezidivsituation bei Chemotherapieversagen.
- Momentan ist unklar, was MCL-Patienten im Rezidiv nach Ibrutinib therapeutisch angeboten werden kann.
- Bortezomib hat bei Patienten mit MCL keinen Stellenwert als Erhaltungstherapie.
- Es zeichnet sich ab, dass Rituximab der Erhaltungstherapiestandard nach Hochdosistherapie beim MCL werden könnte.
Morbus Hodgkin (MH)
Im vergangenen Jahr hatten die Daten zur anti-PD-1-Therapie beim M. Hodgkin großes Aufsehen erregt. In einem Update der Untersuchung wurden nun die Ergebnisse zu Nivolumab bei Patienten mit Morbus Hodgkin mit längerer Nachbeobachtung bestätigt (Gesamtansprechen 20/23, dauerhaftes Ansprechen 10/23) [22]. Dennoch zeigt sich, dass die Therapie mit Nivolumab im Rezidiv nicht bei allen Patienten zu einer dauerhaften Remission führt, was einen selektiven und möglicherweise früheren Einsatz der Substanz sinnvoll erscheinen lässt. In der von M. Roemer vorgestellten Arbeit wurde nun die Prävalenz von 9p24.1/PD-L1/PD-L2-Veränderungen in einer Gruppe neu diagnostizierter Patienten mit MH untersucht und eine mögliche prognostische Korrelation analysiert [14]. Bei der noch relativ kleinen Serie fand sich neben der Bestätigung der bekannten Risikofaktoren interessanterweise eine höhere Assoziation mit fortgeschrittenen Hodgkin-Stadien. Gleichzeitig war eine entsprechende Veränderung unabhängig von etablierten Risikofaktoren mit einer schlechteren Prognose assoziiert.
Nach den Daten des vergangenen Jahres zu Nivolumab konnte die Arbeit von P. Armand nun eine ähnliche Wirksamkeit für den Einsatz des anti-PD-1-Antikörpers Pembrolizumab aufzeigen [23]. In diese Studie wurden 31 Patienten eingeschlossen, mit einem hodgkintypischen medianen Alter von 32 Jahren. 68 % der Patienten hatten mehr als 3 Therapien erhalten, und 71 % hatten sich zuvor einer Hochdosistherapie unterzogen. Bei diesen deutlich vorbehandelten Patienten zeigte sich eine Ansprechrate von 65 % und eine Rate von 16 % kompletter Remissionen. Mit kurzer Nachbeobachtung verblieben 14 von 20 Patienten weiterhin unter Therapie. Zu beachten ist das Nebenwirkungsprofil. So fanden sich typische Nebenwirkungen wie Hypothyreose (16 %), Diarrhoe (13 %), Übelkeit (13 %) und Pneumonitiden (10 %). Ob es grundlegende Unterschiede der Wirksamkeit von Checkpoint-Modulatoren gibt oder Kombinationen die Effektivität noch steigern können, ist Aufgabe kommender Studiengenerationen. Erste Studien möglicher Kombinationen sind schon aktiv [24].
„Expressionsanalysen und die Definition von Hochrisikogruppen könnten in Zukunft eine rationale Strategie für die Berücksichtigung der Checkpoint-Modifier beim Hodgkin-Lymphom sein. Wirksam scheinen verschiedene Modulatoren zu sein – ob einer oder eine Kombination verschiedener die optimale Therapie darstellt, ist Frage zukünftiger Studienstrategien.“ PD Dr. Georg Heß
T-Zell-Lymphome
In den vergangenen Jahren hatten sich im Gegensatz zu den B-NHL nur wenige richtungsweisende Veränderungen bei den Therapieoptionen für das T-NHL ergeben. Der Stellenwert der HDAC-Inhibitoren, Pralatrexat und anderer neuer Medikamente ist bis heute nicht eindeutig geklärt. Auf dem diesjährigen ASH gab es dazu nun interessante Arbeiten.
Zum einen wurden die Ergebnisse einer Phase-III-Studie gezeigt, in der Alisertib – ein Aurorakinase-Inhibitor – mit konventioneller (HDAC-Inhibitoren, Gemcitabin) Therapie verglichen wurde. In einer Phase-II-Studie hatte sich zuvor ein Ansprechen von 30 % für das Medikament gezeigt [25]. Die aktuelle Studie wurde vorzeitig abgebrochen, da die erwartete Wirksamkeit des experimentellen Arms bei Weitem nicht erreicht werden konnte (Gesamtansprechen 34 %, erwartet worden waren 55 %) [4]. Somit muss diese Substanz aus dem Kreis der Therapieoptionen für das T-NHL gestrichen werden.
Überraschend positive Daten gab es hingegen zu einer Kombination von Belinostat mit CHOP für unbehandelte Patienten mit T-NHL [26]. Es zeigte sich eine überraschend gute Verträglichkeit sowie eine vielversprechende Ansprechrate von 86 % mit 67 % CR. Eine Phase-III-Studie ist nun geplant.
Fazit
- Der Aurorakinase-Inhibitor Alisertib zeigt bei der Behandlung von T-Zell-Lymphomen keine zufriedenstellende Ansprechrate und kann nicht als Therapieoption beim T-NHL angesehen werden.
- Die Kombination von Belinostat + CHOP bei unbehandelten Patienten mit T-NHL geht mit einer vielversprechenden Ansprechrate einher. Dies lenkt auch den Blick auf die aktuell bereits laufende randomisierte Therapiestudie mit der Kombination aus Romidepsin, einem weiteren HDAC-Inhibitor und CHOP.
Adulte T-Zell-Leukämie (ATL)
Patienten mit Rezidiv oder Hochrisiko-Subtyp eines ATL (Variante des peripheren T-Zell-Lymphoms, assoziiert mit humanem T-Zell-Leukämievirus Typ 1 [HTLV-1]) wurden im Rahmen einer Phase-II-Studie mit 25 mg/d Lenalidomid behandelt [27]. Von den 26 behandelten Patienten (medianes Alter 68 Jahre, median 2 Vortherapien inkl. Mogamulizumab bei 42 % der Patienten) sprachen 42 % auf die Therapie an. Zusätzlich zeigten 31 % zumindest eine stabile Erkrankung als bestes Ansprechen. Das mediane PFS lag allerdings bei 3,9 Monaten, womit einer Remission auf diese Therapie nach Möglichkeit eine definitive Konsolidierung folgen sollte.
Fazit
- Lenalidomid ist eine Therapieoption beim ALT, sollte bei Remission aber durch eine konsolidierende Therapie ergänzt werden.
- Auch wenn die bisherigen Daten von HDAC-Inhibitoren zumindest in Europa noch keinen großen Stellenwert der Substanzen zur Folge hatten, bleibt die Kombination mit konventioneller Chemotherapie eine aktuelle und spannende Frage.
Quellen
- Rule S, Jurczak W, Jerkeman M et al. Ibrutinib Vs Temsirolimus: Results from a Phase 3, International, Randomized, Open-Label, Multicenter Study in Patients with Previously Treated Mantle Cell Lymphoma (MCL). ASH 2015, Orlando, abstract 469.
- Gerecitano J, Roberts A, Seymour J et al. A Phase 1 Study of Venetoclax (ABT-199 / GDC-0199) Monotherapy in Patients with Relapsed/Refractory Non-Hodgkin Lymphoma. ASH 2015, Orlando, abstract 254.
- Davies A, Caddy J, Maishman T et al. A Prospective Randomised Trial of Targeted Therapy for Diffuse Large B-Cell Lymphoma (DLBCL) Based upon Real-Time Gene Expression Profiling: The Remodl-B Study of the UK NCRI and SAKK Lymphoma Groups (ISRCTN51837425). ASH 2015, Orlando, abstract 812.
- O'Connor OA, Özcan M, Jacobsen ED et al. First Multicenter, Randomized Phase 3 Study in Patients (Pts) with Relapsed/Refractory (R/R) Peripheral T-Cell Lymphoma (PTCL): Alisertib (MLN8237) Versus Investigator's Choice (Lumiere trial; NCT01482962). ASH 2015, Orlando, abstract 341.
- Van Den Neste E, Schmitz N, Mounier N et al. Outcomes in Diffuse Large B-Cell Lymphoma (DLBCL) Patients Relapsing after Autologous Stem Cell Transplantation (ASCT): An Analysis of Patients Included in the Coral Study. ASH 2015, Orlando, abstract 517.
- Dunleavy K, Pittaluga S, Shovlin M et al. Low-intensity therapy in adults with Burkitt's lymphoma. N Engl J Med 2013; 369: 1915-1925.
- Dunleavy K, Noy A, Abramson J et al. Risk-Adapted Therapy in Adults with Burkitt Lymphoma: Preliminary Report of a Multicenter Prospective Phase II Study of DA-EPOCH-R. Presented at ASH 2015, Orlando, abstract 342.
- Moskowitz C, Fanale M, Shah B et al. A Phase 1 Study of Denintuzumab Mafodotin (SGN-CD19A) in Relapsed/Refactory B-Lineage Non-Hodgkin Lymphoma. ASH 2015, Orlando, abstract 182.
- Schuster S, Svoboda J, Nasta S et al. Sustained Remissions Following Chimeric Antigen Receptor Modified T Cells Directed Against CD19 (CTL019) in Patients with Relapsed or Refractory CD19+ Lymphomas. ASH 2015, Orlando, abstract 183.
- Turtle C, Berger C, Sommermeyer D et al. Anti-CD19 Chimeric Antigen Receptor-Modified T Cell Therapy for B Cell Non-Hodgkin Lymphoma and Chronic Lymphocytic Leukemia: Fludarabine and Cyclophosphamide Lymphodepletion Improves In Vivo Expansion and Persistence of CAR-T Cells and Clinical Outcomes. Presented at ASH 2015, Orlando, abstract 184.
- Leonard J, Kolibaba K, Reeves J et al. Randomized Phase 2 Open-Label Study of R-CHOP ± Bortezomib in Patients (Pts) with Untreated Non-Germinal Center B-Cell-like (Non-GCB) Subtype Diffuse Large Cell Lymphoma (DLBCL): Results from the Pyramid Trial (NCT00931918). ASH 2015, Orlando, abstract 811.
- Johnston P, Laplant B, McPhail E et al. Everolimus Plus RCHOP-21 Is Safe and Highly Effective for New Untreated Diffuse Large B-Cell Lymphoma (DLBCL): Results of the Phase I Trial NCCTG1085 (Alliance). ASH 2015, Orlando, abstract 813.
- Dunleavy K, Lai C, Roschewski M et al. Phase I Study of Dose-Adjusted-Teddi-R with Ibrutinib in Untreated and Relapsed/Refractory Primary CNS Lymphoma. ASH 2015, Orlando, abstract 472.
- Roberts AW, Davids MS, Pagel JM et al. Targeting BCL2 with Venetoclax in Relapsed Chronic Lymphocytic Leukemia. N Engl J Med 2015.
- de Vos S, Swinnen L, Kozloff M et al. A Dose-Escalation Study of Venetoclax (ABT-199/GDC-0199) in Combination with Bendamustine and Rituximab in Patients with Relapsed or Refractory Non-Hodgkin's Lymphoma. ASH 2015, Orlando, abstract 255.
- Fowler N, Nastoupil L, de Vos S et al. Ibrutinib Plus Rituximab in Treatment-Naive Patients with Follicular Lymphoma: Results from a Multicenter, Phase 2 Study. ASH 2015, Orlando, abstract 470.
- Dreyling M, Jurczak W, Jerkeman M et al. Ibrutinib versus temsirolimus in patients with relapsed or refractory mantle-cell lymphoma: an international, randomised, open-label, phase 3 study. The Lancet.
- Byrd J, Wierda W, Jones J et al. The Bruton Tyrosine Kinase (Btk) Inhibitor ACP-196: Marked Activity in Relapsed/Refractory CLL with a Favorable Safety Profile. ASH 2015, Orlando, abstract 831.
- Kaplan L, Jung S, Stock W et al. Bortezomib Maintenance (BM) Versus Consolidation (BC) Following Aggressive Immunochemotherapy and Autologous Stem Cell Transplant (ASCT) for Untreated Mantle Cell Lymphoma (MCL): CALGB (Alliance)50403. ASH 2015, Orlando, abstract 337.
- Doorduijn J, Minnema M, Kersten M et al. Bortezomib Maintenance Therapy after Induction with R-CHOP, ARA-C and Autologous Stem Cell Transplantation in Newly Diagnosed MCL Patients, Results of a Multicenter Phase II HOVON Study. ASH 2015, Orlando, abstract 339.
- Callanan MB, Delfau MH, Macintyre E et al. Predictive Power of Early, Sequential MRD Monitoring in Peripheral Blood and Bone Marrow in Patients with Mantle Cell Lymphoma Following Autologous Stem Cell Transplantation with or without Rituximab Maintenance; Interim Results from the LyMa-MRD Project, Conducted on Behalf of the Lysa Group. ASH 2015, Orlando, abstract 338.
- Ansell S, Armand P, Timmerman J et al. Nivolumab in Patients (Pts) with Relapsed or Refractory Classical Hodgkin Lymphoma (R/R cHL): Clinical Outcomes from Extended Follow-up of a Phase 1 Study (CA209-039). ASH 2015, Orlando, abstract 583.
- Armand P, Shipp M, Ribrag V et al. PD-1 Blockade with Pembrolizumab in Patients with Classical Hodgkin Lymphoma after BrentuximabVedotin Failure: Safety, Efficacy, and Biomarker Assessment. ASH 2015, Orlando, abstract 584.
- Diefenbach C, Hong F, Cohen J et al. Preliminary Safety and Efficacy of the Combination of Brentuximab Vedotin and Ipilimumab in Relapsed / Refractory Hodgkin Lymphoma: A Trial of the ECOG-ACRIN Cancer Research Group (E4412). ASH 2015, Orlando, abstract 585.
- Barr PM, Li H, Spier C et al. Phase II Intergroup Trial of Alisertib in Relapsed and Refractory Peripheral T-Cell Lymphoma and Transformed Mycosis Fungoides: SWOG 1108. J Clin Oncol 2015; 33: 2399-2404.
- Johnston P, Cashen A, Nikolinakos P et al. Safe and Effective Treatment of Patients with Peripheral T-Cell Lymphoma (PTCL) with the Novel HDAC Inhibitor, Belinostat, in Combination with CHOP: Results of the Bel-CHOP Phase 1 Trial. Presented at ASH 2015, Orlando, abstract 253.
- Fujiwara H, Ishida T, Nosaka K et al. Multicenter Phase II Study of Lenalidomide in Patients with Relapsed Adult T-Cell Leukemia-Lymphoma. ASH 2015, Orlando, abstract 181.
- Bildnachweis: „Orlando morning”: © rabbit75_fot/Fotolia